Ахалазия кардии 3 степени что это
Ахалазия кардии
Ахалазия кардии – это отсутствие расслабления или недостаточное расслабление нижнего отдела пищевода нейрогенной этиологии. Сопровождается расстройством рефлекторного открытия кардиального отверстия во время акта глотания и нарушением попадания пищевых масс из пищевода в желудок. Ахалазия кардии проявляется дисфагией, регургитацией и болями в эпигастрии. Ведущими методами диагностики служат рентгеноскопия пищевода, эзофагоскопия, эзофагоманометрия. Консервативное лечение заключается в проведении пневмокардиодилатации; хирургическое – в выполнении кардиомиотомии.
МКБ-10
Общие сведения
Ахалазия кардии в медицинской литературе иногда обозначается терминами мегаэзофагус, кардиоспазм, идиопатическое расширение пищевода. Ахалазия кардии, по разным данным, в практической гастроэнтерологии составляет от 3 до 20% всех заболеваний пищевода. Среди причин, вызывающих нарушение проходимости пищевода, кардиоспазм стоит на третьем месте после рака пищевода и послеожоговых рубцовых стриктур.
Патология с одинаковой частотой поражает женщин и мужчин, чаще развивается в возрасте 20-40 лет. При ахалазии кардии в результате нервно-мышечных нарушений снижается перистальтика и тонус пищевода, не происходит рефлекторного расслабления пищеводного сфинктера при глотании, что затрудняет эвакуацию пищи из пищевода в желудок.
Причины
Выдвинуто множество этиологических теорий происхождения ахалазии кардии, которые связывают развитие патологии с врожденным дефектом нервных сплетений пищевода, вторичным повреждением нервных волокон при туберкулезном бронхоадените, инфекционных или вирусных заболеваниях; дефицитом витамина В и т. д. Распространена концепция нарушений центральной регуляции функций пищевода, рассматривающая ахалазию кардии как следствие нервно-психических травм, ведущих к расстройству корковой нейродинамики, иннервации пищевода, дискоординации в работе кардиального сфинктера. Однако до конца факторы, способствующие развитию заболевания, остаются невыясненными.
Ведущая роль в патогенезе ахалазии кардии отводится поражению отделов парасимпатической нервной системы, регулирующей моторику пищевода и желудка (в частности ауэрбаховского сплетения). Вторичная (симптоматическая) ахалазия кардии может быть вызвана инфильтрацией сплетения злокачественной опухолью (аденокарциномой желудка, гепатоцеллюлярным раком, лимфогранулематозом, раком легкого и др.). В ряде случаев ауэрбаховское сплетение может поражаться при миастении, гипотиреозе, полиомиозите, системной красной волчанке.
Патогенез
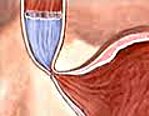
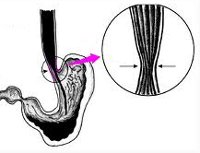
Фактическая денервация верхних отделов ЖКТ вызывает снижение перистальтики и тонуса пищевода, невозможность физиологического расслабления кардиального отверстия во время акта глотания, мышечную атонию. При таких нарушениях пища поступает в желудок только благодаря механическому раскрытию кардиального отверстия, происходящего под гидростатическим давлением жидких пищевых масс, скопившихся в пищеводе. Длительный застой пищевого комка приводит к расширению пищевода – мегаэзофагусу.
Морфологические изменения в стенке пищевода зависят от длительности существования ахалазии кардии. В стадии клинических проявлений отмечается сужение кардии и расширение просвета пищевода, его удлинение и S-образная деформация, огрубление слизистой оболочки и сглаживание складчатости пищевода. Микроскопические изменения при ахалазии кардии представлены гипертрофией гладкомышечных волокон, разрастанием в пищеводной стенке соединительной ткани, выраженными изменениями в межмышечных нервных сплетениях.
Классификация
По выраженности нарушений функций пищевода выделяют стадии компенсации, декомпенсации и резкой декомпенсации ахалазии кардии. Среди множества предложенных вариантов классификации наибольший клинический интерес представляет следующий вариант стадирования:
В соответствии с рентгенологическими признаками различают два типа ахалазии кардии. Первый тип патологии характеризуется умеренным сужением дистального отрезка пищевода, одновременной гипертрофией и дистрофией его циркулярных мышц. Дилатация пищевода выражена умеренно, участок расширения имеет цилиндрическую или овальную формы. Ахалазия кардии первого типа встречается у 59,2% пациентов.
О втором типе ахалазии кардии говорят при значительном сужении дистального участка пищевода, атрофии его мышечной оболочки и частичном замещении мышечных волокон соединительной тканью. Отмечается выраженное (до 16-18 см) расширение супрастенотического отдела пищевода и его S-образная деформация. Ахалазия кардии первого типа со временем может прогрессировать во второй тип. Знание типа ахалазии кардии позволяет гастроэнтерологам предусмотреть возможные трудности при проведении пневмокардиодилатации.
Симптомы ахалазии кардии
Клиническими проявлениями патологии служат дисфагия, регургитация и загрудинные боли. Дисфагия характеризуется затруднением глотания пищи. В некоторых случаях нарушение акта глотания развивается одномоментно и протекает стабильно; обычно дисфагии предшествует грипп или другое вирусное заболевание, стресс. У части пациентов дисфагия вначале носит эпизодический характер (например, при торопливой еде), затем становится более регулярной, затрудняющей прохождение как плотной, так и жидкой пищи.
Дисфагия при ахалазии кардии может быть избирательной и возникать при употреблении только определенного вида пищи. Приспосабливаясь к нарушению глотания, пациенты могут самостоятельно находить способы регуляции прохождения пищевых масс – задерживать дыхание, заглатывать воздух, запивать пищу водой и т. д. Иногда при ахалазии кардии развивается парадоксальная дисфагия, при которой прохождение жидкой пищи затрудняется в большей степени, чем твердой.
Регургитация при ахалазии кардии развивается в результате обратного заброса пищевых масс в полость рта при сокращении мышц пищевода. Выраженность регургитации может носить характер небольшого срыгивания или пищеводной рвоты, когда развивается обильное срыгивание «полным ртом». Регургитация может быть периодической (например, в процессе еды, одновременно с дисфагией), возникать сразу после приема пищи или спустя 2-3 часа после еды. Реже при ахалазии кардии заброс пищи может случаться во сне (так называемая, ночная регургитация): при этом пища нередко попадает в дыхательные пути, что сопровождается «ночным кашлем». Небольшая регургитация характерна для I – II стадии ахалазии кардии, пищеводная рвота – для III – IV стадий, когда происходит переполнение и перерастяжение пищевода.
Осложнения
Нарушение прохождения пищи и постоянные срыгивания при ахалазии кардии приводят к похуданию, потере трудоспособности, снижению социальной активности. На фоне характерной симптоматики у пациентов развиваются неврозоподобные и аффективные состояния. Нередко больные длительно и безуспешно лечатся у невролога по поводу данных расстройств. Между тем, неврогенные нарушения практически всегда регрессируют после излечения ахалазии кардии.
Диагностика
Кроме типичных жалоб и данных физикального обследования в диагностике ахалазии кардии чрезвычайно важны результаты инструментальных исследований. Обследование пациента при подозрении на ахалазию кардии начинают с обзорной рентгенографии грудной клетки. При выявлении на рентгенограмме тени расширенного пищевода с уровнем жидкости показано проведение рентгенографии пищевода с предварительным приемом бариевой взвеси. Рентгенологическая картина при ахалазии кардии характеризуется сужением конечного отдела пищевода и расширением вышележащего участка, S-образной формой органа.
Ценным диагностическим критерием ахалазии кардии служат результаты фармакологических проб с карбахолином или ацетилхолином: при их введении возникают непропульсивные беспорядочные сокращения мускулатуры в грудном отделе пищевода и усиление тонуса нижнего пищеводного сфинктера, что указывает на денервационную гиперчувствительность органа. Дифференциальный диагноз при ахалазии кардии проводят с доброкачественными опухолями пищевода, эзофагеальными дивертикулами, кардиоэзофагеальным раком, стриктурами пищевода.
Лечение ахалазии кардии
Лечение предусматривает устранение кардиоспазма и может проводиться с помощью консервативных или хирургических методов, иногда – лекарственной терапии. Консервативным методом устранения ахалазии кардии является пневмокардиодилатация – баллонное расширение кардиального сфинктера, которое проводится поэтапно, баллонами разного диаметра с последовательным увеличением давления. С помощью кардиодилатации достигается перерастяжение пищеводного сфинктера и снижение его тонуса. Осложнениями баллонной дилатации могут стать трещины и разрывы пищевода, развитие рефлюкс-эзофагита и рубцовых стриктур кардиального сфинктера.
Если ахалазия кардии сочетается с язвенной болезнью двенадцатиперстной кишки, дополнительно показана селективная проксимальная ваготомия. При наличии тяжелого пептического эрозивно-язвенного рефлюкс-эзофагита и выраженной атонии пищевода производится проксимальная резекция желудка и абдоминальной части пищевода с наложением инвагинационного эзофагогастроанастомоза и пилоропластика.
Лекарственная терапия при ахалазии кардии играет вспомогательную роль и направлена на продление ремиссии. С этой целью целесообразно назначение антидофаминергических препаратов (метоклопрамида), спазмолитиков, малых транквилизаторов, антагонистов кальция, нитратов. В последние годы для лечения ахалазии кардии используется ведение ботулотоксина. Важными моментами при ахалазии кардии служит соблюдение щадящей диеты и режима питания, нормализация эмоционального фона, исключение перенапряжения.
Прогноз и профилактика
Течение ахалазии кардии медленно прогрессирующее. Несвоевременное лечение патологии чревато кровотечением, прободением стенки пищевода, развитием медиастинита, общим истощением. Ахалазия кардии повышает риск развития рака пищевода. После проведения пневмокардиодилатации не исключен рецидив через 6-12 месяцев. Наилучшие прогностические результаты связаны с отсутствием необратимых изменений моторики пищевода и ранним проведением оперативного лечения. Пациентам с ахалазией кардии показано диспансерное наблюдение врача-гастроэнтеролога с выполнением необходимых диагностических процедур.
Ахалазия кардии
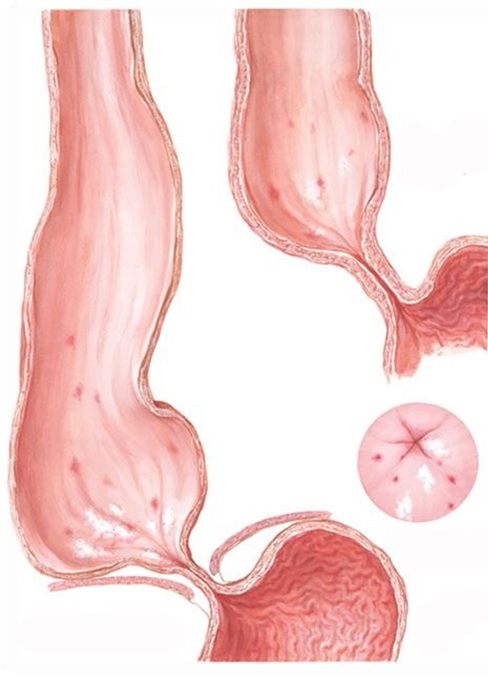
Ахалазия поражает одинаково часто как мужчин, так и женщин, чаще всего в возрасте 30 — 45 лет. Встречается это заболевание в 3 — 20% всех заболеваний пищевода. Раньше считалось, что ахалазия встречается у 1 человека на 100000 населения, но с улучшением диагностики и накоплением данных, стали появляться сообщения, что она встречается с частотой 5 и некоторые авторы считают, что даже 10 человек на 100000 населения
Причина возникновения ахалазии кардии
Сразу необходимо сказать, что достоверно причина ахалазии кардии не известна. Существую различные теории возникновения этого заболевания.
Генетическая теория основывается на том, что у пациентов с ахалазией пищевода находят изменения в одних и тех же локусах генов, кроме того риск заболевания ахалазией у детей с синдромом Дауна выше в 200 раз, чем в популяции
Инфекционная гипотеза — основывается на том, что при инфицировании Trypanosoma cruzi, которая вызывает болезнь Чагаса, также наблюдается дисфагия, по своему механизму похожая на ахалазию кардии. Кроме того рассматривается возможность развития ахалазии на фоне инфицирования вирусом Herpes zoster и вирусом кори
Аутоимунная теоррия — основывается на том, что у пациентом с ахалазией пищевода часто встречаются аутоимунные заболевания. Так у пациентов с ахалазией кардии, риск развития таких заболеваний как увеличивается: сахарного диабета 1-го типа в 5,4 раза, гипотиреоза в 8,5 раза, синдрома Шегрена в 37 раз, системной красной волчанки в 43 раза, увеита в 259 раз.
Но не одна из этих теорий, на сегодняшний день не получила убедительных подтверждений, поэтому нельзя говорит о том что известна причина этого заболевания
Классификация ахалазии кардии
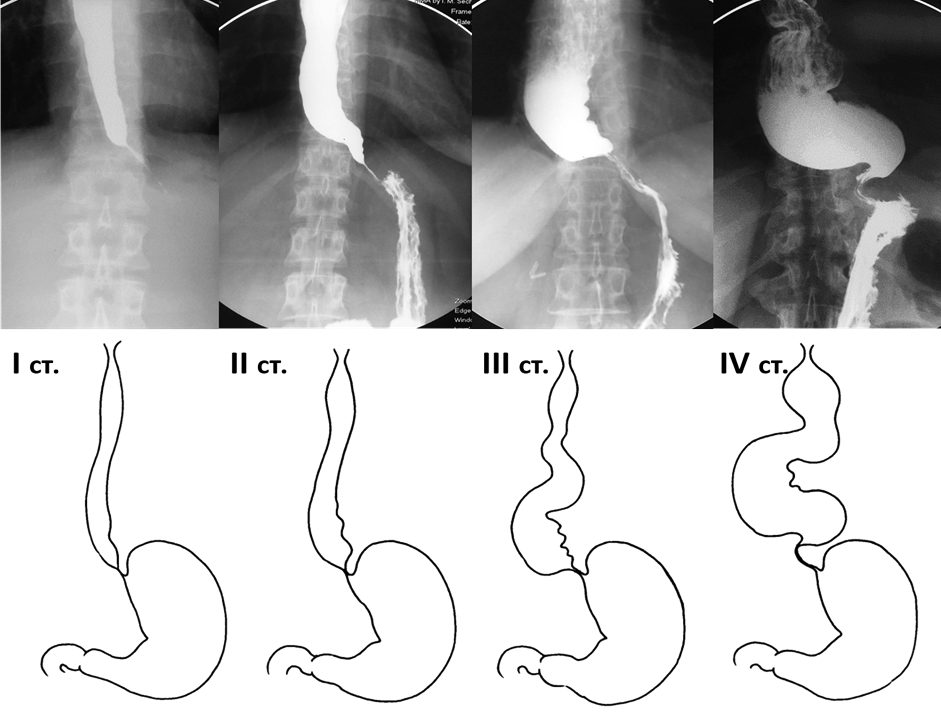
Классификация ахалазии кардии важна, так как в зависимости от степени заболевания, принимается решение о выборе той или иной тактики лечения. Всего различают 4 стадии:
I стадия (ранняя) — преходящие нарушения прохождения пищи, диаметр и перистальтика пищевода вне приступа не изменены ;
II стадия — устойчивое нарушение прохождения пищи, перистальтика пищевода усилена, пищевод не значительно расширен;
III стадия – выявляется стриктура кардиального отдела пищевода, последний значительно расширен, перистальтика вялая, поверхностная. В пищеводе натощак имеется жидкость;
IV стадия – стадия осложнений с изъязвлениями и эрозиями пищевода. Последний расширен до 10 см, S образно изогнут, перистальтика либо отсутствует полностью, либо разнонаправленная, поверхностная.
Клиническая картина ахалазии кардии
Чаще всего опытному гастроэнтерологу или хирургу не составит труда заподозрить ахалазию пищевода по жалобам пациента. Чаще всего пациенты жалуются на дисфагию, затруднение или полная невозможность прохождения пищи по пищеводу. Часто возникает так называемая парадоксальная дисфагия. когда твердая пища проходит легче чем жидкая. Со временем дисфагия прогрессирует и в особо тяжелых случаях пациенты теряют возможность питаться через рот, что приводит их к истощению. Частым симптомом ахалазии кардии является так называемый симптом мокрой подушки, когда у пациента появляется заброс содержимого расширенного пищевода в рот, и если человек спит то содержимое вытекает на подушку, это может быть как мокрота так и остатки пищи. Часто боли усиливаются на фоне стрессовых ситуаций, либо когда пациент нервничает, что нередко приводит пациентов с ахалазией кардии на прием к психиатру, вместо хирурга.
Нередко данное заболевание сопровождается достаточно интенсивными болями. В начале заболевания боли спастического характера, приступообразные, по мере прогрессирования заболевания боли становятся менее интенсивными, но практически постоянными.
Еще одним частым симптомом ахалазии кардии является регургитация, это заброс содержимого расширенного пищевода в рот, так называемая пищеводная рвота. Это состояние на самом деле напоминает рвоту, но в отличии от нее пациент не испытывает тошноты, и возникает она чаще всего при наклонах или в положении лежа.
Нередким симптомом ахалазии пищевода также является кашель, и развитие бронхитов, а иногда и воспаления легких. Проблема в том что во время регургитации агрессивное и инфицированное содержимое попадает в дыхательные пути, что и вызывает вышеуказанные осложнения.
Диагностика ахалазии кардии
Диагностика ахалазии кардии чаще всего не составляет большого труда.
ФГДС (гастроскопия) — необходимо начинать обследование именно с этой процедуры. При выполнении ФГДС выявляется сужение пищевода в месте его впадения в желудок, эндоскопически аппарат проходит в желудок с усилием. При ахалазии 3 и 4 степени, пищевод расширен, содержит натощак остатки пищи, нередко выявляются язвы и эрозии пищевода.
Рентгенография пищевода с барием — позволяет оценить скорость прохождения контраста по пищеводу у пациентов с ахалазией пищевода. Также оценивается поперечный размер пищевода, перистальтика, и наличие изгибов. Именно на основании рентгенографии выставляется степень ахалазии кардии.
КТ исследование — выполняется для оценки наличия или отсутствия воспаления в окружающих тканях, наличие бронхита или пневмонии
Моторика пищевода — считается “золотым стандартом” диагностики ахалазии кардии, однако оборудование для его выполнения крайне дорогостоящее, и при этом его применение достаточно ограничено. В связи с этим такое оборудование имеет несколько клиник, в основном научно исследовательских.
Лечение ахалазии кардии
Сразу необходимо сказать, лечение ахалазии кардии возможно только хирургическим путем, медикаментозное лечение и использование народных средств не приносит значимого облегчения состояния пациентов и носит вспомогательный характер. В лечение ахалазии пищевода используют следующие методы: баллонная дилатация пищевода, инъекции ботулотоксина, лапароскопическая внеслизистая кардиомиотомия, пероральная эндоскопическая миотомия
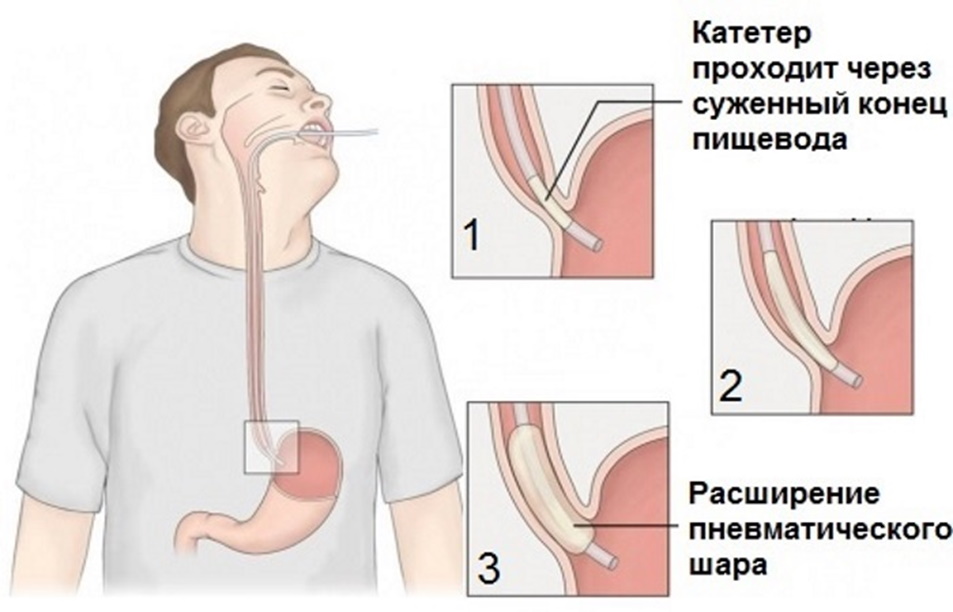
Баллонная дилатация пищевода — наиболее часто используемый метод лечения ахалазии, в
связи с достаточной простотой. Суть метода заключается в том. что под контролем эндоскопа в желудочно пищеводный переход устанавливается силиконовый баллон на зонде, после чего он раздувается воздухом, и тем самым фактически разрывая неработающий сфинктер. Недостатком метода служит, нестойкий эффект, обычно длящиеся 1 — 2 года, и сокращающийся по мере повторения процедуры. Также при баллонной дилатации присутствует риск разрыва пищевода, хоть и достаточно не высокий.
Инъекция ботулотоксина — применяется чаще всего у пациентов с тяжелыми сопутствующими заболеваниями, кому противопоказано хирургическое вмешательство. Применяется крайне редко из-за неустойчивого эффекта. который длится не более 6 месяцев.
Операция при ахалазии кардии — лапароскопическая внеслизистая кардиомиотомия выполняется без разреза, через 1 см проколы. Выделяется часть пищевода, впадающая в желудок, и рассекается кардиальный сфинктер. Для предотвращения рецидива, края разреза мышечного слоя пищевода подшиваются к стенкам желудка, а для предотвращения рефлюкса желудочного содержимого в пищевод, формируется фундопликационная манжета. Этот метод показал свою эффективность в 90% случаев. при низком проценте осложнений, и на сегодняшний день является ведущим методом лечения ахалазии пищевода.
Пероральная эндоскопическая миотомия (ПОЭМ) — достаточно новый метод эндоскопического лечения ахалазии пищевода. Был внедрен в 2007 году хирургами из Японии, в 2010 стал выполняться в некоторых клиниках России. Суть метода та же что и при оперативном лечение, то есть рассечение кардиального сфинктера, только в данном случае, эта манипуляция выполняется из просвета пищевода. В настоящее время идет накопление опыта и результатов такого метода лечения ахалазии. Первые полученные данные говорят о сопоставимой эффективности с оперативным лечением, однако выявился и не достаток. У 40 — 60% перенесших ПОЭМ появляется другое заболевание, рефлюкс-эзофагит, что требует постоянного приема антисекреторных препаратов. Дело в том, что рассекая сфинктер мы добиваемся свободного прохождения пищи, однако сфинктер после рассечения перестает закрываться вообще. В связи с этим желудочное кислое содержимое попадает в пищевод, и вызывает его воспаление. При лапароскопической операции формируется фундопликационная манжета, предотвращающая заброс желудочного содержимого в пищевод.
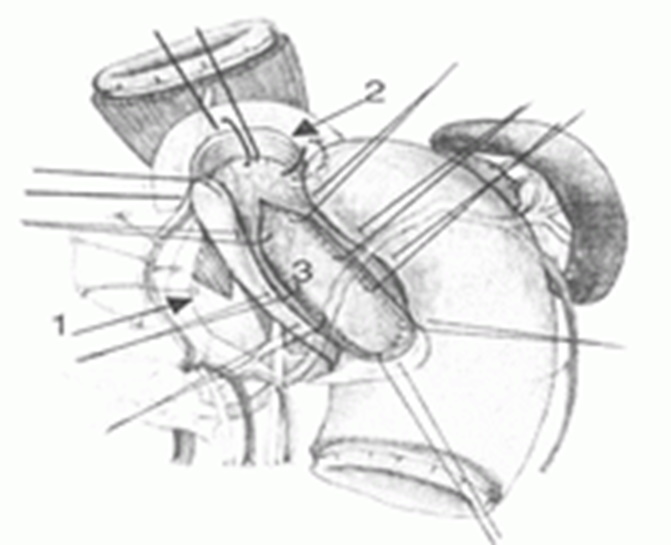
Перечисленные метода лечения ахалазии кардии дают хороший эффект при ахалазии 1 и 2 степени, удовлетворительный результат при ахалазии 3, при 4 степени приходится удалять пищевод, и замещать его желудочным трансплантатом.
В целом при своевременном обращении к врачу, возможно достигнуть высокого качества жизни пациентов, и предупредить осложнения ахалазии пищевода.
Ахалазия кардии и кардиоспазм
Общая информация
Краткое описание
Этиология и патогенез
Несмотря на многовековую историю изучения ахалазии кардии, ее этиология до сих пор неизвестна. В настоящее время рассматриваются три основные гипотезы: генетическая, аутоиммунная и инфекционная.
Кроме NO, нейротрансмиттером тормозящих нейронов является ВИП. Один из его рецепторов — рецептор 1, который принадлежит к семейству секретиновых и экспрессируется различными иммунными клетками, такими как Т-лимфоциты, макрофаги и дендритные клетки. Полиморфизм этого гена (VIPR1) также может играть роль в развитии идиопатической ахалазии. VIPR1 локализуется в хромосоме 3p22. В некоторых исследованиях были установлены пять его простых нуклеотидных полиморфизмов: (rs421558) Intron‑1, (rs437876) Intron‑4, (rs417387) Intron‑6, rs896 и rs9677 (3’UTR).
Рассматривая аутоиммунную природу заболевания, необходимо напомнить о циркулирующих аутоантителах. У пациентов с ахалазией кардии чаще всего обнаруживают следующие нейрональные аутоантитела: антитела к никотиновым рецепторам ацетилхолина — ганглионарного и мышечного типа, к кальциевым каналам — P/Q- и N-типа, к декарбоксилазе глутаминовой кислоты, к скелетным мышцам и антинейрональные нуклеарные антитела, известные также под названием anti-Hu. Так, в одном из последних крупных исследований, проведенном в клинике Mayo, установлено, что у 26% больных с идиопатической ахалазией кардии выявляют антитела к скелетным мышцам, а у 21% — к декарбоксилазе глутаминовой кислоты.
Эпидемиология
Клиническая картина
Cимптомы, течение
Основные симптомы заболевания — прогрессирующая дисфагия, регургитация и загрудинные боли, связанные с неполным опорожнением пищевода и хроническим эзофагитом [21, 22, 30, 34, 35, 45, 71 и др.].
Пациент может самостоятельно уменьшить выраженность дисфагии, используя различные приемы: запивание пищи большим количеством жидкости, заглатывание воздуха, повторные глотательные движения, ходьба. Немаловажное значение имеет и температура принимаемой пищи: большинство больных отмечают, что лучше проходит теплая и горячая пища.
Ярким симптомом заболевания является активная и пассивная регургитация, которая отмечается у 84 и 68% больных соответственно. Активная регургитация представляет собой срыгивание только что съеденной пищи или слизи и более характерна для начальных стадий болезни. Она возникает при незначительной дилатации пищевода, тогда как значительное расширение пищевода может привести к отсроченной регургитации, объем которой значительно больше. Пассивная регургитация возникает вне приема пищи, обычно в горизонтальном положении пациента или при наклоне туловища вперед, чаще наблюдается при ахалазии кардии. Регургитация, особенно пассивная, может сопровождаться аспирацией пищи в дыхательные пути, которая может привести к нарушению функции органов дыхания, сопровождающемуся одышкой и кашлем, и маскировать основное заболевание. Необходимо отметить, что ночной кашель наряду с симптомом «мокрой подушки» свидетельствуют о декомпенсации заболевания и служат абсолютным показанием к проведению пневмокардиодилатации.
Еще одна характерная жалоба больных — боли в груди, которые наблюдаются примерно у 59% из них, чаще в молодом возрасте. При повышении давления в НПС и грудном отделе пищевода возникает интенсивная спастическая загрудинная боль, тогда как при атонии грудного отдела пищевода отмечаются умеренно выраженные боли за грудиной распирающего характера. Боли могут возникать во время приема пищи вследствие перерастяжения стенок пищевода и проходить после срыгивания или «проваливания» пищи в желудок. Они также могут быть вызваны спазмом гладкой мускулатуры пищевода и возникать как во время приема пищи, так и без четкой связи с ним. Для 1/3 больных с ахалазией кардии характерна жгучая боль по ходу пищевода, возникающая вследствие прямого раздражающего действия на пищевод остатков задержавшихся в нем пищи и лактата, продукция которого повышена при избыточной бактериальной ферментации сохраняющихся в пищеводе углеводов.
Диагностика
Для подтверждения диагноза идиопатической ахалазии необходимо использовать инструментальные методы обследования, такие как рентгенография пищевода с контрастированием, ЭГДС и манометрия, которая признана «золотым стандартом» диагностики. Некоторые авторы рекомендуют перед проведением рентгеноконтрастного исследования выполнить обзорную рентгенографию грудной клетки, по результатам которой можно определить наличие уровня жидкости в средостении, обусловленного застоем пищевых масс в пищеводе, а также выявить расширение средостения и отсутствие газового пузыря желудка. Рентгеноконтрастное исследование выполняют с бариевой взвесью, при этом оценивают степень расширения пищевода, его деформацию (S-образный пищевод), длительность задержки контрастной массы в пищеводе, рельеф абдоминального отдела пищевода и области пищеводно-желудочного перехода в момент открытия кардиоэзофагеального сфинктера, наличие или отсутствие газового пузыря желудка и некоторые другие параметры (рис. 1).
При II стадии определяется умеренное (до 3–4 см) расширение просвета пищевода; остатков пищи в пищеводе, как правило, нет, может быть небольшое количество прозрачной жидкости или слизи; слизистая оболочка гладкая, ровная, блестящая, ее складки расположены продольно; перистальтика усилена; кардия расположена по центру, обычно плотно сомкнута, но достаточно легко раскрывается при избыточной (по сравнению с обычным эндоскопическим исследованием) инсуффляции воздуха (рис. 2). При ретроградном осмотре складки в области пищеводно-желудочного перехода плотно обхватывают эндоскоп, слизистая оболочка мягкая, эластичная.
Как правило, каждой клинико-рентгенологической стадии кардиоспазма и ахалазии кардии соответствует определенная эндоскопическая картина, на основании которой стадия болезни может быть установлена и без предшествующего рентгенологического исследования, если оно не может быть выполнено по каким-либо причинам (рис. 3–5).
Рис. 3. Кардиоспазм II стадии.
а — рентгенограмма; б — эндофото (данные ФГБНУ «РНЦХ им. акад. Б.В. Петровского»).
Рис. 4. Кардиоспазм III стадии.
а — рентгенограмма; б — эндофото (данные ФГБНУ «РНЦХ им. акад. Б.В. Петровского»)
«Золотым стандартом» обследования пациентов при подозрении на ахалазию кардии является манометрия. В настоящее время для исследования двигательной функции пищевода можно использовать как метод открытых катетеров (водно-перфузионная манометрия), так и современные высокотехнологичные методы — манометрию высокой разрешающей способности (high resolution manometry — HRM) и объемную 3D-манометрию, которые имеют явные преимущества по сравнению с манометрией, выполняемой с помощью 4- или 8-канального водно-перфузионного катетера. При расположении датчиков давления на расстоянии 5 см друг от друга большие участки перистальтической волны грудного отдела пищевода «выпадают» из анализа. Так, подтягивание НПС и укорочение грудного отдела пищевода у больных с ахалазией кардии часто принимают за истинное, хотя и недостаточное, расслабление сфинктера («псевдорелаксация»). Использование многоканальных катетеров при манометрии высокой разрешающей способности позволяет избежать подобных ошибок (рис. 6).
При анализе результатов обследования пациентов с ахалазией кардии, проведенного с использованием манометрии высокого разрешения, следует учитывать Чикагскую классификацию нарушений моторики пищевода, созданную в 2008 г. Применение этого метода исследования позволило выделить три типа ахалазии кардии в зависимости от выявленных изменений двигательной активности грудного отдела пищевода, что дает возможность более точно прогнозировать эффективность лечения с помощью пневмокардиодилатации (рис. 7).
Дифференциальный диагноз
– кардиоэзофагеальным раком, для которого характерна прогрессирующая дисфагия, как и для истинной ахалазии. Однако быстрое уменьшение массы тела, короткий анамнез, часто пожилой возраст пациентов к моменту появления дисфагии свидетельствуют о злокачественном поражении. При физикальном осмотре можно выявить пальпируемое образование в брюшной полости и лимфаденопатию. При рентгенологическом исследовании с бариевой взвесью просвет пищевода может быть умеренно дилатирован, но степень расширения не коррелирует с выраженностью дисфагии. В дистальном отделе имеется сужение, но в отличие от такового при ахалазии оно не имеет характерного вида птичьего клюва или мышиного хвостика с постепенным симметричным сужением просвета и гладкими стенками, а чаще эксцентрично, с обрывом по типу ступеньки и неровными бугристыми контурами. Для установления точного диагноза необходимо проведение эзофагогастродуоденоскопии (ЭГДС). При малейшем подозрении на наличие злокачественного процесса в области кардии обязательным является получение материала для гистологического и цитологического исследований, поскольку рак развивается у 3–8% больных с ахалазией [30]. Необходимо помнить о возможности развития рака не только в области пищеводно-желудочного перехода, но и в стенке воспаленного расширенного пищевода;
– пептической стриктурой, являющейся осложнением длительно текущей гастроэзофагеальной рефлюксной болезни (ГЭРБ). Для нее также характерна дисфагия: в начальных стадиях отмечается затрудненное прохождение по пищеводу только твердой пищи, тогда как в более поздних стадиях присоединяется нарушение пассажа кашицеобразной пищи и жидкостей. Дисфагии, как правило, предшествует длительно существующая изжога, часто возникающая в ночное время, однако к моменту формирования стриктуры изжога прекращается. Для дифференциальной диагностики важно проведение манометрии и рентгенографии пищевода с контрастированием, результаты которого свидетельствуют об отсутствии значимого расширения просвета пищевода, а в вертикальном положении больного контрастное вещество (взвесь сульфата бария) в отличие от ахалазии кардии длительно в пищеводе не задерживается. При ЭГДС могут быть выявлены эрозии;
– ишемической болезни сердца (ИБС), основное клиническое проявление которой — боли в груди. Этот симптом практически невозможно отличить от такового при ахалазии кардии, особенно если ИБС провоцируется приемом пищи. Не помогает в плане дифференциальной диагностики и эффект от приема нитроглицерина, так как боли при ахалазии, как и при ИБС, купируются после его приема. ЭКГ также не всегда позволяет уточнить диагноз, так как ишемия миокарда очень часто имеет скрытый характер и выявляется лишь при физической нагрузке. В связи с этим в спорных ситуациях необходимо проводить комплексное кардиологическое обследование, включающее велоэргометрию или тредмил-тест, эхокардиографию и комбинированное исследование — суточное холтеровское мониторирование и 24-часовую pH-метрию;
Лечение
Существующие методы лечения кардиоспазма и ахалазии кардии (консервативные, эндоскопические, хирургические) направлены на расширение кардии тем или иным способом либо снижение ее тонуса, для того чтобы улучшить прохождение пищи через область пищеводно-желудочного перехода.
Пациентам с ахалазией кардии необходимо назначить диету по типу пищеводного стола с исключением острых и кислых продуктов; пища должна быть теплой, принимать ее нужно медленно, тщательно пережевывая. Оптимальным считается 4- или 5-разовое питание небольшими по объему порциями. Следует также отметить, что существует индивидуальный набор продуктов, усиливающих дисфагию у конкретных пациентов, которые целесообразно исключить из рациона. После приема пищи не следует принимать горизонтальное положение во избежание ее регургитации. Во время сна пациент не должен находиться в строго горизонтальном положении, так как пища может задерживаться в пищеводе до нескольких часов, а верхний пищеводный сфинктер расслабляется во время сна, что приводит к пассивной регургитации и возможной аспирации дыхательных путей.
Для консервативного лечения пациентов с ахалазией кардии используют две группы препаратов: блокаторы кальциевых каналов и нитраты. Чаще всего применяют нифедипин и изосорбида мононитрат в дозе 5–10 мг, которые следует принимать за 20—30 мин до приема пищи. Эти лекарственные средства снижают давление НПС в среднем на 47–63%, однако полностью купировать симптомы ахалазии удается редко. Необходимо также помнить о возможных побочных эффектах этих препаратов, из которых наиболее часто возникают головная боль, артериальная гипотензия, головокружение. В связи с этим лекарственную терапию применяют в случае невозможности использовать альтернативные методы при лечении пациентов, ожидающих выполнения пневмокардиодилатации или хирургического лечения, и как сопутствующую терапию у больных с ахалазией кардии, сопровождающейся рефрактерной болью в груди.
Процедура основана на расширении суженного участка пищеводно-желудочного перехода с помощью кардиодилататора, в результате чего снижается давление НПС и улучшается пассаж пищи по пищеводу. Для этого используют пневмодилататоры, смонтированные на желудочном зонде, которые имеют форму гантели для лучшей фиксации в зоне пищеводно-желудочного перехода (ЗАО «МедСил», Россия). Дилатацию выполняют под рентгенологическим контролем, однако в случаях выраженного расширения, удлинения и деформации пищевода, проявляющейся в значительном отклонении его от продольной оси (С- или S-образный пищевод), проведение пневмодилататора под рентгенологическим контролем затруднено или невозможно. Использование эндоскопической техники позволяет выполнить дилатацию под контролем зрения при заболевании в любой стадии, а также оценить состояние слизистой оболочки в зоне пищеводно-желудочного перехода непосредственно после окончания вмешательства и немедленно диагностировать возникшие осложнения. Эндоскопические вмешательства являются методом выбора при поздних стадиях кардиоспазма и ахалазии кардии у пациентов, у которых высок операционно-анестезиологический риск.
Лечебную процедуру выполняют с помощью кардиодилататора, который надевают на дистальную часть эндоскопа. Диаметр баллона для дилатации кардии в широкой части составляет 30 и 40 мм, в области «талии» — 25 и 30 мм, длина — 12–15 см. Баллон укреплен на полой трубке, внутренний диаметр которой соответствует наружному диаметру эндоскопа и составляет 9–10 мм, длина — 17–20 см. К проксимальному концу баллона присоединена трубка диаметром около 3 мм для инсуффляции воздуха или введения воды в баллон. «Талия» в средней части баллона облегчает его фиксацию в кардии.
Давление при кардиодилатации повышают постепенно — от 120–160 мм рт. ст. в начале лечения до 300–320 мм рт. ст. в конце курса. Экспозиция составляет 1–2 мин, для достижения эффекта требуется в среднем 4–5 сеансов. Уровень давления контролируют с помощью манометра.
Для проведения дилатации кардии применяют также дилататоры «Rigiflex» («Boston Scientific», MA, США), представляющие собой полиэтиленовые баллоны трех диаметров — 30, 35 и 40 мм. Аналогичные баллоны диаметром 30 и 35 мм производит фирма «Cook Medical» (США).
ПД можно проводить как под рентгенологическим контролем, так и с помощью эндоскопической техники по введенной в желудок через канал эндоскопа направляющей струне. Процедура заключается в установке баллона точно в месте перехода пищевода в желудок. При извитом пищеводе для правильного позиционирования баллона в кардии необходим визуальный контроль, для чего параллельно баллону вводят эндоскоп. Для предупреждения осложнений (перфорация, кровотечение) очень важно избегать форсированной дилатации и повышать давление в баллоне постепенно в течение нескольких сеансов от 160 до 300 мм рт. ст. в течение 40–60 с. Баллон может быть заполнен не только воздухом, но и жидкостью — водой или водорастворимым контрастным веществом для лучшей визуализации. Такая процедура называется гидродилатацией кардии, ее выполняют, как правило, при давлении 0,5–2 атм в течение 2 мин. Уровень давления контролируют с помощью манометра.
Эффективность терапии достаточно высокая, зависит от диаметра кардиодилататора и через 3 года составляет в среднем 74, 86 и 90% при использовании баллонов диаметром 30, 35 и 40 мм соответственно.
После дилатации и для мониторирования состояния после лечения, которое необходимо проводить 1 раз в год, жалобы пациентов могут быть оценены по шкале Eckardt.
Шкала Eckardt
| Симптомы | Баллы* | |||
| 0 | 1 | 2 | 3 | |
| Дисфагия | Никогда | Периодически | 1 раз в день | Каждый прием пищи |
| Регургитация | Никогда | Периодически | 1 раз в день | Каждый прием пищи |
| Боли в груди | Никогда | Периодически | 1 раз в день | Каждый прием пищи |
| Уменьшение массы тела, кг | Нет | 5–10 | >10 | |
* 0–3 балла — ремиссия, более 4 баллов — неэффективность ПД.
Кроме улучшения клинического течения заболевания, предиктором длительной ремиссии после ПД является давление НПС
На эффективность ПД оказывают положительное влияние ряд факторов, такие как возраст пациентов более 40 лет, II тип ахалазии кардии по данным HRM, начальная стадия заболевания, давление НПС 15 мм рт. ст. после ранее выполненной ПД, эвакуация из пищевода менее 50% бариевой взвеси через 1 мин от начала рентгеноскопии пищевода, однократно проведенная ПД с использованием баллона диаметром 30 мм.
Необходимо помнить, что самым тяжелым осложнением ПД, которое наблюдается в 1,5–3% случаев, является перфорация стенки пищевода. Однако использование современных дилататоров и опыт специалистов, выполняющих ПД, позволяют значительно снизить риск ее возникновения. После ПД могут отмечаться также боли в груди, повреждение слизистой оболочки пищевода и гематома, повышение температуры тела и аспирационная пневмония, однако риск их развития очень мал. Достаточно редко после процедуры развивается ГЭРБ.
Еще в 1994 г. в зарубежной литературе появились сообщения об использовании ботулинового токсина А для эндоскопического лечения кардиоспазма и ахалазии кардии [42, 43, 49, 60, 79 и др.]. Ботулиновый токсин оказывает расслабляющее действие на гладкую мускулатуру путем блокирования выброса медиатора парасимпатической нервной системы ацетилхолина холинергическими нейронами и нарушения нервно-мышечной передачи. При этом процесс синтеза и депонирования ацетилхолина в пресинаптической терминали синапса не нарушается [20, 55]. Введение ботулинового токсина А в зону кардии приводит к снижению базального и остаточного давления НПС.
Процедура основана на интрамуральном эндоскопическом введении ботулинового токсина А в НПС в дозе 80–100 ЕД, при этом 1 мл препарата (20–25 ЕД) вводят с помощью иглы диаметром 5 мм для склеротерапии в каждый из четырех квадрантов НПС под визуальным контролем.
Эффективность терапии составляет около 80% в течение 1-го месяца наблюдения, 70% после 3 мес, 50% через 6 мес и около 40% через 1 год, в связи с чем иногда требуется повторная инъекция ботулинового токсина.
Несмотря на безопасность и простоту выполнения, этот метод можно рассматривать в качестве альтернативного варианта только при лечении пациентов, имеющих абсолютные противопоказания к пневмокардиодилатации, эндоскопическому и оперативному вмешательству, особенно если речь идет о лицах старшей возрастной группы, наличии тяжелой сопутствующей патологии сердечно-сосудистой и бронхолегочной систем, а также при наличии S-образного пищевода [9].
К факторам, оказывающим негативное влияние на эффективность этого метода, относят: молодой возраст пациентов, мужской пол, высокое давление покоя НПС, отсутствие эффекта от предыдущих инъекций ботулинового токсина, а наиболее выраженный эффект от лечения можно ожидать у людей пожилого возраста и пациентов с ахалазией и выраженной гипермоторной дискинезией грудного отдела пищевода. Следует также отметить, что до настоящего времени в Российской Федерации препарат «Диспорт» не зарегистрирован в качестве средства для применения в гастроэнтерологии, его разрешено использовать лишь в неврологии и косметологии. Для лечения ахалазии кардии препарат применяют в Республике Татарстан по специальному разрешению Министерства здравоохранения этого субъекта РФ.
При неэффективности нехирургических методов лечения решают вопрос о необходимости выполнения оперативного вмешательства. Следует отметить, что выполняемая в ряде лечебных учреждений эзофагокардиомиотомия по Геллеру, заключающаяся в рассечении мышечной оболочки нижнего конца расширенного сегмента пищевода и кардиальной части желудка по передней и задней стенкам, у 15% больных осложняется развитием ГЭРБ. В связи с этим основным оперативным вмешательством является эзофагокардиомиотомия с неполной фундопликацией для предупреждения рефлюкса. Согласно отдаленным результатам, по эффективности она превосходит ПД, однако из-за травматичности любого оперативного вмешательства, необходимости анестезиологического пособия и вероятности развития послеоперационных осложнений этот метод лечения применяют при неэффективности повторных ПД.
В настоящее время для лечения кардиоспазма широко применяют лапаро- и торакоскопические операции, из которых предпочтение отдают лапароскопической миотомии с частичной фундопликацией в различных модификациях, обеспечивающей беспрепятственное прохождение пищи у пациентов с ослабленной моторикой пищевода, с одной стороны, и предупреждающей рефлюкс — с другой [1, 71, 92, 101 и др.]. Эффективность минимально инвазивных вмешательств не уступает таковой открытых хирургических операций — 94 и 84% соответственно, а частота послеоперационных осложнений ниже. К сожалению, после хирургического лечения также в ряде случаев возникает рецидив дисфагии, в связи с чем требуется повторное проведение консервативного, в том числе с использованием эндоскопических методов, или хирургического лечения.
В терминальной стадии заболевания выполняют экстирпацию или субтотальную резекцию пищевода с одномоментной пластикой желудочной трубкой, в том числе с применением лапарои торакоскопической техники. Показания к выбору метода оперативного вмешательства определяют индивидуально [1, 36 и др.].
В 2007 г. был предложен и апробирован на живых свиньях новый метод лечения ахалазии, заключающийся в обеспечении прямого доступа к мышечному слою пищевода через туннель, созданный в подслизистом слое (один из вариантов NOTES — внутрипросветной эндоскопической хирургии через естественные отверстия) [80]. У человека эта операция, получившая название «пероральная эндоскопическая миотомия» (POEM), впервые выполнена в 2008 г. [62]. С этого времени операцию стали быстро внедрять в клиническую практику, и к настоящему времени она выполнена уже нескольким сотням пациентов [52, 63, 86, 87, 96, 109, 111 и др.].
Авторы рассматривают эту методику в качестве альтернативы баллонной кардиодилатации и эзофагокардиомиотомии по Геллеру. Суть ее состоит в следующем: с помощью специальных инструментов, введенных по инструментальному каналу гибкого эндоскопа, делают продольный надрез слизистой оболочки пищевода на протяжении 1,5–3 см примерно на 10–12 см выше пищеводно-желудочного перехода, через который в подслизистый слой вводят эндоскоп. Вместо воздуха инсуффлируют углекислый газ для предупреждения развития пневмомедиастинума и пневмоперитонеума. Под визуальным контролем на всем протяжении вплоть до малой кривизны желудка как минимум на 3 см ниже пищеводно-желудочного перехода создают туннель между слизистой оболочкой и мышечным слоем путем последовательного пересечения соединительнотканных волокон и сосудов после порционного введения изотонического раствора натрия хлорида с добавлением, как правило, раствора высокой вязкости, чаще всего на основе глицерола и гиалуроновой кислоты, подкрашенного индигокармином или метиленовым синим для лучшей визуализации. Рассечение волокон выполняют специальными ножами различной формы разных производителей («Olympus», «Fujifilm», «ERBE» и др.). Затем постепенно рассекают циркулярные мышечные волокна в направлении сверху вниз. Дефект в слизистой оболочке клипируют.
POEM — эффективная и достаточно безопасная процедура. Исследователи сообщают об уменьшении выраженности симптомов дисфагии с 10 баллов до 1,3 балла, снижении давления НПС с 52,4 (14,2–80,5) до 19,8 (9,3–42,7) мм рт. ст. в течение в среднем 5 мес. При оценке жалоб пациентов по шкале Eckardt отмечается значительное улучшение состояния: если до операции средняя оценка составляла 7–8 баллов, то после нее у всех пациентов она была ниже 3 баллов, в основном 0–1 балл. Частота развития ГЭРБ варьирует, согласно данным разных авторов, от 0 до 37% [109].
Прогноз
Информация
Источники и литература
Информация
3 ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А. И. Евдокимова» Минздрава России, Москва, Российская Федерация