Аркоксиа или нимесулид в чем разница
Современная терапия остеоартроза
Какие основные группы препаратов используются в лечении остеоартроза? В чем преимущества селективных ингибиторов ЦОГ-2? Остеоартроз является мультифакториальным хроническим прогрессирующим заболеванием, которое характеризуется нарушением равновесия ме
Какие основные группы препаратов используются в лечении остеоартроза?
В чем преимущества селективных ингибиторов ЦОГ-2?
Остеоартроз является мультифакториальным хроническим прогрессирующим заболеванием, которое характеризуется нарушением равновесия между анаболическими и катаболическими процессами прежде всего в гиалиновом хряще. Помимо гиалинового хряща при остеоартрозе в патологический процесс вовлекается синовиальная оболочка с развитием в той или иной степени рецидивирующего синовита, а также субхондральная кость, суставная капсула, внутрисуставные связки и околосуставные мышцы.
Остеоартроз встречается в любом возрасте, но чаще всего после 45-50 лет. В возрасте старше 70 лет рентгенологические признаки остеоартроза находят у 90% женщин и у 80% мужчин, причем у 20% из них остеоартроз является клинически манифестным. Боль и ограничение подвижности суставов, обусловленные этим заболеванием, резко ухудшают качество жизни больных и представляют серьезную социально-экономическую проблему, являясь одной из основных причин потери трудоспособности.
Целью медикаментозной терапии остеоартроза является уменьшение и даже полное прекращение болей в суставах и восстановление их функций, а также профилактика дальнейшего прогрессирования данного заболевания путем коррекции нарушенного метаболизма в гиалиновом хряще. В схему медикаментозной терапии остеоартроза включены два основных класса препаратов:
Препараты второго класса тормозят темпы прогрессирования заболевания, то есть обладают хондропротективным действием. К таким медикаментам в первую очередь относятся структурные аналоги хрящевой ткани, а именно препарат дона (виартрил, артрил, праксис, биофлекс), активным ингредиентом которого является глюкозамин сульфат, а также препарат структум, представляющий собой хондроитин сульфат. Эти лекарственные средства модулируют важнейшие функции хондроцитов в поврежденном остеоартрозом хряще, стимулируют синтез сульфатированных и несульфатированных протеогликанов, сопоставимых с физиологическими протеогликанами, включая их способность формировать прочные комплексы с гиалуроновой кислотой.
Помимо структума и дона, к медикаментам второго класса относятся также румалон, представляющий собой вытяжку из хрящевой ткани и костного мозга телят; диацерин — ингибитор интерлейкина-1; негидролизирующиеся соединения сои и авокадо; препараты гиалуроновой кислоты.
Многие из медленно действующих препаратов обладают не только хондропротективным, но и прямым противовоспалительным действием.
Но все же наиболее яркий антивоспалительный эффект имеют нестероидные противовоспалительные препараты (НПВП), без которых не мыслится комплексная терапия остеоартроза [1, 2]. Их назначение оправдано тем обстоятельством, что, хотя остеоартроз является дегенеративным заболеванием, проявления вторичного синовита или воспалительный процесс в периартикулярных мягких тканях усугубляют его прогрессирование. Именно поэтому за рубежом принято понятие «остеоартрит». Препараты этой группы способны быстро снижать интенсивность боли в пораженных суставах, вплоть до полного ее купирования, подавлять экссудативные явления и восстанавливать объем движений, то есть активно воздействовать на основные субъективные и объективные симптомы остеоартроза. Многие пациенты с этим заболеванием принимают НПВП почти постоянно, так как это единственные средства, обладающие выраженным терапевтическим эффектом и позволяющие больным сохранить возможность обслуживать себя самостоятельно.
В настоящее время хорошо известны несколько групп НПВП, детально изучена фармакокинетика, четко определены показания к применению, режимы приема, спектр возможных побочных реакций.
Основными представителями НПВП являются производные арилкарбоновых кислот (аспирин, салицилат натрия, флуфенамовая и мефенамовая кислоты), арилалкановых кислот (диклофенак, ибупрофен, флурбипрофен, напроксен, толметин, индометацин, сулиндак), эноликоновой кислоты (фенилбутазон, пироксикам, мелоксикам). Основным механизмом действия НПВП является подавление биосинтеза простагландинов.
Как известно, простагландины характеризуются широкой палитрой биологического действия. Они являются медиаторами воспалительных реакций и способствуют развитию отека и экссудации, сенсибилизируют рецепторы к медиаторам боли (гистаминам и брадикинину), а также понижают порог болевой чувствительности, повышают чувствительность гипоталамических центров к действию пирогенов. Простагландины регулируют и большое количество физиологических процессов, включая моторику кишечника, агрегацию тромбоцитов, сосудистый тонус, функцию почек, секрецию желудочного сока, трофику слизистой оболочки желудка. Отсюда ясно, почему НПВП обладают не только терапевтическим противовоспалительным, анальгетическим и антипиретическим действием, но и многочисленными нежелательными побочными эффектами.
Наиболее часто встречаются побочные явления со стороны желудочно-кишечного тракта (ЖКТ), которые проявляются в виде желудочной или кишечной диспепсии, образования эрозий и язв в желудке и двенадцатиперстной кишке. Интересно, что в США количество летальных исходов от осложнений со стороны ЖКТ, связанных с приемом традиционных НПВП, превышает смертность от рака шейки матки, бронхиальной астмы или меланомы.
Толчком к разработке новых классов НПВП, обладающих меньшим спектром побочных явлений и хорошей переносимостью, явилось открытие в 1991 году двух изоформ циклооксигеназы (ЦОГ) — ЦОГ-1 и ЦОГ-2. Еще ранее Д. Вейн (J. Vane) обнаружил, что противовоспалительное действие НПВП связано с подавлением ЦОГ — ключевого фермента биосинтеза простагландинов. В 1995 году была выдвинута концепция, согласно которой ЦОГ-1 является конститутивным защитным ферментом, обладающим цитопротективным действием и закономерно присутствующим во многих тканях организма, в то время как ЦОГ-2 обладает провоспалительной активностью и накапливается в больших концентрациях только в очагах воспаления. В это же время стало ясно, что побочные явления НПВП связаны с ингибицией ЦОГ-1, а противовоспалительный их эффект — с ингибицией ЦОГ-2. Таким образом, эффективность и безопасность НПВП ассоциируются с избирательным (селективным) подавлением ЦОГ-2 (б).
Современная патогенетическая классификация НПВП строится на учете их воздействия на отдельные изофермы ЦОГ. Так, большинство НПВП, применяющихся до последнего времени (производные индола, диклофенак натрия, ибупрофен, пироксикам и т. д.), являются неселективными ингибиторами ЦОГ. Мелоксикам и нимесулид относятся к ЦОГ-2-селективным препаратам. Они обладают определенным противовоспалительным действием в дозах, ингибирующих ЦОГ-2 и тем не менее вызывают существенное ингибирование ЦОГ-1. К новому классу специфических ингибиторов ЦОГ-2 относятся целекоксиб (целебрекс) и рофекоксиб. Как видно из определения, специфические ингибиторы ЦОГ-2 действуют только на ЦОГ-2 и не влияют на ЦОГ-1.
Целебрекс был принят к использованию в клинической практике только в декабре 1998 года. Этот препарат является первым специфическим ингибитором ЦОГ-2, специально разработанным для уменьшения числа побочных реакций (по сравнению с другими НПВП). Фармакокинетические свойства целебрекса изучены на здоровых людях. При приеме внутрь максимальная его концентрация в плазме появляется через 3 часа. 90% дозы препарата метаболизируется в печени и выводится с желчью. Белковосвязывающая способность этого НПВП достигает 97%, а период полураспада — 10-12 часов. Продолжительность действия целебрекса составляет 11 часов. Препарат плохо растворяется в воде и поэтому применяется только внутрь. Антациды снижают биодоступность препарата, а прием пищи увеличивает ее на 10-20%. Фармакокинетика не зависит от возраста, что особенно важно, учитывая пожилой возраст больных остеоартрозом. При лечении остеоартроза суточная доза целебрекса обычно не превышает 200-400 мг, но чаще его назначают по 200 мг один раз в день или по 100 мг два раза в день. Препарат лучше принимать с едой, хотя в рекомендациях фирмы, производящей целебрекс, указано что его прием не зависит от употребления пищи [4].
Проведенные плацебо-контролированные и сравнительные (с другими НПВП) исследования показали высокую терапевтическую эффективность целебрекса у больных остеоартрозом коленных и тазобедренных суставов. Оказалось, что этот препарат в дозе 200 или 400 мг в сутки по своей противовоспалительной и анальгетической активности сопоставим с 1000 мг напроксена, 150 мг диклофенака или 2400 мг ибупрофена. Он положительно воздействовал на такие показатели патологического процесса, как выраженность боли в суставах, выраженность и продолжительность утренней скованности, общая активность болезни, оцениваемые врачом и пациентом, а также индекс WOMAC и функция пораженных суставов. При этом препарат достоверно изменял их значения [5]. У преобладающего большинства больных с вторичным синовитом наблюдалось разрешение экссудативных явлений в коленных суставах.
В противоположность стандартным НПВП, которые угнетают синтез протеогликанов артрозным хрящом и тем самым еще более способствуют прогрессирующей дегенерации хряща, целебрекс обладает хондронейтральным действием, а возможно, даже предотвращает лизис хондроцитов и принимает участие в репарации хряща после его повреждения. Из этого следует, что в случае необходимости его можно применять длительно (на протяжении нескольких недель и даже месяцев) без какого-либо отрицательного влияния на ткани пораженного сустава.
Целебрекс, обладающий такой же терапевтической эффективностью, как и другие НПВП, характеризуется более высокой переносимостью и безопасностью применения. При приеме препарата возможно развитие таких побочных явлений, как абдоминальная боль, диарея, тошнота, головная боль, головокружение, ринит, синусит. Однако частота этих реакций не является статистически значимой по сравнению с плацебо.
В случаях применения этого препарата в течение одной недели в высоких и сверхвысоких дозах не было выявлено, согласно данным эндоскопического контроля, желудочно-кишечной токсичности [3]. Частота образования язв желудка и двенадцатиперстной кишки при назначении 200 мг целебрекса, 1000 мг напроксена и 2400 мг ибупрофена непрерывно на протяжении трех месяцев составила 7,5, 36,4 и 23,3% соответственно.
Применение специфических ингибиторов ЦОГ-2 у больных остеоартрозом оправдано и тем обстоятельством, что они совместимы с другими лекарственными агентами. Это позволяет проводить адекватную и своевременную терапию сопутствующих заболеваний, которые закономерно встречаются у лиц пожилого возраста.
Разумный выбор НПВП при сочетанной патологии: заболеваниях суставов и гипертонической болезни
Нестероидные противовоспалительные препараты (НПВП) являются одной из основных групп лекарственных средств, применяемых при лечении ревматоидного артрита (РА). Противовоспалительный и анальгетический эффект данной группы препаратов связан с подавлением а
Нестероидные противовоспалительные препараты (НПВП) являются одной из основных групп лекарственных средств, применяемых при лечении ревматоидного артрита (РА). Противовоспалительный и анальгетический эффект данной группы препаратов связан с подавлением активности циклооксигеназы-2 (ЦОГ-2) в очаге воспаления — ключевого фермента синтеза простагландинов провоспалительной активности, а подавление изоформы ЦОГ-1 приводит к нарушению физиологических реакций: в частности, к нарушению синтеза простагландинов класса Е в слизистой оболочке желудка и развитию НПВП-гастропатии.
Большинство «стандартных» НПВП способно подавлять активность обеих изоформ ЦОГ, поэтому их применение часто ограничено из-за развития побочных эффектов, в первую очередь — со стороны желудочно-кишечного тракта (ЖКТ). Субъективные симптомы со стороны ЖКТ встречаются примерно у трети больных, а в 5% случаев представляют серьезную угрозу жизни пациентов. Именно поэтому в последние годы особо пристальное внимание привлекает проблема безопасного применения НПВП. Полагают, что препараты более селективные в отношении ЦОГ-2 реже вызывают развитие НПВП-гастропатии. Изучение механизмов действия НПВП послужило толчком к созданию новых препаратов, обладающих всеми положительными свойствами стандартных НПВП, но менее токсичных, — это специфические ингибиторы ЦОГ-2 [3, 4, 13].
В последние годы особую актуальность приобрела проблема взаимодействия НПВП и гипотензивных препаратов, а также связи между применением НПВП и развитием гипертонической болезни (ГБ). Неселективные НПВП могут привести к повышению АД (преимущественно диастолического) не только у больных артериальной гипертензией (АГ), но и у лиц с нормальным АД за счет ингибиции системного и локального, внутрипочечного синтеза простагландинов. Известно, что постоянный прием НПВП вызывает у пациентов увеличение АД в среднем на 5,0 мм рт. ст. Характерным свойством НПВП является также взаимодействие с гипотензивными препаратами, в основе гипотензивного действия которых лежат преимущественно простагландин-зависимые механизмы. Назначение НПВП пациентам, получающим по поводу АГ β-адреноблокаторы, ингибиторы АПФ и диуретики, приводит к снижению гипотензивного эффекта [8, 9].
Нимесулид был разработан еще в 1985 г. и является одним из первых НПВП, при изучении которого продемонстрирована более высокая селективность в отношении ЦОГ-2 и накоплен большой клинический опыт. В многочисленных исследованиях in vitro и in vivo было показано, что нимесулид примерно в 5–20 раз более селективно ингибирует ЦОГ-2, чем ЦОГ-1. Большой интерес представляет и тот факт, что нимесулид обладает широким спектром ЦОГ-независимых эффектов, которые могут определять его противовоспалительную, анальгетическую и хондропротективную активность [1, 2, 5, 7, 11, 12].
Нимесулид хорошо переносится больными и редко вызывает развитие серьезных побочных эффектов, требующих отмены препарата. По результатам ряда исследований, частота побочных эффектов, развивающихся на фоне приема нимесулида, достоверно не отличается от плацебо или ниже, чем при приеме других НПВП. Например, по данным мета-анализа, у больных, получавших нимесулид, общая частота побочных реакций со стороны ЖКТ была значительно ниже (8,7%), чем при назначении других НПВП (16,8%). Низкую частоту поражения ЖКТ на фоне лечения нимесулидом связывают не только с ЦОГ-2-селективностью препарата, но и с антигистаминным действием, приводящим к снижению секреции соляной кислоты в желудке [6, 10, 13].
Таким образом, нимесулид относится к селективным ингибиторам ЦОГ-2, сравним по эффективности с «классическими» НПВП, но отличается более благоприятным профилем токсичности. Фармакоэкономический анализ свидетельствует о преимуществах нимесулида по сравнению с диклофенаком, в первую очередь в связи с более низкой частотой поражения ЖКТ.
Целью нашего исследования явилось изучение эффективности и переносимости найза (нимесулида) у больных РА в сравнении с ортофеном (диклофенаком).
Материалы и методы
Оба НПВП назначались случайным способом 40 больным с момента первого установления диагноза РА, согласно критериям Американской коллегии ревматологов. Найз применялся в виде таблеток по 100 мг дважды в день, ортофен — в виде таблеток по 25 мг в суточной дозе 150 мг. Одновременно всем больным проводилась базисная терапия, преимущественно метотрексатом или сульфасалазином. Эффективность и переносимость НПВП оценивались через 3 нед. от начала лечения, т. е. в те сроки, когда эффект базисных препаратов еще не имел клинической значимости.
В I группе из 20 пациентов, получавших найз, было 14 женщин и 6 мужчин, средний возраст пациентов составил 55,1 года, длительность суставного синдрома к моменту установления диагноза — от 3 до 14 мес., в среднем — 7,25 мес. Во II группе из 20 больных, получавших ортофен, было 18 женщин и 2 мужчин, средний возраст больных — 42,75 года, длительность суставного синдрома — от 2 до 14 мес., в среднем — 5,65 мес. Клиническая характеристика обеих групп представлена в таблице 1.
Результаты лечения оценивались по динамике показателей суставного синдрома (суставной индекс Ричи (СИ), счет болезненных суставов (СБС), счет припухших суставов (СПС), продолжительность утренней скованности (мин), выраженность боли по визуально-аналоговой шкале (ВАШ)) и на основании общей оценки эффективности лечения, по мнению врача и больного. Кроме того, у всех больных оценивалась динамика АД на фоне лечения НПВП.
Результаты
В I группе на фоне лечения найзом в суточной дозе 200 мг за 3 нед. лечения достигнута достоверная динамика показателей суставного синдрома. При этом эффективность терапии оценена 17 пациентами (85%) как хорошая и 3 (15%) — как удовлетворительная. По мнению врача, в 16 случаях (80%) наблюдалась хорошая эффективность препарата, в 4 случаях (20%) — удовлетворительная (рис. 1). Переносимость найза у 85% была хорошей, только у 2 больных (10%) отмечались изжога и гастралгии, у 1 больного (5%) — чувство тяжести в эпигастральной области. Однако при фиброгастроскопии у этих пациентов не выявлено эрозивного повреждения слизистой оболочки желудка. В группе больных, принимавших найз, не потребовалось отмены препарата ни у одного больного.
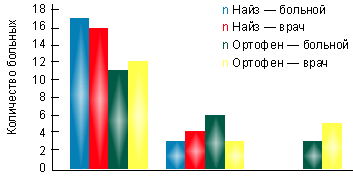 |
| Рисунок. Оценка эффективности препаратов на основании мнения больного и врача |
Во II группе на фоне терапии ортофеном в суточной дозе 150 мг через 3 нед. также отмечена существенная динамика показателей суставного синдрома. Однако оценка эффективности терапии показала, что только 11 пациентов (55%) оценили эффективность препарата как хорошую, 6 (30%) — как удовлетворительную и трое больных (15%) признали ее неудовлетворительной. По мнению лечащего врача, достаточная эффективность ортофена, соответствующая градации «хорошая», отмечалась в 12 случаях (60%), удовлетворительная — в 3 (15%) и неудовлетворительная — в 5 (25%) случаях (рис.).
Переносимость препарата ортофен была хуже, чем у найза: у 9 пациентов (45%) отмечались симптоматические побочные эффекты, причем у 3 больных (15%) потребовалась отмена препарата через 2 нед. от начала лечения в связи с выявленным при ФГДС эрозивным поражением слизистой оболочки антрального отдела желудка. В целом из побочных эффектов чаще отмечались изжога — у 7 (35%) пациентов, гастралгии — у 8 (40%), тошнота — у 4 (20%) и диарея — у 2 (10%) больных.
Особый интерес представляет влияние исследуемых НПВП на уровень АД, так как из 40 больных у 15 имелась сопутствующая ГБ, по поводу которой проводилась гипотензивная терапия. Динамика уровня АД в обеих группах на фоне лечения найзом и ортофеном представлена в таблице 2. Следует отметить, что терапия найзом не требовала усиления проводимой гипотензивной терапии (β-блокаторами, ингибиторами АПФ, диуретиками) и не вызывала повышения АД у ранее нормотензивных пациентов. В то же время лечение ортофеном потребовало коррекции доз гипотензивных препаратов у 4 (66,7%) из 6 больных ГБ и вызвало повышение АД у 5 (25%) женщин в постменопаузе с исходно высоконормальным АД. Данный эффект неселективного НПВП — ортофена — следует считать предсказуемым, особенно с учетом характера проводимой гипотензивной терапии. Все больные ГБ получали в разных комбинациях β-адреноблокаторы, ингибиторы АПФ и диуретики; при этом ни одному пациенту не был назначен дигидропиридиновый антагонист Са — амлодипин, который является препаратом выбора для лечения АГ в условиях терапии НПВП.
Таким образом, результаты открытого клинического исследования показали, что препарат найз у больных РА проявляет выраженную противовоспалительную активность, превосходящую диклофенак. При этом найз характеризуется хорошей переносимостью, малым числом симптоматических побочных эффектов и превосходит с этой точки зрения наиболее широко применяемый в клинической практике ортофен. Дополнительным преимуществом препарата найз можно считать менее выраженное влияние на уровень АД. При назначении найза не требовалось увеличения дозы гипотензивных препаратов. С учетом высокой распространенности эссенциальной гипертензии в популяции, взаимодействие НПВП с наиболее часто используемыми гипотензивными средствами представляется актуальной проблемой. Ревматические заболевания, требующие постоянной терапии НПВП, часто сочетаются с АГ. При этом у большинства больных ГБ коррекция АД может достигаться только благодаря комбинированной антигипертензивной терапии, а монотерапия дигидропиридиновыми антагонистами Са признается недостаточно эффективной. Следовательно, в большинстве случаев при лечении воспалительных ревматических заболеваний у лиц, страдающих ГБ, невозможно полностью нивелировать отрицательное взаимодействие «стандартных» НПВП с основными кардиологическими препаратами — β-адреноблокаторами, ингибиторами АПФ и диуретиками. В такой ситуации представляется рациональным выбор для проведения противовоспалительной терапии специфических ингибиторов ЦОГ-2, представителем которых является найз.
Литература
И. М. Марусенко, кандидат медицинских наук
Н. Н. Везикова, кандидат медицинских наук, доцент
В. К. Игнатьев, доктор медицинских наук, профессор
Петрозаводский университет, кафедра госпитальной терапии
Нестероидные противовоспалительные препараты при остеохондрозе
Нестероидные противовоспалительные препараты – группа лекарств, предназначенных для снятия боли, воспаления, жара в организме. При лечении заболеваний опорно-двигательного аппарата используются в составе комплексной терапии как средства, устраняющие боли
ДОСТУПНЫЕ ЦЕНЫ НА КУРС ЛЕЧЕНИЯ
Мягко, приятно, нас не боятся дети
ДОСТУПНЫЕ ЦЕНЫ НА КУРС ЛЕЧЕНИЯ
Мягко, приятно, нас не боятся дети
Нестероидные противовоспалительные препараты (НПВП) или средства (НПВС) – это группа лекарственных веществ, которые обладают обезболивающими, противовоспалительными и жаропонижающими свойствами. Термин «нестероидные» в названии медикаментов указывает на их отличие от глюкокортикоидов, которые параллельно с вышеуказанными качествами несут в себе массу нежелательных побочных эффектов, присущих стероидам.
Первое противовоспалительное вещество было получено из коры ивы в 1829 году, это была салициловая кислота. На тот момент главными обезболивающими препаратами считались опиаты, которые вызывали быстрое привыкание, угнетали психику и дыхательные функции, обладали седативными качествами.
С тех пор нестероидные средства прочно заняли свои позиции в медицинской практике при лечении заболеваний, проявляющихся мышечными болями, лихорадкой, воспалением и подобными состояниями. Современная медицина значительно расширила список нестероидных противовоспалительных препаратов, которые сочетают в себе высокую эффективность, улучшенную переносимость и минимум побочных эффектов. Кроме того, большую часть подобных лекарств можно приобрести в аптечных сетях по достаточно доступным ценам без рецепта доктора.
При болях в спине, остеохондрозе, радикулите, люмбалгии, невралгиях и прочих заболеваниях опорно-двигательного аппарата НПВП используются для устранения болевых ощущений, снятия спазмированности и воспаления мягких тканей, что позволяет частично восстановить двигательные возможности пациента. При этом следует помнить, что противовоспалительные средства только купируют боль, но не являются лекарством от основного заболевания.
Механизм воздействия
Основным и главным элементом воздействия НПВС является ингибирование (подавление) синтеза (выработки) простагландинов из арахидоновой кислоты. Простагландины – медиаторы воспалительных реакций, которые провоцируют локальное расширение сосудистого русла в очаге патологии, отек, спазм, экссудацию, миграцию лейкоцитов и прочие явления.
Другие биологически активные качества препаратов:
Менее выраженные механизмы воздействия:
Классификация НПВС
Нестероидные противовоспалительные препараты подразделяются по активности основного воздействия и химическому составу:
При этом по нарастанию противовоспалительного воздействия на организм человека, лекарственные препараты можно расставить в следующем порядке: аспирин, амидопирин, ибупрофен, напроксен, кетопрофен, пироксикам, диклофенак, флурбипрофен, индометацин.
По нарастанию анальгезирующих качеств: аспирин, ибупрофен, напроксен, пироксикам, амидопирин, флурбипрофен, индометацин, диклофенак натрия, кетопрофен, кеторолак.
Показания к применению
Нестероидные противовоспалительные средства рекомендуется использовать для лечения хронических и острых заболеваний, связанных с возникновением воспаления, болевого синдрома, повышения температуры.
Наиболее часто НПВС назначаются при:
Противопоказания
Несмотря на все положительные качества противовоспалительных препаратов, не стоит забывать, что и они имеют определенные побочные эффекты. Наиболее часто они связаны с пищеварительным трактом и почками (так как большинство НПВС являются кислотами), а именно:
Кроме того, препараты аспириновой группы противопоказаны детям до 12 лет, аспирин и индометацин вызывают приступы бронхиальной астмы. Со стороны сердечно-сосудистой системы возможно нарушение свертываемости крови, цитопения, инфаркт миокарда, инсульт, тромбоз периферических сосудов и прочие нарушения.
Гораздо реже при лечении противовоспалительными лекарствами наблюдаются:
Список основных препаратов, используемых при остеохондрозе
Индометацин. Рекомендуется для системного применения при лечении остеохондроза, остеоартрита, спондилита, подагры, ревматизма, болей в позвоночнике и прочих заболеваний. Принимается в виде таблеток, капсул во время или после еды, ректальных свечей в дозировке 25-50 мг 2-3 раза в сутки, но не более 200 мг. Может оказывать побочное воздействие на желудочно-кишечный тракт и нервную систему (головокружение, депрессия, шум в ушах, нарушение зрительных функций).
Ибупрофен. Применяется при радикулитах, артрозах, деформирующем остеоартрозе, анкилозирующем спондилите, подагре, бурсите, инфекционно-воспалительных заболеваниях структур скелета. Выпускается в виде гелей, мазей, таблеток, капсул, ампул, суппозиториев. Назначается по 0,4-0,8 г 3-4 раза в сутки после еды для лечения заболеваний опорно-двигательного аппарата. Для устранения болевого синдрома, при травмах мягких тканей или растяжении связок – 1,2-2,4 г в сутки, разделенных на несколько приемов. Может вызывать изжогу, диарею, тошноту, головокружения, аллергические реакции и пр.
Диклофенак. Используется для посттравматического лечения суставов и мягких тканей, мышечных болевых синдромов, отечности и воспалений, ревматических и неревматических мышечных болей. Выпускается в виде таблеток различной дозировки, покрытых оболочкой и растворяющихся в желудке, растворов для инъекций, ректальных свечей, гелей и мазей различной концентрации. Суточная доза при приеме внутрь не должна превышать 150 мг, для 1% геля – 2-4 г, 5% геля – 2 г. Местной реакцией на применение лекарства может быть зуд, покраснение, экзема, фотосенсибилизация, шелушение, системной – отек Клинке, бронхоспазм, крапивница, гастрит, язва.
Кетонал. Средство предназначено для симптоматической терапии дегенеративно-дистрофических заболеваний скелета, а также для снятия болевых синдромов различной этиологии. Таблеточная форма препарата назначается для приема внутрь после еды, запивая водой или молоком (не менее 100 мл), в дозировке 150-200 мг, разделенных на 2 приема. Можно чередовать употребление: утром – в виде таблеток, вечером – в виде ректальных суппозиториев. Побочные эффекты: тошнота, рвота, диарея, метеоризмы, головокружения, сонливость, быстрая утомляемость, нервозность, аллергические реакции.
Мовалис. Прописывается в острый начальный период для лечения или краткосрочными курсами для устранения симптомов артритов, остеохондроза, спондилита, ревматизма и прочих поражений опорно-двигательного аппарата. Выпускается в виде гелей, мазей, таблеток, покрытых оболочкой, ампул, суппозиториев. Препарат принимается во время еды, запивая достаточным количеством воды в дозировке 7,5-15 мг/сут, допускается комбинирование различных форм вещества (таблетки, свечи, уколы), но суточная доза не должна превышать 15 мг. Нежелательные последствия, иногда вызываемые лекарством: изменение состава крови, сонливость, дезориентация, колит, гастрит, язва, перфорация ЖКТ, нефрит, повышение артериального давления, одышка, аллергия.
Пироксикам. Рекомендуется для лечения воспалительных и дегенеративно-дистрофических заболеваний суставов и позвоночника, болевого синдрома и отечности сухожилий, мышц, суставов, после перенапряжения, травм, хирургических операций, инфекционно-воспалительных поражений тканей организма. Принимается внутрь после еды, запивая достаточным количеством воды в дозе 20-40 мг, разделенных на 1-2 приема в сутки. В числе побочных эффектов могут возникать: слабость, бессонница, депрессия, сухость во рту, стоматит, отрыжка, запоры, учащенное сердцебиение, скачки артериального давления и прочие проявления.