Аскариды и токсокары чем лечить
Что такое токсокароз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 13 лет.
Определение болезни. Причины заболевания
Токсокароз — зоонозный гельминтоз с фекально-оральным механизмом передачи, протекающий у человека исключительно в форме тканевого паразитирования личиночной стадии паразита (биологический тупик), проявляющийся в форме токсико-аллергических реакций различной степени выраженности и полиорганных поражений в зависимости от численности и локализации паразитов. Имеет склонность к длительному рецидивирующему течению.
Этиология
Тип — Nemathelmintes (круглые черви)
Класс — Nematoda (собственно круглые черви/нематоды)
Род — Toxocara (от греч. toxon — стрела, cara — голова)
Виды — Toxocara canis (поражает человека и животных семейства псовых), Toxocara mistax (поражает животных семейства кошачьих), Toxocara vitulorum (поражает крупный рогатый скот), Toxocara leonina (возникает у львов).
В патологии человека основная роль принадлежит Toxocara canis, роль остальных видов дискутабельна — они способны поражать людей с дефектами иммунной системы, в остальных случаях чаще всего наблюдается спонтанное выздоровление без каких-либо значимых клинических проявлений.
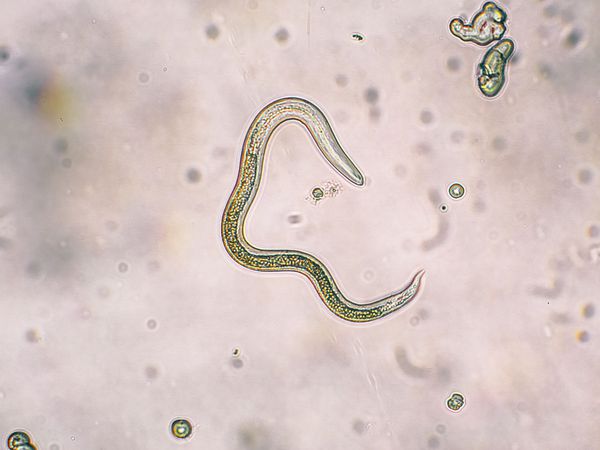
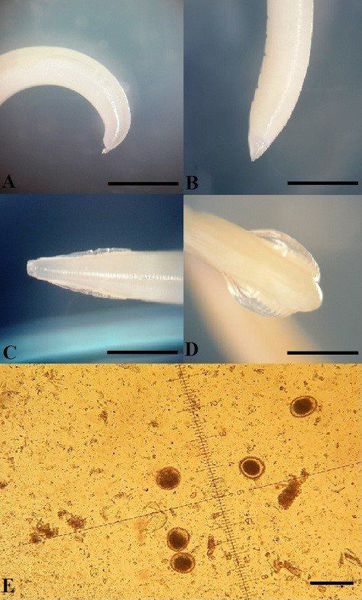
Взрослые половозрелые токсокары — это раздельнополые достаточно крупные черви с заострёнными концами (имеют некоторое сходство с аскаридами человека). Кутикула светло-жёлтого цвета. Длина самки достигает 18 см (с прямым хвостом), в передней половине тела есть отверстие вульвы. Самцы вырастают до 10 см (с загнутым хвостовым концом и консусовидным придатком). Головной конец имеет вид широких крыльев (вздутия кутикулы размерами до 2,3×5×0,3 мм), что является внешним отличительным признаком. Есть расширенный пищевод (желудочек). Продолжительность жизни взрослых особей — до шести месяцев.
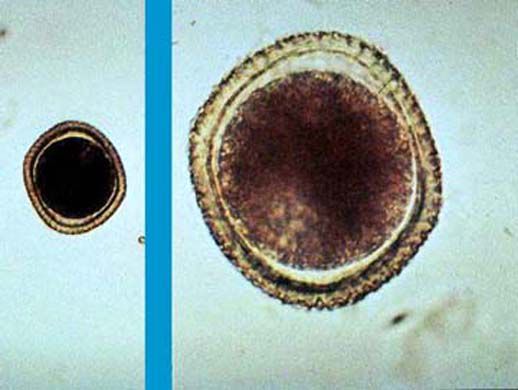
За сутки самка может откладывать свыше 200 тысяч яиц в кишечнике животного (собаки). Яйца имеют округлую форму, размерами 65-45 мкм, покрыты плотной бугристой оболочкой, коричневого цвета различных оттенков, прекрасно защищающей их от неблагоприятного воздействия внешней среды. Внутри яиц находятся тёмные бластомеры (зародыши). С калом незрелые яйца паразита (неинвазионные) попадают в окружающую среду (почву), где при благоприятных условиях (достаточная влажность — не ниже 70%, температура — не ниже 14°C и насыщение кислородом) происходит созревание яиц (в среднем около 2-3 недель) и образование в них инвазионной личинки, длительно сохраняющей свою жизнеспособность (до 3-5 лет). Яйца обладают высокой устойчивостью к действию агрессивных условий внешней среды, длительно выживают даже под воздействием ядов (таких, как медный купорос, сулема и другие).
У животных токсокары паразитируют в тонком кишечнике до 6 месяцев, питаясь содержимым кишечника (инвазированность может достигать несколько сотен гельминтов).
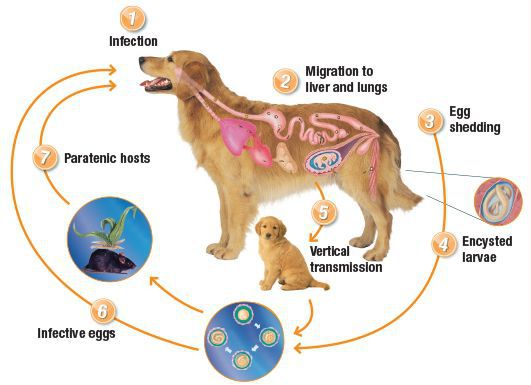
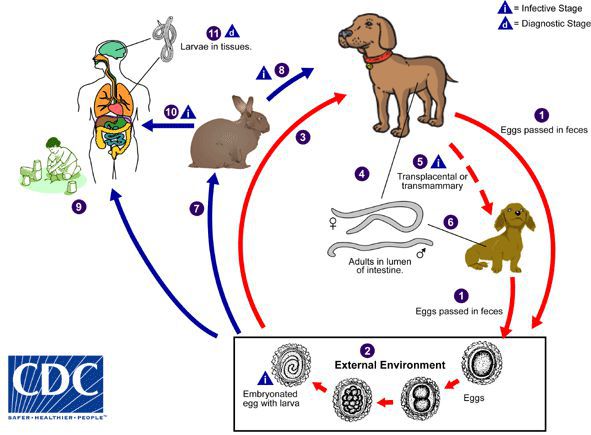
В жизни паразита у животного выделяют несколько различных путей развития. Основной происходит по аналогии с циклом развития аскарид при аскаридозе. Он протекает у молодых животных — щенков до двух месяцев. После заглатывания инвазионных яиц в тонкий кишечник собаки выходят личинки, которые, пробуравливая его стенку, попадают в систему воротной вены и, мигрируя по кровеносным сосудам, попадают в лёгочную капиллярную сеть. Большая часть личинок поднимаются по воздухоносным путям, они вновь заглатываются, попадая снова в тонкий кишечник. Там личинки растут и через пять недель от момента заражения начинают выделять яйца. Другая часть личинок у молодняка и в основном у взрослых животных проникает через стенку лёгочной вены в большой круг кровообращения, после чего разносится и оседает в самых разнообразных органах и тканях, где личинки образуют гранулематозные инфильтраты и пребывают в «спящем» состоянии в течении многих лет (соматические личинки).
У самок в период беременности на фоне гормональной и иммунологической перестройки организма дремлющие личинки возобновляют активность и, совершая миграцию, трансплацентарно инвазируют плод, т.е. новорождённый щенок уже оказывается инвазирован паразитом. Также возможна передача личинок с молоком при кормлении.
Имеет место заражение животного и при поедании факультативных хозяев (резервуарных, паратенических), инвазированных личинками — грызунов, скота, червей и других. По этой причине реализуются дополнительные варианты заражения.
Таким образом, источником распространения яиц паразита в окружающую среду в основном являются щенки, у которых наблюдается преимущественно гепатопульмональный вариант циркуляции возбудителя, а взрослые животные, как правило, являются лишь носителями личинок паразита в тканях даже при многократных заражениях за время жизни. [1] [4] [6] [8] [10]
Эпидемиология
Источником инвазии являются преимущественно собаки (щенки), с калом которых яйца паразита попадают в почву. Менее значимыми источниками являются другие представители псовых (лисы и волки).
Учитывая, что 1 гр фекалий собаки содержит до 15-30 тысяч яиц паразита, а распространённость собак и особенно их бездомных собратьев в последнее время крайне велика, степень загрязнённости яйцами токсокар окружающей нас среды огромна. Например, по самым скромным подсчётам, контаминация детских песочниц и газонов в Санкт-Петербурге — не менее 85%, что создаёт реальную угрозу инфицирования людей.
Механизм заражения — фекально-оральный.
Внутриутробная передача личинок от матери-плоду или через молоко у человека не доказана. Люди не являются источником распространения токсокар, так как в их организме черви существуют лишь в виде тканевых личинок и никогда не достигают половой зрелости (не паразитируют в кишечнике и не откладывают яиц), т.е. люди являются эволюционным тупиком в круговороте жизни данного вида паразита.
Определённую роль в распространении яиц паразита играют тараканы (могут поедать и выделять в жизнеспособном виде часть яиц) и мухи (как механические переносчики).
Восприимчивость — всеобщая. В реализации клинически выраженной формы заболевания играет роль количество попавших в организм яиц паразита и свойства иммунной системы. Наиболее часто заболевают дети (больше мальчики). [1] [5] [6] [8] [10]
Симптомы токсокароза
Клиническая симптоматика токсокароза не имеет специфичных симптомов. Она достаточно сходна с симптоматикой других тканевых гельминтозов в соответствующие фазы развития и выражается в виде синдромальных проявлений различной интенсивности и в разнообразных сочетаниях.
Широко распространено т.н. токсокароносительство — когда явные клинические признаки заболевания отсутствуют, и диагноз можно поставить лишь на основании обнаружения титра антител (обычно в низкой концентрации). Также распространена субклиническая инвазированность («скрытый токсокароз») — когда на фоне выявления антител к токсокарам в периферической крови появляется незначительная эозинофилия, клинические проявления не выявляются или не могут быть прямо связаны с токсокарами — температура 37,1-38,0°C, увеличение лимфоузлов, частые простудные заболевания, аллергизация и другое.
Следует выделять проявления висцерального (тканевого) и глазного токсокароза.
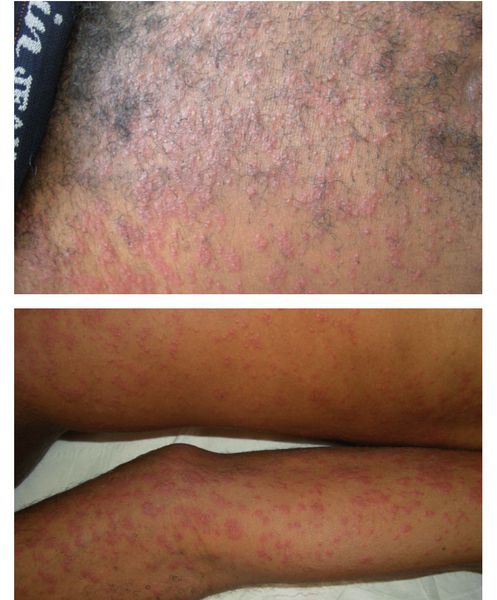
При висцеральной форме заболевания через 2-3 недели от момента заражения в острую фазу возникает повышение температуры до фебрильных цифр (38,0-39,0°C), слабость, головные боли, повышенная утомляемость, бессонница, полиморфные высыпания различных участков тела (в основном по типу крапивницы), иногда отёк Квинке, боли в мышцах, увеличение периферических лимфоузлов (умеренная болезненность), сухой кашель, нередко с обструктивным компонентом.
Детям при такой форме заболевания характерен синдром Леффлера (выраженный непроходящий кашель, гиперлейкоцитоз за счёт эозинофилии, летучие эозинофильные инфильтраты в лёгких), а также диффузные боли в животе и неустойчивый стул. Увеличиваются размеры печени и селезёнки, нарастает эозинофилия крови и гипергаммаглобулинемия (повышенная концентрация иммуноглобулинов в крови).
Как правило, проявления острой фазы продолжаются не более одного месяца и по мере улучшения общего самочувствия и стихания гиперэозинофилии купируются. Однако в некоторых случаях, особенно у детей, острая фаза приобретает затяжное течение с ярко выраженным лёгочным синдромом, проявляющимся в виде длительного мучительного кашля, обструкциями (непроходимость дыхательных путей) и ателектазами (спадение доли лёгкого), приступами удушья, нередко в дальнейшем с формированием гиперреактивности трахеобронхиального дерева (отличительная особенность — повышенная чувствительность к физиологическому раствору) и развитием бронхиальной астмы.
Чем раньше распознано заболевание и начата специфическая противопаразитарная терапия, тем больше шансов на быстрое купирование болезни, регресс бронхолёгочной симптоматики и снижение риска развития бронхиальной астмы. При длительно персистирующей инфекции и развитии астмы даже полное излечение от токсокароза не даёт существенного клинического эффекта, так как уже формируется патологический аутоиммунно-аллергический комплекс.
Возможно токсико-аллергическое поражение сердца, проявляющиеся учащённым сердцебиением, болями в области сердца, нарушением ритма, глухостью тонов при аускультации, колебаниями артериального давления и кардиомиопатией. Описан синдром Леффлера II — эозинофильный васкулит (воспаление стенок сосудов), пристеночный фибропластический эндокардит (воспаление внутренней оболочки сердца).
Возможно развитие поражения нервной системы в виде судорожного синдрома, нарушения психики, развития изолированного и/или сочетанного поражения отдельных нервов, менингитов и менингоэнцефалитов (повреждающее действие как личинок, так и токсико-аллергической интоксикации).
В хроническую фазу болезни при слабой выраженности общеинфекционной симптоматики проявления острого периода претерпевают значительную регрессию и приобретают характер преимущественно изолированных органных поражений — бронхиальная астма, миокардит, дерматит, гепатит, астеноневротический синдром нетипичного течения.
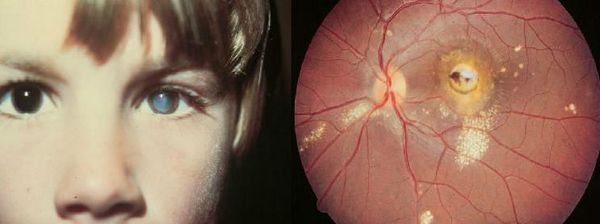
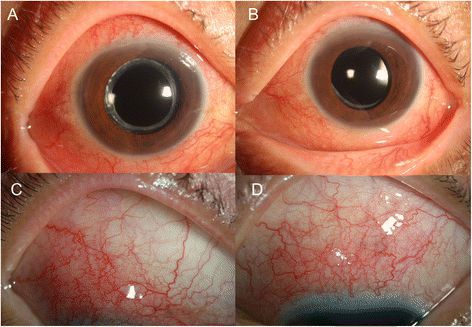
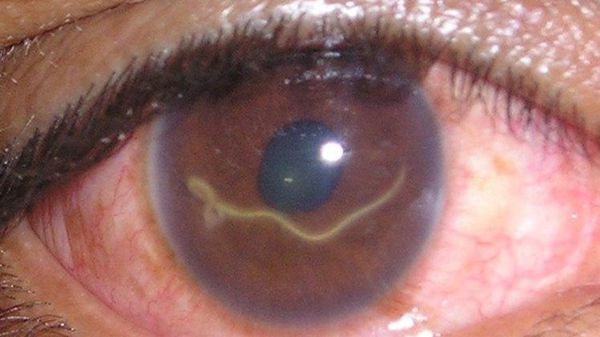
Глазной токсокароз проявляется обычно изолированным поражением одного глаза (без проявлений висцерального процесса). Он характеризуется в зависимости от локализации (задний гранулематозный хориоретинит, кератит, эндофтальмит, увеит, иридоциклит и другое) и может проявляться снижением остроты зрения, потерей части зрительной картинки, нарушением цвето- и световосприятия. Иногда возникает отёк параорбитальной области, гиперемия тканей и экзофтальм (выпучивание глаза). [1] [2] [6] [7] [9]
Патогенез токсокароза
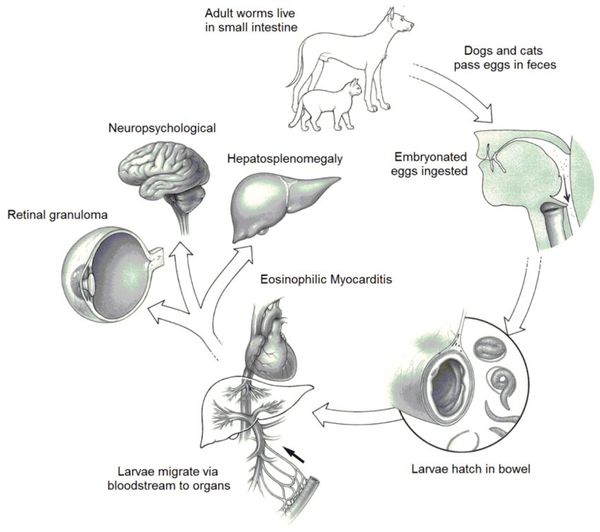
Входные ворота — ротовая полость. При проглатывании яиц токсокар они попадают в тонкий кишечник, где разрушается оболочка яйца, и живые личинки выходят в просвет кишки, пенетрируют (пробуравливают) стенку кишечника и с током крови через систему воротной вены попадают в печень. Там одна их часть задерживается (частично гибнет), окружается воспалительными инфильтратами с образованием паразитарных гранулём, а другая часть через печёночные вены попадает в правые отделы сердца, откуда проникает в лёгочную капиллярную сеть и разносится по большому кругу кровообращения, заселяя все возможные органы (кожу, мышцы, глаза, головной мозг, щитовидную железу и другие) и ткани (также оседая в них и формируя воспалительно-аллергические инфильтративные образования).
В этих органах, в зависимости от индивидуальных свойств иммунной системы и массивности заражения, личинки могут сохраняться десятилетиями, обуславливая весь комплекс патологических изменений. При значимом снижении иммунитета или влиянии неблагоприятных факторов не исключается повторная миграция.
В процессе миграции личинки паразита механически травмируют ткань человеческого организма, вызывая воспалительные реакции, геморрагии, некрозы.
Главное же воздействие на организм оказывают иммунопатологические реакции, связанные с выраженным аллергическим действием антигенов токсокар (аллергические реакции немедленного и замедленного типов). Происходит сенсибилизация иммуноаллергических клеток и последующее резкое повышение выброса медиаторов аллергии и выработки IgE, что обуславливает выраженный каскад реакций острой аллергии (крапивница и сокращение бронхов). Это в какой-то мере может стать позитивным звеном и привести к гибели части личинок, однако часто характер процесса несёт чрезмерный ответ и становится патологическим для организма.
В отсроченный период в результате реакций гиперчувствительности замедленного типа происходит контакт предварительно сенсибилизированных лимфоцитов с антигенами токсокар, что проявляется в образовании специфических иммунных комплексов и последующим привлечением в околопаразитарные ткани макрофагов, эозинофилов и иммунных кластеров с формированием паразитарных гранулём в любых человеческих органах (преимущественно в печени, лёгких, сердце, лимфатических узлах, коже и другое) с длительно протекающими токсико-аллергическими поражениями органа и организма целом.
С течением времени гранулёмы могут обрастать капсулой фиброзного характера, что несколько отграничивает патологический паразитарно-аллергический процесс и может являться препятствием при диагностике и лечении.
Преимущественная локализация гранулём определяет главенствующие клинические и патоморфологические изменения, например, обнаружено сходство изменений в лёгких при токсокарозе и бронхиальной астме: по статистике около 50% случаев бронхиальной астмы ассоциировано с токсокарозом и выявлением специфических антител при ИФА.
Длительное паразитирование у человека может приводить к функциональному истощению и извращению иммунологических реакций, что проявляется общим снижением и неадекватными реакциями иммунитета на какие-либо стандартные раздражители.
При малоинтенсивном заражении вследствие слабого иммунного ответа возможно изолированное единичное проникновение личинок в глаза (преимущественно в области сетчатки вблизи зрительного нерва или желтого пятна), что выражается развитием кровоизлияний, образованием эозинофильно-лимфоцитарных гранулём, длительно протекающими воспалительными процессами (воспалительно-аллергическими) различных сред глаза (в зависимости от локализации гельминта) и иногда приводит к потере органа зрения. [1] [6] [10]
Классификация и стадии развития токсокароза
Наименование заболевания по МКБ-10: В83.0 Висцерaльнaя формa зaболевaний, вызывaемых мигрaцией личинок гельминтов [висцерaльнaя Larva migrans]. Токсокaроз.
По течению заболевание бывает:
По клинической форме выделяют:
Степени тяжести заболевания:
Характер течения токсокароза:
Осложнения токсокароза
Диагностика токсокароза
Лабораторная диагностика:
Дифференциальная диагностика:
Лечение токсокароза
Необходимость лечения определяется совокупностью клинических и лабораторных проявлений заболевания.
Лёгкие и абортивные формы как правило не нуждаются в специфической терапии, так как организм самостоятельно производит деструкцию и удаление паразитов (если их небольшое количество) и требуют лишь симптоматического лечения — назначения противоаллергических и дезинтоксицирующих средств.
При более серьёзных поражениях проводиться комплексное противопаразитарное лечение с применением специфических противопаразитарных препаратов (действующих на тканевые формы червей) под контролем общелабораторных показателей в сочетании с дезинтоксикацией, поддержкой функции печени, снижением аллергической составляющей и иногда гормонотерапией.
При острых формах (особенно у детей) лечение проходит в стационаре под постоянным контролем медперсонала, при хронических формах — обычно в амбулаторном порядке.
Контроль излеченности путём определения титра антител в ИФА и общих анализов осуществляется не ранее, чем через 5-6 месяцев после окончания лечения, так как в первые месяцы из-за распада личинок и капсул количество антител резко повышается и может быть неверно истолковано.
Также показано диспансерное наблюдение в течения 6-12 месяцев в зависимости от конкретных проявлений с периодическим лабораторным обследованием. [1] [2] [6]
Прогноз. Профилактика
Как правило, при малоинтенсивных заражениях и своевременно начатом лечении прогноз благоприятный. При тяжёлых и запущенных формах (несвоевременное распознавание и лечение) возможно развитие осложнений (бронхиальная астма), редко — летальный исход (при ВИЧ в стадии СПИДа, других СПИД-ассоциированных состояниях, а также гипермассивной инвазии).
Профилактика и противоэпидемические мероприятия:
Современный взгляд на проблему гельминтозов у детей и эффективные пути ее решения
По данным Всемирной организации здравоохранения, из 50 млн человек, ежегодно умирающих в мире, более чем у 16 млн причиной смерти являются инфекционные и паразитарные заболевания. В структуре инфекционных заболеваний кишечные гельминтозы находятся на тре
По данным Всемирной организации здравоохранения, из 50 млн человек, ежегодно умирающих в мире, более чем у 16 млн причиной смерти являются инфекционные и паразитарные заболевания. В структуре инфекционных заболеваний кишечные гельминтозы находятся на третьем месте. Согласно оценке Всемирного банка, экономический ущерб от кишечных гельминтозов занимает четвертое место среди наносимого всеми болезнями и травмами. Учитывая важность борьбы с паразитарными болезнями для многих стран, 54-я сессия Всемирной ассамблеи здравоохранения в 2001 г. одобрила стратегию борьбы с геогельминтозами до 2010 г. [5].
В РФ ежегодно на гельминтозы обследуются более 10 млн человек, большинство из них — дети. В 2002 г. было выявлено 813 тыс. зараженных, из них 681 тыс. (83,8%) составили дети в возрасте до 14 лет [4]. У детей встречаются более 15 видов гельминтов, из которых наиболее распространены энтеробиоз, аскаридоз, описторхоз, дифиллоботриоз, трихоцефалез, гименолепидоз. В последние годы все чаще регистрируется токсокароз, что связано с широким внедрением в практику диагностической тест-системы для его выявления.
В структуре гельминтозов ведущее место занимают энтеробиоз (91%) и аскаридоз (8%). Среди всех инвазированных на долю детей приходится 92,3% случаев энтеробиоза, 71,1 % — аскаридоза, 61,5% — трихоцефалеза и 66,2% — токсокароза.
Заболеваемость энтеробиозом и аскаридозом детей в сельской местности значительно выше, чем в городах, что, по-видимому, связано с разными санитарно-гигиеническими условиями в детских учреждениях города и села, а также со степенью загрязненности яйцами гельминтов окружающей среды (рис. 5).
Аскаридоз представляет собой один из наиболее распространенных гельминтозов, в формировании очагов которого основное значение имеет загрязненность почвы яйцами аскарид. В 2002 г. выявлено 74 196 случаев аскаридоза, в том числе 52 801 — у детей в возрасте до 14 лет, по сравнению с 2001 г. заболеваемость увеличилась на 3,5% и составила 217,7 на 100 тыс. детей.
Заболеваемость трихоцефалезом при явной тенденции к снижению за последнее десятилетие в 2002 г. выросла на 2,8% и составила 7,4 на 100 тыс. детей. Трихоцефалез регистрируется в основном в Южном федеральном округе (Республика Дагестан, Чеченская Республика).
Энтеробиоз по-прежнему занимает первое место по степени распространенности среди других гельминтозов. В 2002 г. зарегистрировано 614 955 случаев заболевания среди детей, что составило 2535,5 на 100 тыс. пациентов.
Максимальное число инвазированных энтеробиозом в 2002 г. выявлено в Сибирском, Северо-Западном, Уральском, Дальневосточном, Приволжском федеральных округах.
Особенностью большинства гельминтозов является хроническое течение заболевания, связанное с длительным присутствием возбудителя заболевания в организме и многократными повторными заражениями. Гельминтозы у детей, как правило, сопровождаются разнообразными неспецифическими клиническими проявлениями: слабостью, утомляемостью, раздражительностью, нарушениями сна, диспепсическими явлениями, замедлением роста и прибавки в весе, снижением иммунного статуса. Важнейшим компонентом патологии при гельминтозах является сенсибилизирующее действие продуктов обмена и выделения гельминтов, приводящее к развитию аллергических реакций в виде атопического дерматита, астматического бронхита, ринита, блефарита и др.
Выборочный анализ результатов диспансеризации 520 детей, проведенной в Свердловском районе г. Перми в 2002 г., показал, что аскаридоз выявлен у 1,35%, а энтеробиоз — у 5,8% обследованных. При этом в среднем показатель числа нарушений состояния здоровья на 1 ребенка у детей с энтеробиозом в группе дошкольников составил 2,5, а у школьников — 2,9. Чаще других отмечались заболевания мочеполовой системы (у девочек), аллергодерматит, анемия, синдром вегетативной дистонии, невропатические состояния и заболевания желудочно-кишечного тракта. Из заболеваний, диагностированных у детей с аскаридозом, наиболее часто встречались синдром вегетативной дистонии, функциональные заболевания желудочно-кишечного тракта, пневмония, аллергодерматит. Среди детей с аскаридозом показатель заболеваемости на 1 ребенка составил в среднем 2,0. В контрольной группе, в которую входили дети без паразитарных болезней (37 человек), среднее число нарушений здоровья было существенно ниже, чем среди инвазированных аскаридозом и энтеробиозом, и составило 0,2. Таким образом, наличие аскаридоза и энтеробиоза приводит к ухудшению общего состояния здоровья детей. При этом ими чаще заражаются дети с имеющимися разнообразными фоновыми заболеваниями, приводящими к ослаблению организма.
Остановимся подробнее на значении в развитии патологии у детей наиболее распространенных гельминтозов — аскаридоза и энтеробиоза [1, 3].
Аскаридоз. Развитие возбудителя аскаридоза (рис. 2, 3) в организме человека происходит с миграцией личинок, вышедших из яиц, по кровеносному руслу через легкие; затем личинки заглатываются с мокротой и развиваются во взрослые особи в кишечнике. Продолжительность жизни аскариды в организме человека составляет несколько месяцев. Аскаридоз оказывает значительное влияние на качество питания и иммунологические механизмы у детей. Аскаридный аллерген является самым сильным из аллергенов паразитарного происхождения. Он может вызывать реакции в легких, коже, конъюнктиве, желудочно-кишечном тракте. Аллергические реакции бывают столь выраженными, что нередко представляют угрозу для жизни ребенка.
Иммунодепрессивным действием аскарид обусловлено отсутствие эффекта от вакцинации и ревакцинации против кори, дифтерии, столбняка, полиовирусов у детей.
Ведущими механизмами патогенеза миграционной стадии аскаридоза являются травмирующее действие личинок и сенсибилизация паразитарными антигенами. При этом в разных органах и тканях возникают 2 основных вида поражений.
В кишечной фазе аскаридоза важными патогенетическими факторами являются способность аскарид, достигающих в длину 20–40 см, к спиральным движениям вперед и стремление проникать в небольшие отверстия (фатеров сосок, дренажные трубки и проч.). Наличие инвазии приводит к гипертрофии мышечных слоев стенки кишечника, уменьшению глубины крипт, изменению химического состава содержимого кишечника, нарушению моторно-секреторной функции желудка и кишечника. Аскариды выделяют ингибиторы трипсина и хемотрипсина, вследствие чего ухудшаются процессы всасывания пищевых веществ, белков, жиров. При аскаридозе развивается функциональная недостаточность пиридоксина, снижается уровень ретинола и аскорбиновой кислоты, уменьшается толерантность к лактазе. Аскаридоз, как правило, сопровождается дисбиозом кишечника.
Часто симптомами кишечной фазы аскаридоза являются тошнота, рвота, диарея, утомляемость, головокружение, плохой сон, боли в животе. Повышенный уровень эозинофилов в периферическом русле крови характерен для миграционной фазы аскаридоза.
Осложнения кишечной фазы аскаридоза: кишечная непроходимость, вызванная клубком взрослых аскарид; перитонит вследствие перфорации кишечной стенки или проникновения аскарид в полость живота через операционный шов; механическая желтуха при миграции гельминтов в общий желчный проток; блокада протоков поджелудочной железы; асфиксия из-за миграции аскарид в верхние дыхательные пути.
Энтеробиоз. Развитие возбудителя энтеробиоза (рис. 1) в организме человека происходит в пределах желудочно-кишечного тракта. Личинки выходят из яиц (рис. 4) и в среднем в течение 2 недель развиваются во взрослые особи, которые паразитируют в нижних отделах тонкого и верхних отделах толстого кишечника. Продолжительность жизни остриц может достигает 100 дней, а состояние инвазированности у детей вследствие повторных заражений может продолжаться намного дольше.
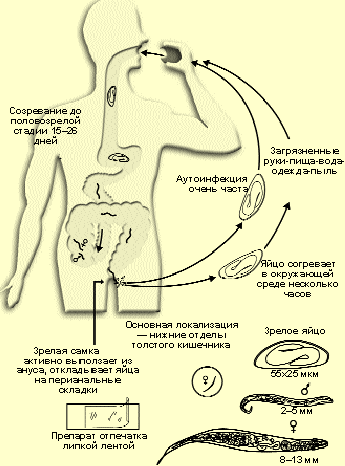 |
| Рисунок 1. Жизненный цикл возбудителя энтеробиоза (по H. C. Jeffrey, R. M. Leach, 1975) |
Воспалительные реакции при энтеробиозе развиваются уже под действием личинок, которые вырабатывают гиалуронидазу, протеолитические ферменты, лектиноподобные вещества, способствующие активации системы комплемента, выделению простагландинов клетками окружающих гельминта тканей хозяина [1, 2, 3].
При энтеробиозе нарушаются процессы всасывания и переваривания пищевых продуктов. У 30–40% инвазированных снижается кислотность желудочного сока вплоть до анацидоза и угнетения пепсинобразующей функции. У большинства детей изменяется микробиоценоз кишечника. Нарушения всасывания и переваривания пищевых веществ в кишечнике приводят к потере массы тела, задерживают рост и развитие ребенка.
Дополнительным фактором патогенеза энтеробиоза является механическое воздействие остриц в кишечнике, ведущее к точечным кровоизлияниям, эрозиям, проникновению бактериальной флоры, в частности возбудителей кишечных инфекций.
Ярким симптомом энтеробиоза является перианальный зуд, возникающий при движении самки во время яйцекладки (рис. 6). Выраженный зуд возникает, как правило, во время сна, чаще ночью, с 23.00 до 1.00 ч. Именно в это время гельминты могут, оставаясь незамеченными, отложить яйца, которые созреют до инвазионной, заразной, стадии уже к утру. Несмотря на кажущуюся безобидность, перианальный зуд тяжело переносится детьми и может сохраняться довольно долго после излечения энтеробиоза в результате формирования стойкого очага возбуждения в коре головного мозга. Осложнениями, возникающими в результате перианального зуда, являются повреждения кожи при расчесах, перианальные прурит, экзема, мокнущий дерматит. Этиологическим агентом воспалительного процесса чаще всего бывают стрептококки.
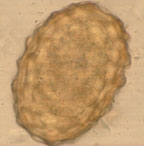 |
| Рисунок 2. Яйцо аскариды (70 мкм) |
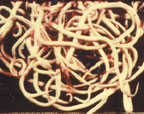 |
| Рисунок 3. Взрослые особи аскарид |
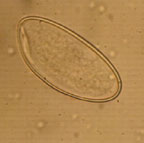 |
| Рисунок 4. Яйцо острицы (50–60 мкм) |
Боли в животе — частый симптом энтеробиоза. Боль преходящего характера отмечается у большинства инвазированных. Иногда острая боль в животе может быть причиной обращения за хирургической помощью. В таких случаях конкретной патологии обнаружить зачастую не удается, выявляется только скопление газов.
В последние годы увеличилось число случаев формирования у детей перианальных гранулем или абсцессов, внутри которых обнаруживались самки остриц или яйца гельминта. В связи с этим целесообразно проводить обследование на энтеробиоз всех детей с данными состояниями.
Во многих случаях энтеробиоз протекает длительно и многократно повторяется. В результате этого нарушается кишечный биоценоз, снижаются антагонистические свойства кишечной микрофлоры по отношению к возбудителям острых кишечных инфекций. У большинства инвазированных детей уменьшается число кишечных палочек и увеличивается доля лактонегативной кишечной флоры. Повышается активность энтерокиназы и щелочной фосфатазы в фекалиях. Так как микрофлора кишечника является одним из факторов, поддерживающих активность ферментов кишечника, развивающиеся вследствие энтеробиоза нарушения процессов переваривания и всасывания пищевых веществ приводят к потере массы тела и задерживают рост и развитие ребенка. Острицы оказывают механическое действие на слизистую кишечника, что ведет к точечным кровоизлияниям, эрозиям, проникновению бактериальной флоры, в частности возбудителей кишечных инфекций. Снижаются антагонистические свойства флоры по отношению к возбудителям брюшного тифа и других кишечных инфекций [1, 3].
В случае миграции остриц в брюшную полость, мочевыводящие и половые пути могут развиваться воспалительные и аллергические реакции вне кишечника.
 |
| Рисунок 5. Заболеваемость городских и сельских детей энтеробиозом и аскаридозом в 2002 г. |
Одним из распространенных осложнений при энтеробиозе является вульвовагинит вследствие проникновения остриц в половые пути и присоединения бактериальных инфекций. В случае развития вульвовагинита у девочки следует назначить паразитологическое обследование на энтеробиоз и при положительном результате провести лечение этой инвазии с одновременным бактериологическим обследованием и при необходимости антибактериальной терапией.
На фоне энтеробиоза у детей часто развиваются инфекции мочевыводящих путей, особенно у девочек, поскольку энтеробиоз служит фактором, предрасполагающим к развитию этого осложнения.
Паразитирование остриц у детей приводит к подавлению неспецифического иммунитета, проявляющемуся снижением уровня a-интерферона в сыворотке крови. Снижение неспецифической резистентности организма ребенка ведет к повышению заболеваемости вирусными, бактериальными инфекциями.
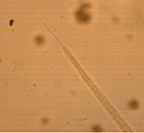 |
| Рисунок 6. Хвостовой конец самки острицы |
Наличие энтеробиоза приводит к снижению эффективности профилактических прививок. Иммунная прослойка против дифтерии исходно ниже среди инвазированных острицами детей. Не развивается защитный иммунитет при первичной вакцинации против этой опасной инфекции, а при ревакцинации во многих случаях иммунный ответ отсутствует. Затрудняется формирование иммунитета при вакцинации против кори столбняка, поэтому для повышения эффективности прививок сначала необходимо убедиться в том, что организм ребенка свободен от возбудителей гельминтозов.
У детей с аллергическими заболеваниями энтеробиоз развивается существенно чаще. В связи с относительно высокой степенью вероятности выявления энтеробиоза у детей с аллергическими заболеваниями пациентам этой группы следует рекомендовать обследование на энтеробиоз и дегельминтизацию в случае выявления инвазии.
Энтеробиоз отрицательно влияет на нервно-психическое развитие детей. Эта инвазия ведет к отставанию от соответствующих возрастных норм. Среди инвазированных энтеробиозом высок процент раздражительных детей, с нарушением процесса засыпания, имеющих отрицательные привычки (грызть ногти, сосать пальцы и др.).
При энтеробиозе у детей существенно снижается уровень меди, цинка и магния в крови. Поскольку недостаток этих микроэлементов может отрицательно влиять на физическое и психическое развитие детей, следует возмещать их потерю, вводя в рацион ребенка определенные продукты, назначая медикаменты (или пищевые добавки) вплоть до нормализации данных показателей после излечения энтеробиоза.
Основные показания к обследованию на гельминтозы:
Диагноз энтеробиоза и аскаридоза ставится только при получении положительных результатов лабораторного паразитологического обследования пациента. При подозрении на энтеробиоз исследуют перианальный соскоб (отпечаток), на аскаридоз — пробы фекалий. На бланке направления в лабораторию следует указать, какой именно гельминтоз врач подозревает у ребенка. От этого будет зависеть выбор наиболее эффективного метода исследования специалистами лаборатории.
Лечение аскаридоза и энтеробиоза
Поиск средств для лечения гельминтозов, в том числе энтеробиоза и аскаридоза, начался много веков назад. Ибн Сина рекомендовал для изгнания остриц принимать девясил и чистотел с сахаром, запивая их водой. Лекарство для изгнания глистов («умерщвления червей»), указанное в «Папирусе Эберса», содержит среди прочих компонентов косточки финика и растения дисарт, сладкое пиво. Салернский кодекс здоровья, который относится к началу XVI века, рекомендует другое средство — мяту [3].
Современный арсенал лекарственных средств, используемых для лечения кишечных гельминтозов, включает значительное количество препаратов различных химических классов. Они применяются как в клинической практике для лечения выявленных больных или паразитоносителей, так и с целью массовой профилактики.
На российском фармацевтическом рынке в настоящее время представлены несколько антигельминтных препаратов, действующих на возбудителей аскаридоза и энтеробиоза (табл. 1).
Наиболее эффективными препаратами для лечения энтеробиоза и аскаридоза являются производные карбаматбензимидазола (мебендазол, медамин) и тетрагидропиримидина (пирантел). Помимо способности к воздействию на зрелые формы гельминтов их отличает высокая овицидная и ларвицидная активность. Препараты этих фармакотерапевтических групп нарушают окислительные процессы, угнетают транспорт глюкозы у гельминтов, действуют на мускулатуру кишечных нематод путем деполяризации их нервно-мышечных соединений и блокируют действие холинэстеразы.
Эффективность лекарственных средств, используемых для лечения энтеробиоза и аскаридоза, очень высока, способ приема весьма прост и рассчитан в первую очередь на детей. Очень важно, что вследствие их приема не активизируется процесс выделения возбудителя в окружающую среду. Таким образом, человек во время лечения не становится более опасным для окружающих. Однако яйца остриц, уже попавшие в окружающую среду, в частности в помещение, сохраняются долго — более 2 недель. Поэтому рекомендуется повторить лечение энтеробиоза через 2-3 недели в той же дозе на тот случай, если гигиенические мероприятия оказались недостаточно эффективными. По этой же причине одновременно с лечением инвазированных нужно сделать все возможное для того, чтобы очистить помещения от возбудителей.
В течение многих лет для лечения аскаридоза и энтеробиоза во всем мире применяется пирантел, завоевавший популярность среди врачей-педиатров и пациентов. Согласно рекомендациям, разработанным в США (Medical Letter, 2002), пирантел считается препаратом первой линии для лечения энтеробиоза у детей и взрослых.
Антигельминтное действие пирантела памоата связано со стимулирующим влиянием на Н-холинорецепторы ганглионарных синапсов гельминтов, приводящим к спастическому параличу и последующему изгнанию их из организма человека. Клинические испытания эффективности и переносимости пирантела показали его высокую лекарственную активность при энтеробиозе и аскаридозе — 94—100%, а также хорошую переносимость [1, 3].
Пирантел для лечения энтеробиоза назначают из расчета 10 мг/кг в сутки однократно во время или после еды. Для лечения аскаридоза пирантел назначается в дозе 5 мг/кг однократно. Препарат хорошо переносится детьми, в отдельных случаях могут развиться тошнота, рвота, понос, боли в животе, очень редко возникают транзиторное повышение активности печеночных трансаминаз, головная боль, головокружение, нарушения сна. Пирантел противопоказан детям с болезнями печени.
Мы имеем большой опыт лечения энтеробиоза у детей препаратом пирантел (таблетки, суспензия). Пирантел хорошо известен на мировом рынке антигельминтных препаратов и широко применяется для лечения энтеробиоза в России многими поколениями врачей. По нашему мнению, этот препарат имеет ряд преимуществ по сравнению с другими антигельминтными средствами. Во-первых, препарат в форме суспензии легко давать детям, во-вторых, пирантел имеет приятный персиковый вкус, вследствие чего, во время лечения у ребенка не возникает отрицательных эмоций, и, наконец, в-третьих — пирантел обладает приемлемой ценой и широко продается в аптеках. Флакон снабжен мерной ложечкой со шкалой деления 2,5 и 5,0 мл, что позволяет легко дозировать препарат в зависимости от массы тела инвазированного ребенка (или взрослого). Пирантел-суспензия может применяться у детей уже с 6-месячного возраста.
Наряду с пирантелом, хорошим антигельминтным действием при энтеробиозе и аскаридозе обладают мебендазол и медамин.
Мебендазол (вермокс) для лечения энтеробиоза детям 2–5 лет назначается из расчета 5 мг/кг в сутки, старше 5 лет — 100 мг в сутки. Для лечения аскаридоза детям 2–5 лет препарат назначают из расчета 5 мг/кг в 2 приема в сутки в течение 3 сут, детям старше 5 лет мебендазол назначается в дозе 10 мг/кг в сутки в 2 приема в течение 3 сут.
Мебендазол не рекомендуется применять в первом триместре беременности. Необходимо помнить, что препарат противопоказан детям до 2 лет. К побочным действиям мебендазола относятся боли в животе, жидкий стул.
Медамин (2-медоксикарбаниламино-бензимидазол) по химическому строению и спектру антигельминтного действия близок к мебендазолу. Для лечения энтеробиоза он назначается в дозе 10 мг/кг в сутки в 2-3 приема (возможен и одномоментный прием) после приема небольшого количества пищи, таблетки рекомендуется разжевать и запить водой. Для лечения аскаридоза медамин назначают в тех же дозах в течение 3 дней.
К побочным действиям медамина относятся тошнота, слабость. При аллергических проявлениях препарат отменяют. Медамин противопоказан в первом триместре беременности.
Для восстановления микробиоценоза толстой кишки у больных кишечными нематодозами, в том числе энтеробиозом и аскаридозом, и повышения эффективности специфической терапии рекомендуется назначение бификола, молочного бифидум-бактерина. Давно известны пищевые продукты и лекарственные растения, которые могут применяться для лечения и профилактики энтеробиоза. Хорошее антигельминтное действие оказывают морковь и морковный сок. Также можно использовать антигельминтную активность грецких орехов, лесной земляники, граната (особенно гранатового сока), чеснока и любистока.
Из лекарственных растений применяют зверобой продырявленный в виде отваров и настоев, чая, а также девясил высокий (Inula helenicum). Эффективность фитотерапии энтеробиоза невысока, однако введение в рацион питания пищевых продуктов, обладающих антигельминтным действием, является хорошей мерой профилактики энтеробиоза и усиливает действие назначаемых врачом медикаментозных препаратов.
Критериями эффективности лечения гельминтозов является отрицательный результат контрольного паразитологического исследования проб фекалий (при аскаридозе) и перианального соскоба или отпечатка (при энтеробиозе), а также исчезновение клинических симптомов инвазии.
Профилактика гельминтозов
Особенности профилактики гельминтозов зависят от особенностей их эпидемиологии. При энтеробиозе и аскаридозе единственным источником инвазии является человек. Заражение происходит при заглатывании зрелых инвазионных яиц гельминтов. Однако в остальном эпидемиология этих гельминтозов сильно различается. Яйца остриц созревают в помещениях и на теле человека в течение нескольких часов и сохраняются в среднем до 1 месяца на различных предметах обихода. Яйца аскарид созревают при попадании в почву в течение нескольких месяцев и сохраняются там до 10 лет и больше. Энтеробиоз передается внутри помещений от одного человека к другому в основном через грязные руки, постельное и нательное белье, загрязненные яйцами остриц игрушки, посуду и другие предметы обихода.
Аскаридозом человек заражается при заглатывании частиц почвы, содержащей инвазионные яйца аскарид (с немытыми овощами, зеленью, фруктами). Повышает опасность заражения (в случае аскаридоза) наличие у ребенка такой вредной привычки, как геофагия (пробование или поедание земли, песка, глины), которая встречается довольно часто (у 3—10% детей в возрасте до 7 лет).
Профилактика энтеробиоза и аскаридоза — важнейшая задача медицинских, воспитательных учреждений, родителей. Она может быть решена при одновременном выполнении комплекса мероприятий, основными компонентами которого считаются выявление и лечение зараженных и санитарно-гигиенические меры. Профилактика аскаридоза, энтеробиоза и других гельминтозов в Российской Федерации регламентируется новыми санитарными нормами и правилами, утвержденными Минздравом РФ в 2003 г.
По вопросам литературы обращайтесь в редакцию.
Т. И. Авдюхина, кандидат медицинских наук, доцент
Т. Н. Константинова, кандидат медицинских наук, доцент
М. Н. Прокошева
РМАПО, Москва ДКБ им. П. И. Пичугина, Пермь