Атипичная резекция легкого что это значит
Атипичная резекция легкого что это значит
а) Показания для атипичной торакоскопической резекции легкого:
— Плановые: удаление ограниченных патологических очагов, расположенных на поверхности легкого. Резекция показана после первого рецидива спонтанного пневмоторакса.
— Противопоказания: предшествующая торакальная операция или диффузное заболевание, поражающее все легкое.
— Альтернативные операции: торакотомия с атипичной резекцией/лобэктомией/пульмонэктомией.
б) Предоперационная подготовка:
— Предоперационные исследования: рентгенография органов грудной клетки, компьютерная томография, подумайте об исследовании функции внешнего дыхания.
— Подготовка пациента: начало лечения с дренированием плевральной полости.
в) Специфические риски, информированное согласие пациента:
— Рецидив после удаления буллы или пузыря (менее 10% случаев)
— Кровотечение
— Подкожная эмфизема
— Инфекция (местная, эмпиема, пневмония)
— Повреждение нервов (межреберных, синдром Горнера)
— Может потребоваться переход к торакотомии
г) Обезболивание. Общее обезболивание (интубация).
д) Положение пациента. На боку, рука располагается горизонтально на уровне плеча.
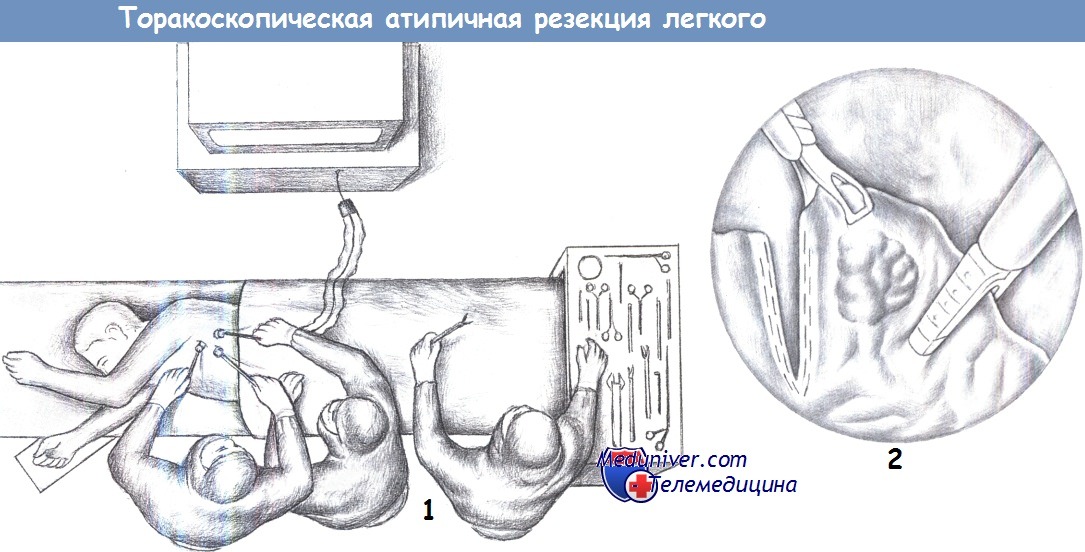
е) Доступ при торакоскопической атипичной резекции легкого. В подмышечном треугольнике, где мышечной ткани меньше: передний край широчайшей мышцы спины в пятом межреберье, под эндоскопическим контролем в седьмом межреберье по средней подмышечной линии, а также в пятом межреберье по заднему краю большой грудной мышцы.
ж) Этапы торакоскопической атипичной резекции легкого:
— Расположение, хирургическая бригада, доступы
— Клиновидное иссечение
— Проверка герметичности
— Дренаж
з) Анатомические особенности, серьезные риски, оперативные приемы:
— Небольшие пузыри можно перевязать у основания эндопетлей и иссечь.
— Плевродез: выскабливание париетальной плевры в области верхней грудной апертуры тупфером (абразионная техника) или аргоновоплазменная коагуляция. Альтернатива: выполнение плеврэктомии.
и) Меры при специфических осложнениях. При наличии выраженного утолщения плеврального покрова, плохом обзоре или кровотечении перейдите к открытой операции.
к) Послеоперационный уход после торакоскопической атипичной резекции легкого:
— Медицинский уход: пережмите плевральные дренажи и удалите их через 2 дня (предварительное условие: отсутствие утечки воздуха).
— Активизация: немедленно.
— Период нетрудоспособности: 2 недели.
л) Оперативная техника торакоскопической атипической резекции легкого:
— Положение пациента, хирургическая бригада, доступы
— Клиновидное иссечение
— Проверка герметичности
— Дренаж
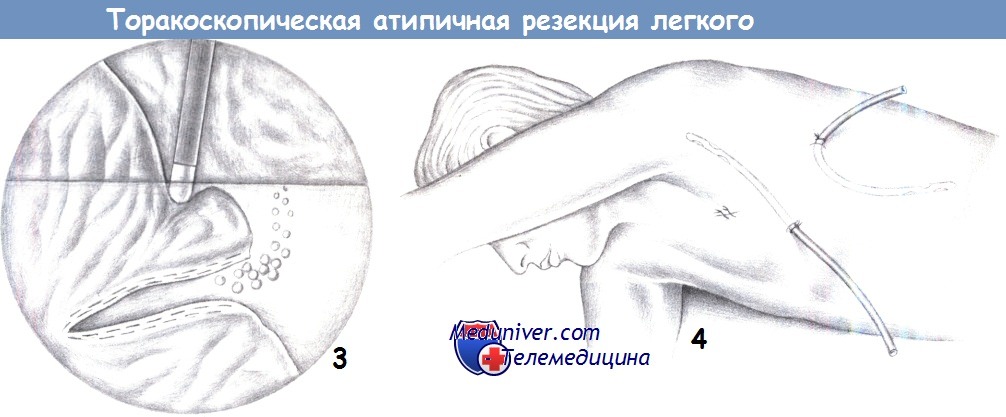
2. Клиновидное иссечение. Поверхностные узелки резецируются сшивающим аппаратом Endo-GIA. Для более глубоких узлов рекомендуется клиновидное иссечение двумя или более кассетами сшивающего аппарата Endo-GIA. Клиновидные иссечения нужно планировать так, чтобы вся иссеченная паренхима могла бы быть герметизирована и ушита аппаратом. Резецированный препарат извлекается в контейнере через место введения троакара.
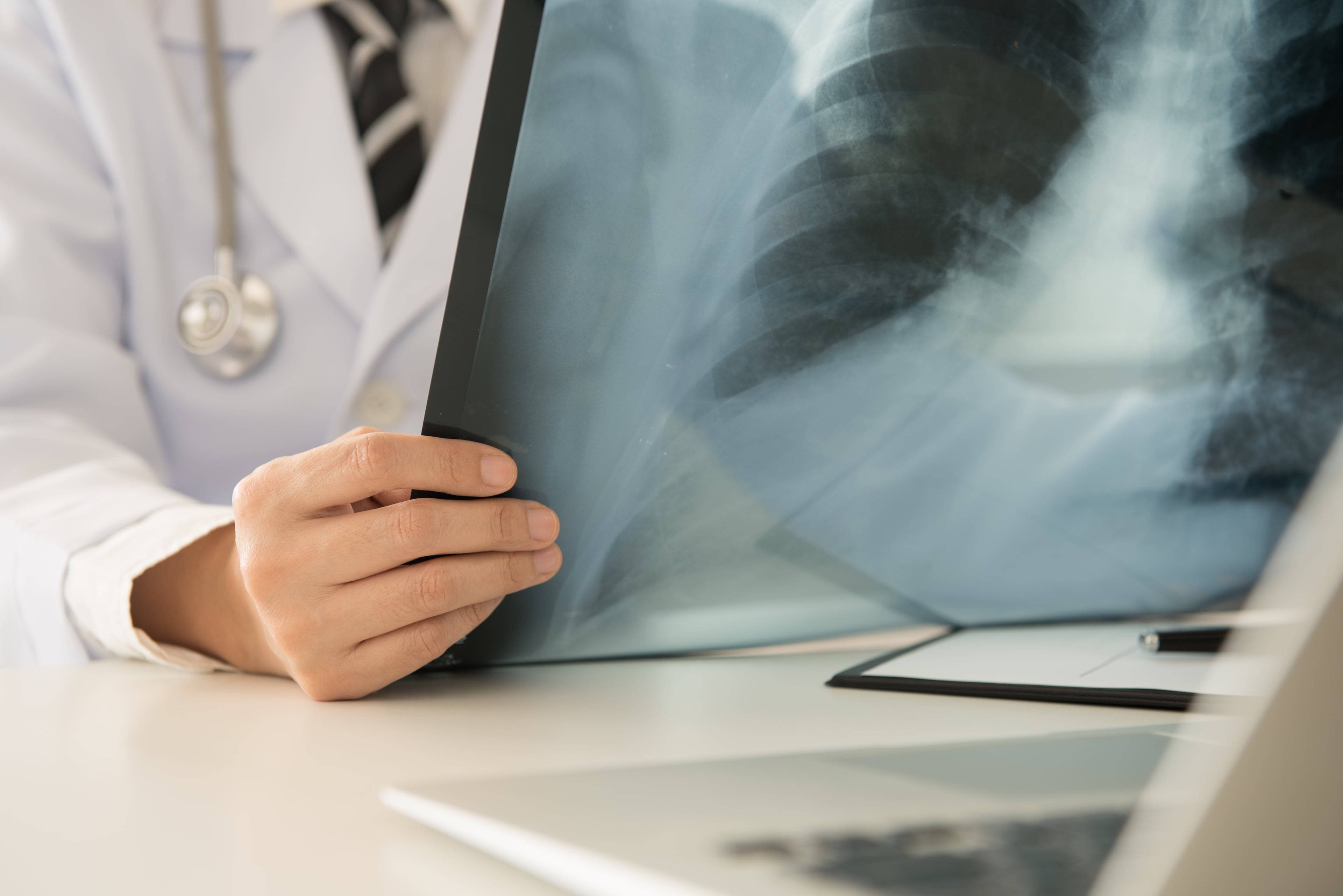
3. Проверка герметичности. Чтобы оценить проникновение воздуха через линию резекции после завершения прошивания аппаратом, рекомендуется проверка герметичности при заполнении плевральной полости водой. Для этого отключенное легкое нужно снова соединить с вентиляционной системой.
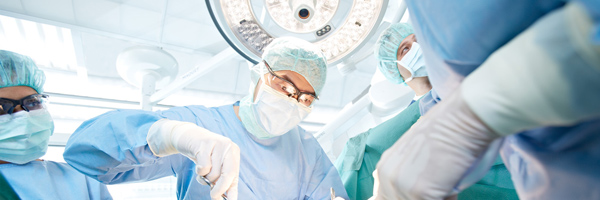
4. Дренаж. После расправления легкого, через места введения троакаров устанавливаются один или два плевральных дренажа.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Атипичная резекция легкого что это значит
а) Показания для атипичной резекции легкого:
— Плановые: метастазы; отграниченные доброкачественные очаговые образования (например, булла при наличии спонтанного пневмоторакса после первого рецидива).
— Относительные показания: злокачественное поражение бронха с внелегочными метастазами или значительно ограниченной функцией легкого.
— Альтернативные операции: торакоскопическое вмешательств!
б) Предоперационная подготовка. Предоперационные исследования: рентгенография органов грудной клетки, функциональные параметры внешнего дыхания компьютерная томография (возможно, с биопсией), бронхоскопия, медиастиноскопия.
в) Специфические риски, информированное согласие пациента:
— Стойкий бронхоплевральный свищ
— Кровотечение
— Инфекция (эмпиема плевры)
— Переломы ребер
г) Обезболивание. Общее обезболивание (интубация): рассмотрите возможность интубации двухпросветной трубкой.
д) Положение пациента. На боку, рука над головой. Предупреждение: опасайтесь повреждения плечевого сплетение
е) Доступ при атипичной резекции легкого. Подмышечная торакотомия.
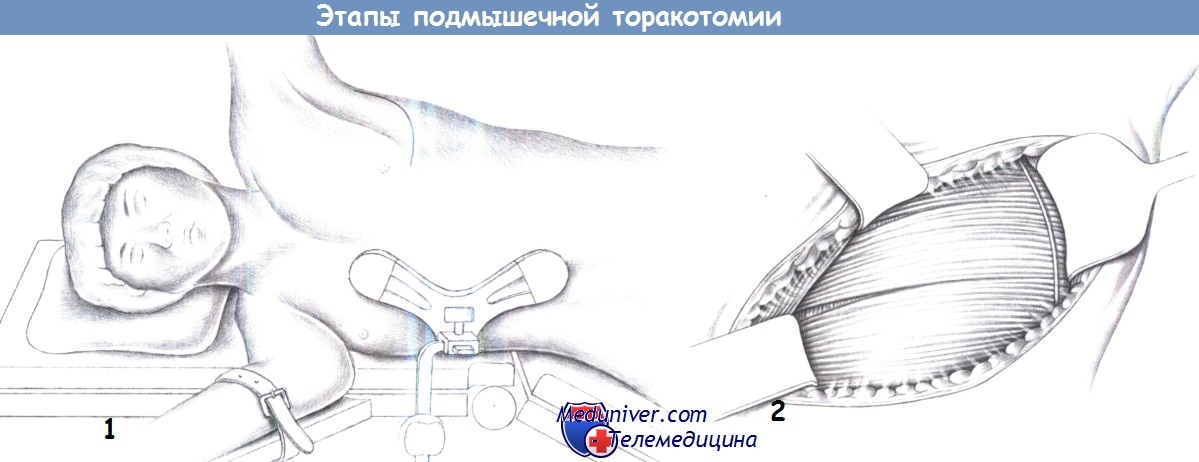
ж) Этапы операции:
— Клиновидное иссечение
— Обшивание зоны иссечения
— Резекция верхушки
— Обшивание зоны иссечения
з) Анатомические особенности, серьезные риски, оперативные приемы:
— Буллы обычно расположены в верхушке легкого или вдоль краев междолевых щелей.
— Используйте сшивающий аппарат со скобками 3,5 мм.
и) Меры при специфических осложнениях. Постоянное поступление воздуха по плевральным дренажам: дренажи с аспирацией при 15-20 см водн. ст.
к) Послеоперационный уход после атипичной резекции легкого:
— Медицинский уход: если при рентгенографии определено, что легкое расправлено, перекройте плевральные дренажи и удалите их после контрольной рентгенографии (обычно через 2-4 дня).
— Активизация: немедленно.
— Период нетрудоспособности: 1-2 недели.
л) Оперативная техника атипичной резекции легкого:
— Клиновидное иссечение
— Обшивание зоны иссечения
— Резекция верхушки
— Обшивание зоны иссечения
1. Клиновидное иссечение. Изолированные периферические узелки в легком могут быть удалены путем атипичной резекции. Использование линейного сшивающего аппарата доказало свою практичность при пережатии и иссечении клиновидных участков легкого, с последующим обшиванием.
2. Обшивание зоны иссечения. По завершении иссечения линия скобочного шва может быть обшита непрерывным швом. Если не использовался сшивающий аппарат, можно также ушить легкое непрерывным швом (2-0 PGA) между зажимами, обеспечивая герметичное закрытие легочной паренхимы.
3. Резекция верхушки. Ограниченные очаговые образования в нижней доле или в верхушечных сегментах (например, пузыри и буллы) можно пережать линейным сшивающим аппаратом соответствующей ширины, резецировать между рядами скобок и ушить.
4. Обшивание зоны иссечения. Линию скобочного шва можно обшить непрерывным швом. Резекция легкого может быть выполнена без сшивающих аппаратов. Для этого область резекции изолируется между зажимами, иссекается, и легкое ушивается непрерывным швом.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Атипичная резекция легкого
Содержание Скрыть
Атипичная (краевая) резекция представляет собой разновидность хирургического вмешательства, которое заключается в иссечении части пораженной анатомической структуры, расположенной за пределами границы органа. Операция назначается в соответствии с определенными показаниями. Чтобы удалить намеченную область, используют технику пришивания участка легкого с последующим его иссечением.
Что такое
Атипичная резекция легкого – это вид оперативного вмешательства, в ходе которого удаляется часть легочной паренхимы, которая располагается на краю границы анатомической структуры. После проведения операции рана подлежит ушиванию. Благодаря такой технике выполнения в большинстве случаев удается сохранить здоровые ткани и нормальную работу органа.
Показания
Даная разновидность хирургической процедуры назначается в том случае, когда благодаря диагностическому обследованию была выявлена опухоль доброкачественного характера.
Кроме того, манипуляция показана в качестве одного из терапевтических методов при обнаружении пневмосклероза ограниченной формы, то есть, когда наблюдается перерождение фибром органа.
Также применяется при ограниченном туберкулезе и диссеминированном патологическом процессе, невыясненной этиологии происхождения.
Противопоказания
Среди общих ограничений специалисты выделяют дыхательную недостаточность и выраженное нарушение функционирования сердечно-сосудистого аппарата в необратимой форме. Однако стоит отметить, что противопоказания, связанные с работой сердца и сосудистой системы, до сих пор остаются спорным моментом.
В некоторых случаях отмечается возможность удаления легкого у больного с явными признаками изменений миокарда, что не приводит к существенным рискам для здоровья и жизни пациента.
Именно по этой причине специалистам рекомендуется принимать во внимание индивидуальные особенности сердечной мышцы при проведении комплекса диагностических методов с целью оценки состояния сердца.
Среди абсолютных противопоказаний выделяют декомпенсацию сердечно-сосудистой деятельности, которая находится на выраженной стадии и не корректируется при помощи применения медикаментозных препаратов.
Также оперативное вмешательство может быть противопоказано при гипертензии малого круга кровообращения.
Также с особым вниманием нужно оценивать риски от операции при выявлении печеночной и почечной недостаточности.
Кроме того, атипичная резекция не проводится при диффузном поражении всего легкого.
Подготовка
После того как будет поставлен окончательный диагноз и назначена дата проведения операции по удалению части легочной паренхимы, пациент должен выполнить ряд рекомендаций, которые дает врач для того, чтобы все манипуляции прошли максимально успешно.
Прежде всего больной проходит диагностическое обследование, которое включает компьютерную томографию, рентгенографию грудной клетки, медиастиноскопию, бронхоскопию, а также тест на определение функциональных параметров внешнего дыхания.
Кроме того, важной составляющей на подготовительном этапе является и нормализация психологического состояния человека. Чтобы предотвратить нервный срыв и снизить вероятность развития шока после операции, проводится соответствующее профессиональное вмешательство.
Чтобы в послеоперационный период вероятность появления осложнений была минимальной, назначается терапия лекарственными средствами антибактериальной группы.
Ход операции
Все хирургические манипуляции выполняются под общей анестезией с введением эндотрахеального интубационного наркоза.
Краевая резекция, при которой подразумевается сохранение легкого, без выделения отдельных структур органа и их раздельной обработки. Часть анатомического элемента, который подлежит иссечению, прошивают при помощи специального приспособления и накладывают на него двойной ряд металлических скрепок. После этого пораженный участок удаляется.
В зависимости от стадии течения патологического процесса и объема поврежденной области, может применяться две разновидности доступа к очагу поражения.
Торакотомия
Это вид полостной операции, при которой происходит вскрытие грудной клетки. Для доступа к атипичной ткани специалисты используют хирургический ретрактор, который также позволяет защитить рядом расположенные мягкие ткани от травмирования.
Торакоскопия
Относится к малоинвазивным методикам. При его применении не требуется вскрытия грудины. Весь ход процедуры осуществляется с эндоскопом, который позволяет вывести картину происходящего на монитор в многократном увеличении.
Мы делаем медицинскую информацию понятной, доступной и актуальной.
Такая тактика целесообразна при незначительных поражениях легкого.
В случае необходимости в прооперированную полость может вставляться дренаж.
Осложнения
К наиболее распространенным осложнениям, которые могут появиться в процессе хирургического вмешательства или непосредственно в послеоперационный период, относят кровотечение или инфицирование раневой поверхности.
Кроме того, не исключается формирование стойкого бронхоплеврального свища, а также перелом ребер в ходе операции.
Реабилитационный период
Во время восстановления необходимо обеспечить свободную проходимость воздухоносных путей, а также добиться максимально быстрого расправления оставшейся части прооперированного легкого.
После того как рентгенография покажет, что орган полностью расправился, то дренажное приспособление извлекается. Как правило, это происходит на 2-4 сутки после операции. На больного накладывается период нетрудоспособности сроком от одной до двух недель.
Атипичная резекция легкого — это органосохраняющая операция по удалению части пораженной структуры. Процедура имеет свои определенные показания и противопоказания. Поэтому перед решением о ее использовании требуется прохождение ряда диагностических мероприятий.
Лечение I и II стадий немелкоклеточного рака легкого
Для I и II стадий немелкоклеточного рака легкого (НМРЛ) характерно вовлечение в патологический процесс только одного легкого и отсутствие поражения средостения или каких-либо других структур. На раннем этапе выявляется не более 30% всех случаев НМРЛ [1].
Общие принципы терапии
Стадирование рака легкого осуществляется в соответствии с системой TNM. В настоящее время стадию НМРЛ определяют, основываясь на последней, 8-й редакции системы, принятой в 2016 году [1].
Таблица 1. Стадирование рака легкого по системе TNM 8 пересмотра [2].
| Стадия заболевания | ТХ | N0 | М0 |
|---|---|---|---|
| Стадия IA1 | T1a(mi) | N0 | M0 |
| T1a | N0 | M0 | |
| Стадия IA2 | T1b | N0 | M0 |
| Стадия IA3 | T1c | N0 | M0 |
| Стадия IB | T2a | N0 | M0 |
| Стадия IIA | T2b | N0 | M0 |
| Стадия IIB | T1a-c | N1 | M0 |
| T2a | N1 | M0 | |
| T2b | N1 | M0 | |
| T3 | N0 | M0 |
* T1a(mi) – минимально инвазивная карцинома.
Основным методом лечения I и II стадий НМРЛ является полная хирургическая резекция опухоли при отсутствии противопоказаний к операции. Для пациентов со II стадией НМРЛ показана адъювантная химиотерапия. Ее также может быть целесообразно назначать при стадии IB, особенно с признаками высокого риска. Пациентам с опухолями стадии IA после резекции адъювантная химиотерапия не показана [3].
Послеоперационная лучевая терапия показана только пациентам I и II стадии, у которых обнаружено опухолевое поражение в области резекции [4].
Лучевая терапия – альтернатива для пациентов, не являющихся кандидатами на хирургическое лечение вследствие сопутствующих заболеваний или отказа от операции [5]. Стереотаксической радиотерапии отдается предпочтение при опухолях с размерами менее 5 см. Обычное фракционирование показано пациентам с более массивными поражениями или при недоступности стереотаксической радиотерапии.
Алгоритм лечения потенциально резектабельного НМРЛ
Хирургическое лечение НМРЛ
Хирургическая лечение – стандартный подход при НМРЛ I и II стадии, а также в случае отсутствия доказательств вовлечения средостения до хирургической резекции.
Анатомическая резекция – лобэктомия
Процедурой выбора считается хирургическая резекция одной доли легкого, лобэктомия, имеющая важное преимущество по сравнению с пневмонэктомией в случаях, когда поражение может быть резецировано полностью, – способность сохранять легочную функцию [6]. При этом альтернативой открытой торакотомии считается видеоторакоскопия [7], обеспечивающая снижение инвазивности лечения ранней стадии НМРЛ.
Применение видеоторакоскопии позволяет снизить последствия хирургического вмешательства, в том числе уменьшить выраженность послеоперационного болевого синдрома, что особенно важно для пациентов с тяжелой сопутствующей патологией [8]. Кроме того, благоприятная переносимость видеоторакоскопии может увеличить комплайенс постоперационной адъювантной химиотерапии. Так, анализ данных 100 пациентов с НМРЛ после лобэктомии и последующей адъювантной химиотерапии показал, что при проведении вмешательства с помощью видеоторакоскопии гораздо реже приходилось откладывать назначение химиотерапии (18% против 58%) и снижать ее дозу (26% против 49%) по сравнению с открытой торакотомией [9].
Несмотря на то, что эффективность видеоторакоскопии по сравнению с обычными хирургическими методами не была подтверждена в рандомизированных исследованиях, ретроспективные данные позволяют сделать вывод о безопасности и эффективности лобэктомии с помощью видеоторакоскопии для пациентов с I стадией НМРЛ без ущерба для выживаемости 10.
Ограниченная (сублобарная) резекция может подразумевать анатомическую или неанатомическую сегментэктомию с удалением первичной опухоли, внутрилегочных, прикорневых и медиастинальных лимфатических узлов. Сублобарная резекция может быть терапией выбора для пациентов, которые не в состоянии перенести удаление всей доли легкого вследствие снижения функции легких, преклонного возраста или тяжелой сопутствующей патологии.
Результаты ряда исследований свидетельствуют, что сублобарная резекция связана с худшими показателями выживаемости по сравнению с лобэктомией [6,14]. По различным данным, при неанатомической резекции увеличивается частота местного рецидива на 5-10% [15]. Предложенная в качестве способа уменьшения частоты локального рецидива при сублобарной резекции интраоперационная брахитерапия, к сожалению, оказалась неэффективной, что подтверждено данными клинического исследования III фазы ALLIANCE [16], свидетельствующими об отсутствии существенной разницы между сублобарной резекцией с и без сочетания с интраоперационной брахитерапией.
Однако существует и противоположная точка зрения, утверждающая, что эффективность сублобарной резекции на ранних стадиях НМРЛ, особенно при размере поражения не более 2 см, может быть сравнима с результатом, полученным после лобэктомии [17].
Согласно рекомендациям Европейского общества торакальных хирургов 2006 года, целесообразно проводить систематическое удаление лимфоузлов во всех случаях с целью обеспечения полноты резекции [18]. Такая же тактика декларируется и в рекомендациях Британского торакального общества 2010 года [19].
Согласно федеральным российским рекомендациям, стандартным объемом медиастинальной лимфаденэктомии при операциях на правом легком считается удаление правых нижних паратрахеальных (трахеобронхиальных, паратрахеальных, претрахеальных) узлов, на левом легком – парааортальных, субаортальных, левых нижних паратрахеальных узлов, а также независимо от стороны операции – бифуркационных, параэзофагеальных и узлов легочной связки соответствующих сторон [15].
Согласно рекомендациям Европейского общества торакальных хирургов ESTS [20], у пациентов с минимальным получением образцов тканей лимфоузлов, независимо от местоположения первичной опухоли, необходимо исследовать следующие уровни лимфоузлов и удаленные узлы, при наличии таковых:
У пациентов с систематической радикальной средостеночной лимфаденэктомией вся доступная средостеночная жировая ткань, относящаяся к одной стороне тела, подлежит удалению, включая следующие уровни:
Пациенты, у которых не все упомянутые уровни лимфоузлов были удалены, автоматически классифицируются как имеющие «минимальное получение образцов ткани лимфоузлов».
При метастатическом поражении лимфоузлов средостения показана расширенная медиастинальная лимфаденэктомия, подразумевающая удаление превенозных, ретротрахеальных и верхних паратрахеальных узлов с окружающей клетчаткой соответствующей стороны [15].
При микроскопическом вовлечении опухолевых клеток по линии резекции (R1) прогноз заболевания значительно менее благоприятный по сравнению с резекцией с отрицательными микроскопическими полями (R0) [21,22].
Для пациентов со стадией IIB вследствие вовлечения в опухолевый процесс грудной стенки может быть показана резекция грудной стенки в едином блоке с опухолью и тканью легкого («en-bloc»). По данным ретроспективного исследования с участием 212 пациентов, это позволило достичь высоких показателей выживаемости в течение пяти лет [23].
Частота локального рецидива после хирургического вмешательства у пациентов с НМРЛ I и II стадии составляет, по разным данным, от 6% до 55% [24,25].
Адъювантная терапия
После потенциально радикальной резекции опухоли при НМРЛ существует вероятность прогрессирования заболевания вследствие отдаленного метастазирования или местного рецидива. Адъювантная химиотерапия после радикальных операций у некоторых больных на ранних стадиях заболевания (IB и II) позволяет улучшить безрецидивную и общую 5-летнюю выживаемость.
Клинические исследования, в которых в качестве адъювантной химиотерапии применялись современные схемы на основе цисплатина, продемонстрировали преимущество в выживаемости для пациентов с НМРЛ II стадии и, возможно, со стадией IB [26], но не подтвердили эффективность у пациентов со стадией IA [27].
Адъювантную терапию назначают после восстановления пациента от хирургического лечения (но не позже 8 недель), ее длительность в среднем составляет 3-4 цикла. Для химиотерапии можно использовать любые платиносодержащие комбинации с включением препаратов 3 поколения или этопозида. Наиболее изученными считаются комбинации винорельбина и цисплатина, гемцитабина и цисплатина, паклитаксела и карбоплатина [15].
Определенных рекомендаций по назначению таргетных препаратов в качестве адъювантной терапии на сегодня не существует. Данные ряда исследований свидетельствуют, что у пациентов с мутацией EGFR на ранней стадии заболевания (особенно на стадии IIIA после резекции опухоли) назначение в качестве адъювантного лечения эрлотиниба сопряжено с увеличением выживаемости без рецидива [26, 28]. Однако неизвестно, свидетельствуют ли эти результаты об улучшении общей выживаемости или о пролонгировании времени до рецидива.
В то же время в работе Kelly K с соавт. с участием 973 пациентов с НМРЛ и мутацией в гене EGFR [29] было показано, что адъювантная химиотерапия эрлотинибом не пролонгирует выживаемость без рецидива. Столь противоречивые данные свидетельствуют о необходимости дальнейших исследований эффективности ингибиторов тирозинкиназы в качестве адъювантной химиотерапии у EGFR-позитивных пациентов с НМРЛ.
Прогноз НМРЛ I и II стадии
У пациентов со стадией I и II НМРЛ на прогноз заболевания влияет ряд факторов, среди которых:
Постоперационное наблюдение
Целью постоперационного наблюдения после первичного лечения НМРЛ является раннее обнаружение рецидива или второго первичного рака легкого.
Физический осмотр, КТ грудной клетки рекомендовано проводить каждые 6 месяцев на протяжении первых двух лет после лечения, а затем – ежегодно [41]. Однако на конгрессе Европейского общества медицинской онкологии ESMO 2017 года в Мадриде были представлены результаты исследования с участием 1775 пациентов с полностью резецированным НМРЛ I-II-IIIA стадии, продемонстрировавшие отсутствие разницы в общей выживаемости между пациентами, проходящими КТ-сканирование каждые 6 месяцев в первые два года после операции, и пациентами, не делающими этого исследования.
Тем не менее, наблюдение на основе КТ по-прежнему остается оптимальным способом контроля из-за возможного развития повторного случая первичного рака у пациентов после полной резекции НМРЛ.