Атрофия легких что такое
Атрофический бронхит
Атрофический бронхит — это хроническая патология, которая сопровождается воспалительным процессом в бронхах и дистрофически-склеротическими изменениями слизистой оболочки.
Что такое атрофический бронхит?
Это одна из хронических форм бронхита, которая очень распространена в странах с развитой промышленностью. При этой патологии изменяется структура эпителия бронхов, а слизистая оболочка становится более тонкой.
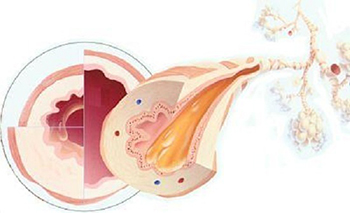
По причине появления бронхиты подразделяются на:
По локализации воспалительного процесса бронхит может быть:
По характеру воспаления:
По фазе обострения:
Непосредственно атрофический бронхит подразделяется на:
Односторонний процесс диагностируется реже, чем двусторонний, а его клинические проявления выражены не так сильно.
Причины возникновения
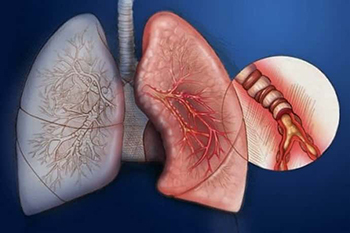
Также внутренними причинами является наследственная предрасположенность, наличие аллергий.
Бронхи истощаются на фоне следующих заболеваний:
Симптомы и признаки
Двусторонний атрофический бронхит сопровождается приступообразным сухим кашлем, который усиливается после контакта с резкими запахами, приемом пищи, вдыхания холодного воздуха, психоэмоционального напряжения.
Кашель длительный, обострения сменяются периодами ремиссии.
Некоторые пациенты жалуются на боль в грудине, особенно при глубоком вдохе, одышку, иногда может наблюдаться кровохаркание.
Кашель более выражен ночью и в утренние часы. Температура тела в стадии обострения может подниматься до 38 °С. Присутствует утомляемость. В периоды ремиссии кашель становится редким — по утрам.
Диагностика
Диагностика атрофического бронхита заключается в следующем:
Какой врач лечит?
Лечением атрофического бронхита занимается пульмонолог. Его можно найти в Клинике Здоровья на Курской. Находясь в стенах клиники, пациент может пройти полное обследование и сразу же проконсультироваться со специалистом, то есть начать лечение максимально быстро.
Методы лечения
Лечение первично-дистрофического атрофического бронхита заключается в устранении контакта с провоцирующим фактором. Также пациенту назначаются антигистаминные препараты, муколитики, бронходилататоры, поливитамины. При воспалительном процессе назначают антибактериальную терапию.
Результаты
При своевременном обращении к врачу и правильном лечении прогноз благоприятный.
Реабилитация и восстановление образа жизни
В восстановительный период назначаются ингаляции с лекарственными маслами и веществами, которые оказывают противовоспалительное, антисептическое и отхаркивающее действие.
Также показана физиотерапия — УВЧ-терапия, лазеротерапия, ультрафиолет, электрофорез, парафиновые аппликации, озокерит на грудь, кислородные и хвойные ванны.
Образ жизни при атрофическом бронхите
Атрофический бронхит склонен прогрессировать. Если вовремя не оказывается лечение, возможно развитие осложнений — пневмоторакс, эмфизема, легочная гипертензия, хроническая дыхательная недостаточность.
Известно, что наряду с возрастным уменьшением дыхательного объема происходит возрастное уменьшение напряжения кислорода в артериальной крови. Возрастное понижение напряжения кислорода кажется неожиданным с позиций представлений о ее газовом гомеостазисе и о наибольшей заботе организма о поддержании постоянства содержания именно кислорода, недостаток которого лимитирует окислительные реакции значительно сильнее, чем их лимитирует неадекватное удаление углекислого газа, а отсутствие кислорода вызывает гибель человека уже через несколько минут.
Однако, по мере старения человека снижается не только напряжение кислорода, но и количество эритроцитов и общий гемоглобин, создавая условия для развития гипоксии тканей у сгариков. Не исключено, что между процессом возрастного снижения интенсивности обмена веществ и процессом возрастного уменьшения дыхательного объема и альвеолярной вентиляции существуют более сложные отношения, чем простое адекватное отслеживание понижения интенсивности обмена уменьшением величины альвеолярной вентиляции. Изложенные ранее данные позволяют говорить о наличии снижения дыхательного объема и альвеолярной вентиляции независимо от снижения интенсивности обмена веществ.
С рождением человека начинается процесс «старения» коллагена в некоторых тканях организма ребенка. С прекращением роста человеческого организма прекращается растягивающее воздействие на подавляющее большинство органов и тканей. И теперь скорость обновления коллагена начинает постепенно уменьшаться во всех органах и тканях организма, начинается повсеместное «старение» коллагена. Жесткость коллагена во всех структурах, в состав которых входит соединительная ткань, увеличивается. Скорость «старения» коллагена в разных органах и тканях у разных людей после остановки роста организма будет определяться индивидуальными особенностями образа жизни конкретного человека. Она будет различаться не только между разными людьми, но и между разными тканями в организме одного и того же человека. Так, у пианиста, скрипача и т.п. скорость «старения» коллагена мелких суставов кистей рук будет минимальна или может вообще отсутствовать. Однако, скорость старения коллагена внутренних органов и всего остального организма у них может быть в среднем такой же, как у большинства людей. Она будет определяться цепью усиливающих друг друга процессов, в которых вызываемое атрофией легких уменьшение напряжения кислорода в артериальной крови может играть существенную роль.
Фиброз легких: симптомы, лечение и профилактика
Фиброз легких — это процесс образования в легких фиброзной (рубцовой) ткани, что приводит к нарушениям дыхательной функции.
Зиновенкова Елена Алексеевна
Заведующая отделением профпатологии, врач общей практики (семейный врач), врач-терапевт, врач-пульмонолог
Фиброз легких — это процесс образования в легких фиброзной (рубцовой) ткани, что приводит к нарушениям дыхательной функции. При фиброзе снижается эластичность и растяжимость легочной ткани, затрудняется прохождение кислорода и углекислого газа через стенку альвеол (легочных пузырьков, в которых происходит контакт вдыхаемого воздуха с кровью).
Причины заболевания
Фиброз легкого может возникнуть вследствие развития воспаления на альвеолах интерстициальных легочных тканей. В результате это становится причиной образования рубцов и дальнейшего разрастания тканей.
К основным причинам образования можно отнести:
• Наследственный фактор – первая и основная причина
• Курение
• Пребывание в загрязненной местности или в промышленном районе, на вредном производстве
• Осложнение таких заболеваний, как сахарный диабет, красная системная волчанка, ревматоидный артрит
• Осложнение заболеваний легких – такие как альвеолит, саркоидоз, асбестоз, туберкулез
• Длительное вдыхание частиц органических веществ или минералов
• Интоксикация химическими веществами
• Радиоактивное излучение на участке грудной клетки
Виды легочного фиброза
• Идиопатический легочный фиброз – когда определить болезнь, которая его вызвала, невозможно
• Интерстициальный легочный фиброз – когда причину заболевания можно обнаружить
Формы
Фиброз может быть односторонним и двусторонним, очаговым (поражается небольшой участок легкого) и тотальным (распространяется на все легкое).
• фиброз (пневмофиброз) – умеренное тяжистое разрастание соединительной ткани, чередующееся с неизмененной легочной тканью;
• склероз (пневмосклероз) – грубое замещение участков легочной ткани соединительной с уплотнением легких;
• цирроз легких – полное замещение легочной ткани соединительной с повреждением бронхов и сосудов легкого.
По причине развития выделяют:
• фиброз как следствие пылевых заболеваний легких (силикоз — профессиональное заболевание легких, развивающееся после длительного вдыхания пыли силикатов; асбестоз — профессиональное заболевание легких, возникающее после длительного вдыхания пыли асбеста);
• лекарственный фиброз (развивается на фоне длительного приема препаратов для лечения аритмии, химиотерапевтических препаратов (для лечения опухолей));
• фиброз при заболеваниях соединительной ткани (ревматоидном артрите, системной склеродермии, системной красной волчанке);
• фиброз инфекционной природы (после пневмонии или туберкулеза легких);
• идиопатический (первичный) фиброз (возникает без видимой причины).
Симптомы фиброза легких
• Ведущим симптомом является одышка – сначала при физической нагрузке, а по мере прогрессирования заболевания и в покое.
• Кашель (сухой или с отделением небольшого количества мокроты).
• Бледность, цианоз (синюшность) кожных покровов.
• При длительном течении процесса – изменение формы пальцев (утолщение пальцев, выпуклость ногтевой пластины).
• При длительном течении процесса и большом объеме поражения развиваются признаки сердечной недостаточности (так называемого «легочного сердца»): усиление одышки, сердцебиение, отеки на ногах, набухание и пульсация шейных вен, загрудинные боли.
• Слабость, повышенная утомляемость, неспособность выполнять тяжелую физическую нагрузку.
Лечение заболевания
Специфического эффективного лечения фиброза легких нет. Среди основных рекомендаций выделяют следующие:
• исключить воздействие повреждающих факторов (профессиональные вредности);
• ограниченные участки пневмосклероза, не проявляющие себя клинически, в терапии не нуждаются;
• кислородотерапия (ингаляции кислорода с помощью специальных аппаратов);
• оперативное лечение: возможно удаление функционально неполноценного ограниченного очага, в случае тотального фиброза (распространяющегося на все легкое) – пересадка легких.
Сегодня в области медицины проводятся различные разработки препаратов, которые способствуют уменьшению таких рубцов. Также некоторые из них при различных типах фиброза способны уменьшать процессы, способствующие рубцеванию ткани. К таким препаратам относят кортикостероиды, которые могут подавить иммунную систему. В случае подавления иммунной системы уменьшается воспаление легких и последующее рубцевание ткани в легких. Кроме этого, прием кортикостероидов может вестись в комплексе с противовоспалительными и другими препаратами.
Осложнения и последствия
• Хроническая дыхательная недостаточность (недостаточность кислорода организму).
• Легочная гипертензия.
• Хроническое легочное сердце.
• Присоединение вторичной инфекции (с развитием пневмонии).
Профилактика фиброза легкого
• Использование средств индивидуальной защиты при работе с профессиональными вредностями, соблюдение правил техники безопасности.
• Своевременное лечение воспалительных заболеваний легких (пневмонии; туберкулеза).
• Отказ от курения.
• При приеме препаратов, способных привести к развитию фиброза легких (некоторые антиаритмические препараты), – периодический профилактический контроль за состоянием легких.
Врач общей практики (семейный врач), врач-терапевт Зиновенкова Елена Алексеевна
Атрофический бронхит
Атрофический бронхит – это морфологическая разновидность хронического бронхита, характеризующаяся структурной перестройкой покровного эпителия и истончением слизистой оболочки бронхов. Клиника атрофического бронхита включает в себя сухой кашель (длительный, рецидивирующий или постоянный), дискомфорт и боль при глубоком дыхании, одышку, эпизоды кровохарканья. Диагностика основывается на данных эндоскопического исследования и морфологии бронхобиоптатов; также проводится рентгенография легких, спирография, анализ мокроты и промывных вод бронхов. Терапевтические мероприятия при обострении симптоматики могут включать лечебные бронхоскопии, ингаляции, физиотерапию.
МКБ-10
Общие сведения
Причины
Общепризнанно, что к структурным изменениям слизистой бронхов приводят такие факторы внешней среды, как запыленность и загрязнение атмосферного воздуха, никотиновая зависимость, профессиональные вредности (контакт с пылью, газами, химическими веществами, пневмокониозы и пр.). Среди эндогенных причин следует отметить наследственно-конституциональные особенности и гормональную дисфункцию. Именно эндогенные механизмы, по мнению исследователей, объясняют тот факт, что атрофический бронхит нередко сочетается с аналогичным поражением слизистых оболочек полости рта и ЖКТ (атрофическим гингивитом, атрофическим гастритом).
К возникновению и прогрессированию атрофических процессов в бронхиальном дереве могут приводить местные воспалительные заболевания: хронический необструктивный и обструктивный бронхит, бронхоэктатическая болезнь, хроническая пневмония, повторные ОРВИ и др. Примерно у трети пациентов с атрофическим бронхитом обнаруживается повышенная чувствительность к пылевым, пыльцевым, бытовым и другим аэрогенным аллергенам.
Патогенез
С учетом морфо- и патогенеза склеротического процесса в слизистой оболочке бронхов различают первично-дистрофическую и первично-воспалительную форму атрофического бронхита. Первично-дистрофическая бронхопатия развивается на фоне отсутствия легочного анамнеза, как следствие регенераторно-пластической недостаточности. Это состояние характеризуется сокращением или прекращением синтеза клеточных белков под действием повреждающих эндо- и экзогенных факторов, что приводит к дистрофическим изменениям в клетках и невозможности выполнения ими своих функций. Первично-воспалительная форма атрофического бронхита возникает у пациентов с длительным предшествующим течением ХНЗЛ. При этом структурная перестройка стенки бронхов развивается постепенно (от катаральных, к катарально-склеротическим и затем к склеротическим изменениям), а уровень метаболических реакций бронхиального эпителия остается высоким.
Симптомы атрофического бронхита
Больные с первично-дистрофической формой атрофического бронхита отмечают связь появления симптомов с вирусной инфекцией, психоэмоциональными нагрузками, контактом с производственными поллютантами, возобновлением курения и др. Наиболее типична жалоба на сухой ирритативный кашель, который может сохраняться длительное время, носить рецидивирующий или постоянный характер. Приступообразное возникновение или усиление кашля может спровоцировать разговор, холодный воздух, прием пищи, эмоциональное напряжение, что отражает изменение чувствительности слизистой оболочки бронхов к действию рядовых неспецифических факторов. Часть больных атрофическим бронхитом отмечает дискомфортные ощущения и даже боль в грудной клетке при глубоком вдохе, однократные или повторные эпизоды кровохарканья.
В случае первично-воспалительного атрофического бронхита симптоматика появляется в связи с обострением основного бронхолегочного процесса. В острой стадии наблюдается гипертермия, влажный кашель, одышка. Вне обострения симптомов может не быть; иногда сохраняется небольшой кашель, обычно по утрам. Данная форма имеет прогрессирующее течение и, как правило, приводит к развитию хронической дыхательной недостаточности, диффузного пневмосклероза, эмфиземы легких и легочной гипертензии.
Диагностика
Стандартная диагностика (физикальная, рентгенологическая, лабораторная) при атрофическом бронхите обязательно должна быть дополнена проведением эндоскопии и исследованием бронхобиоптатов. Объективные данные неспецифичны: аускультативная картина отличается разнообразием – от везикулярного дыхания до сухих или влажных хрипов, при эмфизематозных изменениях над легкими перкуторно определяется коробочный звук. Рентгенография легких зачастую не выявляет отклонений от нормы; в некоторых случаях обнаруживаются признаки деформирующего бронхита и диффузной эмфиземы. По результатам спирометрии могут определяться вентиляционные нарушения по рестриктивному, обструктивному или смешанному типу.
Подтвердить диагноз атрофического бронхита возможно только после проведения бронхоскопии с биопсией. Эндоскопически визуализируется истончение и бледность слизистой оболочки бронхов, ее мелкая складчатость, усиление сосудистого рисунка, легкая кровоточивость при контакте, запустевание и зияние устьев бронхиальных желез. При морфологическом исследовании биоптата бронхов определяются признаки дистрофии эпителия, резкое снижение высоты эпителиального пласта, плоскоклеточная метаплазия покровного эпителия. Анализ бронхоальвеолярного секрета при атрофическом бронхите характеризуется снижением количества нейтрофильных гранулоцитов и макрофагов, а также низким уровнем провоспалительной и антиоксидантной активности жидкости, полученной в ходе бронхоальвеолярного лаважа.
Лечение атрофического бронхита
Терапия первично-дистрофической формы атрофического бронхита начинается с выявления и устранения фактора риска (прекращения контакта с производственными вредностями, элиминации аллергена, коррекции гормональной дисфункции и пр.). Медикаментозная терапия включает назначение поливитаминов, бронходилататоров, антигистаминных и гемореологических средств. При первично-воспалительном атрофическом бронхите в периоды обострения основного заболевания проводятся санационные бронхоскопии с антисептиками, антибактериальная терапия. В дополнение к фармакотерапии назначаются лекарственные, масляные ингаляции, спелеотерапия, физиотерапевтические процедуры (лазеротерапия, ультрафиолетовое облучение, УВЧ-терапия, ультразвуковая терапия).
Профилактика
Эмфизема легких
Эмфизема легких (ЭЛ) занимает одно из ведущих мест среди заболеваний органов дыхания как по распространенности, так и по тяжести проявлений. Заболеваемость ЭЛ постоянно возрастает, особенно у лиц пожилого возраста.
Эмфизема легких (ЭЛ) занимает одно из ведущих мест среди заболеваний органов дыхания как по распространенности, так и по тяжести проявлений. Заболеваемость ЭЛ постоянно возрастает, особенно у лиц пожилого возраста. На аутопсии эмфизема выявляется более чем у 60% пациентов, умерших после 60 лет, в то время как клиницисты ставят этот диагноз менее чем в 20% случаев [23]. Значительная распространенность этого заболевания, прогрессирующее течение, временная нетрудоспособность и ранняя инвалидизация больных из-за развития дыхательной недостаточности и легочного сердца наносят значительный экономический ущерб.
Определение
Эмфизема легких — это анатомическая альтерация легких, характеризующаяся патологическим расширением воздушных пространств, расположенных дистальнее терминальных бронхиол, и сопровождающаяся деструктивными изменениями альвеолярных стенок. В соответствии с этим определением обязательным признаком ЭЛ считается не только расширение, но и деструкция респираторных отделов легких, причем термин «деструкция» должен пониматься не только как разрушение, но и как нарушение нормальной структуры. Такое определение ЭЛ (с морфологических позиций) позволяет отличать ее от различных форм вздутия легких, которые возникают вследствие обратимого нарушения бронхиальной проходимости (приступа бронхиальной астмы); гипервоздушности, появляющейся при интенсивной физической нагрузке, энергичном разговоре, холодовом воздействии на дыхательные пути; от так называемой компенсаторной, или викарной, эмфиземы, а также от интерстициальной эмфиземы, которая представляет собой скопление воздуха в межуточной ткани [5, 18, 23].
ЭЛ наряду с хроническим обструктивным бронхитом и бронхиальной астмой относится к группе хронических обструктивных болезней легких (ХОБЛ). Все эти заболевания сопровождаются нарушением бронхиальной проходимости, с чем и связано некоторое сходство их клинической картины. Однако каждая из форм ХОБЛ имеет свои, специфические особенности, и правильная, своевременная диагностика этих заболеваний позволяет провести целенаправленную профилактику и рациональную терапию.
Этиопатогенез
Эмфизема легких по этиопатогенетическим признакам подразделяется на первичную и вторичную. Первичная ЭЛ развивается без предшествующей бронхолегочной патологии и является самостоятельной нозологической формой. Раньше первичную эмфизему называли идиопатической, эссенциальной, генуинной и т. п., так как причина ее до сих пор остается недостаточно ясной. В последнее время в ее развитии важное значение стали придавать генетическим факторам, в частности дефициту a1-антитрипсина (a1-AT). Вторичная ЭЛ возникает на фоне других заболеваний органов дыхания, в первую очередь хронического обструктивного бронхита. По распространенности поражения выделяют диффузную и локальную формы ЭЛ. Первичная и вторичная ЭЛ, развившаяся на фоне хронического обструктивного бронхита, относится к диффузной форме. Такие причины, как рубцовые изменения в легочной паренхиме и плевре, локальные нарушения бронхиальной проходимости, врожденные изменения легочной ткани, перерастяжение части легкого вследствие сморщивания или оперативного удаления других его частей, приводят к развитию локальных форм эмфиземы легких (иррегулярной, буллезной, околорубцовой). Однако локальные формы ЭЛ далеко не всегда соответствуют приведенному выше морфологическому определению [18].
Генетическим факторам, и в первую очередь дефициту a1-АТ, отводится важная роль в развитии ЭЛ. a1-АТ, относящийся к сывороточным белкам из группы a1-глобулинов, представляет собой гликопротеид с молекулярной массой 50 000-55 000. Он обусловливает примерно 90% всей трипсинингибирующей способности плазмы. a1-антитрипсин является основным ингибитором сериновых протеаз, к которым относятся трипсин, химотрипсин, нейтрофильная эластаза, коллагеназа, тканевой калликреин, плазминоген, фактор Ха. a1-АТ кодируется геном Pi (proteinase inhibitor), расположенным на длинном плече хромосомы 14 [23]. Его количество в сыворотке крови у здорового человека в норме составляет 1,5–3,5 г/л. Уровень сывороточного a1-АТ равен 0,80 г/л (11 mumol/L), что составляет примерно 35% нормального уровня и является тем порогом, ниже которого значительно повышается риск развития эмфиземы легких [42]. Выделено не менее 90 различных генетически детерминированных вариантов a1-АТ [31]. Доказана значительная роль гомозиготных форм наследственного дефицита a1-АТ в развитии первичной диффузной ЭЛ, а также цирроза печени. Эмфизема возникает у таких людей в 15 раз чаще. Роль гетерозиготных форм дефицита a1-АТ в развитии ЭЛ окончательно не установлена. Существует специфика географического и этнического распределения вариантов a1-АТ. Распространенность наследственного дефицита a1-АТ в России существенно ниже, чем в странах Северной Европы, эндемичных по данной патологии [21, 23, 31, 37].
Врожденный дефицит a1-АТ может при определенных условиях привести к избыточному действию ферментов, в том числе эластазы, прижизненному разрушению тончайших межальвеолярных перегородок и слиянию отдельных альвеол в более крупные эмфизематозные полости с постепенным уменьшением общей дыхательной поверхности легких [18]. Главная роль в рассматриваемых процессах принадлежит нейтрофильной эластазе. Одним из главных источников эластазы в организме человека являются нейтрофилы. Косвенное значение имеют также макрофаги. Следует отметить, что врожденный дефицит a1-АТ ведет к развитию ЭЛ преимущественно у взрослых в возрасте 30-40 лет, что, вероятно, связано с провокационными факторами: курением, воздушными поллютантами, неблагоприятными условиями труда [17]. Однако не у всех пациентов с дефицитом a1-АТ развивается эмфизема, особенно если они не подвергались воздействию табачного дыма и поллютантов [28].
Возможно, имеются и другие механизмы развития ЭЛ.
Среди экзогенных факторов в развитии ЭЛ большое значение имеют курение, загрязнение воздуха, легочные инфекции. Особенно агрессивным фактором является курение, от интенсивности и длительности которого зависит тяжесть заболевания. Среди наиболее вероятных компонентов табачного дыма, способствующих развитию ЭЛ, — кадмий, окиси азота и серы. Механизм действия табачного дыма при ЭЛ связан в первую очередь с тем, что его компоненты активизируют деятельность альвеолярных макрофагов и нейтрофилов, что способствует повышению уровня нейтрофильной эластазы, металлопротеиназ, играющих важную роль в патогенезе ЭЛ. Кроме того, при длительном курении снижается активность ингибиторов протеолиза, и прежде всего a1-АТ, а протеазы, особенно в условиях даже малейшей недостаточности функции антиферментов, вызывают значительное повреждение эластических волокон и разрушение тонких структур респираторного отдела легкого. Кроме того, табакокурение активизирует процессы свободнорадикального окисления. В табачном дыме содержатся оксиданты, которые подавляют активность антиэластазных ингибиторов, тормозят восстановительные процессы в поврежденном эластическом каркасе легкого. Под влиянием курения снижается и содержание антиоксидантов в плазме крови. Все это способствует развитию ЭЛ [18, 23, 25, 34].
Среди факторов, провоцирующих развитие ЭЛ, особо следует отметить поллютанты и профессиональные вредности, так как они оказывают повреждающее действие на легочную ткань, приводят к формированию хронических процессов в дыхательных путях и появлению дисбаланса в системе протеолиз-антипротеолиз. Наибольшее значение среди поллютантов имеют диоксиды серы и азота, озон. Проникновение воздушных поллютантов ингаляционным путем приводит к повреждению мембран апикальной части эпителиальных клеток, что способствует выходу воспалительных медиаторов, лейкотриенов и нарушению в системе оксидант-антиоксидант. Истощение антиоксидантной системы играет важную роль в продолжающемся воспалении слизистой оболочки дыхательных путей [23]. К развитию эмфиземы приводит также воздействие взвешенной пыли, твердых частиц, углеводородов и др. Особенно опасна для развития ЭЛ ископаемая угольная пыль [6]. Исследования показали, что у эмфиземы, вызванной воздействием минеральной пыли и табачного дыма, сходные механизмы возникновения [30].
Одной из причин развития ЭЛ является легочная инфекция. Инфекционное воспаление стимулирует протеолитическую активность макрофагов и нейтрофилов. Бактерии также могут выступать в качестве дополнительного источника протеолитических агентов, в том числе эластазы. Все это ведет к развитию протеазно-антипротеазного дисбаланса. В последнее время немаловажное значение в патогенезе ХОБ и ЭЛ придается респираторным вирусам. Сами по себе вирусы не вызывают выраженной нейтрофильной или макрофагальной реакции, но из-за высокой контагиозности и способности подавлять местный и общий иммунитет они в большинстве случаев способствуют обострению воспалительных процессов с развитием бактериальной инфекции [13, 19].
Раньше развитие эмфиземы легких на фоне ХОБ связывалось с нарушением бронхиальной проходимости, что приводило к возникновению клапанного механизма и развитию феномена «воздушной ловушки». Однако в настоящее время значение механизма «воздушной ловушки» в развитии эмфиземы легких оспаривается. По мнению ряда авторов, клапанный механизм следует рассматривать скорее как следствие, а не причину заболевания.
Таким образом, ведущим патогенетическим механизмом развития ЭЛ считается дисбаланс в системе протеазы-антипротеазы, при котором наблюдается избыток протеаз или недостаток антипротеаз, что ведет к аутолизу тончайших структур респираторного отдела легочной ткани [8, 23].
Патологическая анатомия эмфиземы легких
Изменения в гистологической картине эмфиземы касаются бронхов и бронхиол, соединительной и эластической ткани легких, альвеолярного эпителия и легочных сосудов. Основным морфологическим критерием диффузной эмфиземы легких является деструкция респираторного отдела легких. Новейшие исследования показали, что размеры входа в альвеолы у здорового человека составляют не более 10 мкм, в то время как при ЭЛ альвеолярные поры превышают 20 мкм. Стенки альвеол представлены гладкими мышцами сосудов. Истончаются и запустевают капилляры. Эластические волокна находятся на стадии дегенерации. Все это приводит к уменьшению поверхности активно функционирующих альвеол. Эмфизематозно измененные альвеолы вызывают сдавление неизмененных, что также имеет немаловажное значение в нарушении вентиляционной функции легких [23].
Морфологическая классификация ЭЛ основана на ее отношении к различным частям ацинуса или дольки. Различают панацинарную (панлобулярную,), центриацинарную (центрилобулярную, проксимальную), периацинарную (дистальную, парасептальную), иррегулярную (околорубцовую), буллезную эмфиземы.
Панацинарная (панлобулярная) эмфизема характеризуется более или менее равномерным поражением ткани ацинусов. Процесс захватывает весь ацинус без избирательного изменения в области респираторных бронхиол или альвеол. Изменения преобладают в нижних отделах легких. Такая форма чаще наблюдается при первичной диффузной эмфиземе у больных с гомозиготным дефицитом a1-АТ.
При центриацинарной (центрилобулярной, проксимальной) эмфиземе изменения происходят в первую очередь в центральной части ацинуса, что соответствует респираторным бронхиолам, которые увеличены, так как их стенки подвергаются деструкции и растягиваются. Респираторные бронхиолы окружены неизмененными или малоизмененными альвеолами по периферии ацинуса. Центриацинарная ЭЛ чаще развивается у больных хроническим обструктивным бронхитом и наблюдается преимущественно в верхних отделах легких (задних и апикальных сегментах), иногда в верхушечных сегментах нижних долей.
Морфологически выделяют также периацинарную (дистальную, перилобулярную, парасептальную) эмфизему легких, при которой поражаются преимущественно периферические отделы ацинусов, прилежащие к межацинарным перегородкам, плевре.
Отношение иррегулярной, или околорубцовой, эмфиземы легких к ацинусу установить трудно, так как ее развитие чаще всего связано с рубцовыми изменениями в легких или с очагами фиброза. Она развивается при туберкулезе, саркоидозе, пневмокониозе, гистоплазмозе, эозинофильной гранулеме и др. Такая эмфизема является неравномерной, локальной. Она имеет деструктивный характер, но процесс локализуется в строго определенном участке легочной ткани. При иррегулярной эмфиземе поражаются как альвеолы, так и респираторные бронхиолы, альвеолярные ходы и мешочки; особенно характерно для нее расширение альвеолярных ходов [10, 23].
Буллезная эмфизема характеризуется формированием воздушных полостей диаметром более 0,5 см (булл). Эмфизему легких, сопровождающуюся формированием множества крупных булл, называют иногда буллезной болезнью. По локализации буллы делят на подплевральные и интрапаренхиматозные. По размеру различают мелкие (до 1 см), средние (1–5 см), крупные (5–10 см) и гигантские (более 10 см) буллы. По форме — округлые, овальные, полиморфные. Выделяют также напряженные, ненапряженные и спавшиеся; вентилируемые и невентилируемые; тонкостенные и толстостенные буллы. Для клинического применения разработана следующая классификация буллезной эмфиземы легких [7]: солитарные буллы; множественные буллы; буллы с диффузной эмфиземой; буллы с другими заболеваниями (симптоматические буллы); односторонняя легочная эмфизема (cиндром Маклеода). Следует различать понятия буллы и блебы. Блебы (blebs), или пузыри, образуются в соединительнотканных прослойках легкого при интерстициальной эмфиземе легких вследствие разрыва легочных структур с проникновением воздуха в интерстиций. Чаще всего буллы образуются при локализованных или иррегулярных видах ЭЛ. Однако и при диффузных формах (центриацинарной, панацинарной), особенно на поздних стадиях заболевания, возможно развитие множественных булл.
Необходимо иметь в виду, что приведенное выше морфологическое деление эмфиземы легких является схематичным и морфологическое распознавание различных видов эмфиземы, особенно на поздних стадиях развития, в запущенных случаях, может представлять значительные трудности [13, 18].
Патологическая физиология
Функциональные изменения при ЭЛ обусловлены несколькими взаимосвязанными механизмами: нарушением эластического каркаса легких, ведущим к изменению структуры легочных объемов и механических свойств легких; бронхиальной обструкцией; деструкцией межальвеолярных перегородок с прогрессирующим уменьшением общей функционирующей поверхности легких и снижением диффузионной способности. Одним из важных патогенетических факторов является механизм экспираторного закрытия мелких дыхательных путей. В настоящее время большое внимание в патогенезе ЭЛ уделяется также утомлению дыхательной мускулатуры. Кроме того, дыхательная недостаточность усугубляется сдавлением гигантскими буллами нормальной в функциональном отношении легочной ткани. Нарушение газообмена при ЭЛ обусловлено: ухудшением легочной вентиляции, поддерживающей постоянный газовый состав альвеолярного воздуха; нарушением кровообращения в легких и корреляцией между процессами вентиляции и перфузии в альвеолах; затруднением диффузии газов через альвеолокапиллярную мембрану из-за ее деструкции; раскрытием в легких артериовенозных анастомозов. Сложная патофизиологическая картина ЭЛ в каждом конкретном случае имеет свои особенности, зависящие от ее формы и тяжести течения [16, 18, 23].
Клиническая картина ЭЛ включает проявления самой эмфиземы, хронического бронхита, который часто предшествует ее развитию или сопутствует ей, а также дыхательной и сердечной недостаточности, осложняющих ее течение. Имеется сходство в клинической картине ЭЛ, хронического обструктивного бронхита, бронхиальной астмы (особенно ЭЛ и ХОБ), что является одной из причин их объединения в понятие хронических обструктивных заболеваний легких (ХОБЛ). Однако каждое из этих заболеваний имеет свои характерные особенности.
Одышка — первая и основная жалоба больных эмфиземой легких. Одышка в начале болезни появляется только при значительной физической нагрузке, и первоначально больные часто ее не замечают. Одышка у больных ЭЛ опасна тем, что долгие годы, заметно не проявляясь и исподволь прогрессируя, она превращается в состояние, угрожающее жизни больного. Толерантность к физическим нагрузкам резко снижена, так как даже в состоянии покоя компенсаторные возможности находятся на пределе. Одышка обычно имеет экспираторный характер. У больных наблюдаются короткий, «острый», «хватающий» вдох и удлиненный, иногда ступенеобразный выдох. Они осуществляют выдох при сомкнутых губах, надувая щеки («пыхтят»). При этом повышается давление в бронхиальном дереве, что уменьшает экспираторный коллапс мелких бесхрящевых бронхов (обусловленный нарушением эластических свойств легочной ткани и возрастанием внутригрудного давления) и способствует увеличению объема вентиляции. Кашель не является специфической жалобой больных ЭЛ и чаще всего обусловлен наличием хронического бронхита. Как правило, кашель при этом бывает сухой или с небольшим количеством трудноотделяющейся мокроты слизистого характера. Обострение бронхита всегда сопровождается усилением кашля и отделением мокроты слизисто-гнойного характера. Необходимо обращать внимание на появление непродуктивного кашля и прекращение отхождения мокроты, что может свидетельствовать о тяжелом обострении обструктивной болезни легких, нередко связанном с развитием синдрома утомления дыхательных мышц. Застою мокроты в просвете дыхательных путей способствует также употребление седативных и противокашлевых средств [23].
Масса тела при ЭЛ снижена, что связано с напряженной работой респираторных мышц, направленной на преодоление высокого сопротивления терминального отдела дыхательных путей [23]. Пациенты с эмфиземой легких в начальных стадиях заболевания принимают вынужденное положение на животе с опущенными вниз головой и плечевым поясом, что приносит им облегчение. При таком положении больного достигаются повышение брюшного давления, поднятие вверх диафрагмы и улучшение ее функции. Однако при тяжелой эмфиземе c выраженными изменениями грудной клетки и утомлением респираторных мышц горизонтальное положение вызывает напряженную работу диафрагмы, поэтому больные вынуждены даже спать в сидячем положении [23]. Больные ЭЛ нередко занимают положение сидя с несколько наклоненным вперед туловищем, опершись руками о колени или край кровати, что позволяет фиксировать плечевой пояс и включить дополнительную мускулатуру в акт дыхания. Цвет кожных покровов при эмфиземе легких скорее розовый, чем синюшный. Маловыраженный цианоз обусловлен длительным сохранением газового состава крови, только в далеко зашедших случаях появляется цианоз, который обусловлен развитием гиперкапнии. При этом у больных выявляется «вересковый язык» (голубой оттенок языка), который является клиническим показателем гиперкапнии и больше характерен для ХОБ. Наблюдается набухание шейных вен во время выдоха из-за повышения внутригрудного давления. Большое значение в прогнозе заболевания имеет оценка дыхательной мускулатуры, так как появление синдрома ее утомления всегда свидетельствует о прогрессировании болезни и усугублении дыхательной недостаточности [23]. Необходимо оценить синхронность участия в дыхательном цикле диафрагмы, мышц брюшного пресса, плечевого пояса, шеи и межреберных мышц. Нужно уметь выявлять дискоординацию дыхательных движений, а также следить за появлением признаков парадоксального дыхания, когда ребра на вдохе парадоксально втягиваются, что связано с тягой низкостоящей уплощенной диафрагмы.
При осмотре грудной клетки выявляется бочкообразная грудная клетка. Иногда наблюдается кифоз. При перкуссии определяется коробочный звук. Отмечаются увеличение высоты стояния верхушек, смещение нижних границ легких вниз и резкое ограничение подвижности нижнего легочного края. Характерно уменьшение сердечной и печеночной тупости за счет повышенной воздушности и увеличения объема легочной ткани. При аускультации выслушивается ослабленное везикулярное дыхание (в тяжелых случаях — резко ослабленное). Побочные дыхательные шумы не характерны для больных ЭЛ. Однако при форсированном выдохе или при проведении кашлевой пробы могут появляться скудные сухие свистящие хрипы.
Изолированная ЭЛ встречается редко. Как правило, она сочетается с признаками хронического обструктивного бронхита. Дифференциальная диагностика этих двух состояний представляет порой определенные трудности, что является еще одной причиной их объединения в понятие ХОБЛ. Признаки бронхита и эмфиземы очень часто, особенно в запущенных случаях, встречаются в различных сочетаниях. Однако нередко у больных ХОБЛ удается выделить преобладание признаков ЭЛ или бронхита, в связи с чем говорят о двух вариантах ХОБЛ: эмфизематозном и бронхитическом. Эмфизематозный вариант иногда называют «одышечный», «розовый», «пыхтящий», а больных этим вариантом ХОБЛ — «розовыми пыхтельщиками». Основной жалобой является прогрессирующая одышка, напоминающая пыхтение. В клинической картине ведущими являются симптомы, типичные для ЭЛ. Характерны длительное сохранение газового состава крови в покое и позднее развитие легочного сердца. Бронхитический тип («кашляющий», «синюшный», «отечный») характеризуется преобладанием симптомов бронхита. Основной жалобой является продуктивный кашель. Наблюдаются выраженный цианоз, симптомы легочного сердца, которое развивается на ранних стадиях болезни. Больные с таким вариантом ХОБЛ имеют вид «синюшных отечников». Эти два варианта ХОБЛ в чистом виде встречаются редко, и причисление больных к тому или иному типу часто вызывает затруднение. Значительная часть пациентов попадает в смешанную, промежуточную, группу лиц, у которых имеются признаки ХОБ, ЭЛ, дыхательной недостаточности и легочного сердца, выраженные в той или иной степени.
Инструментальные методы диагностики
Рентгенологическое исследование. Основными рентгенологическими признаками являются увеличение прозрачности легочных полей и их общей площади, ослабление сосудистого легочного рисунка, низкое расположение и уплощение диафрагмы, ограничение ее подвижности, увеличение костодиафрагмальных углов. Сердце, как правило, не увеличивается; вследствие низкого стояния диафрагмы оно принимает каплевидную форму («капельное сердце»). Происходит расширение ретростернального пространства, увеличение размеров которого и ослабление легочного рисунка на периферии наилучшим образом коррелируют с выраженностью эмфиземы [13]. Особое значение в диагностике имеют рентгенофункциональные пробы, в частности проба Ю. Н. Соколова и ее модификации, которые основаны на изменении прозрачности легочных полей в разных фазах дыхания. На томограммах определяются уменьшение калибра мелких сосудистых разветвлений, расширение корней легких. На ангиограммах выявляются признаки деваскуляризации. Бронхографическая картина характеризуется как «зимнее дерево без листьев».
Функциональное исследование легких имеет важное значение в диагностике ЭЛ, для которой характерны увеличение общей емкости легких и остаточного объема, снижение жизненной емкости легких. Наблюдаются повышение сопротивления в дыхательных путях на выдохе (в отличие от ХОБ, при котором сопротивление повышено на вдохе и выдохе) и стойкое снижение скоростных показателей (ФЖЕЛ, ОФВ1, теста Тиффно, скоростных максимальных экспираторных потоков, рассчитываемых по кривой поток/объем). Проведение ингаляционных тестов с бронходилятаторами позволяет выявить у больных эмфиземой стойкий необратимый характер бронхиальной обструкции. У больных ХОБ может наблюдаться частичный бронходилятационный ответ. Одним из ранних признаков ЭЛ является снижение диффузионной способности. Отмечаются также увеличение статической и уменьшение динамической растяжимости легочной ткани [13, 18, 23].
При развитии дыхательной недостаточности, чтобы правильно выбрать лечение и определить прогноз, необходимо исследовать газовый состав крови. Напряжение кислорода в артериальной крови ниже 60 мм рт. ст. свидетельствует о терминальной дыхательной недостаточности. Таким больным целесообразно проводить длительную кислородотерапию. Особого внимания требуют больные с повышенным напряжением СО2 в артериальной крови, так как с гиперкапнией связаны обострение дыхательной недостаточности и развитие синдрома утомления дыхательных мышц [23].
Изменения в периферической крови
Для больных ХОБЛ в связи с гипоксией характерно развитие полицитемического синдрома (повышение числа эритроцитов и уровня гемоглобина, низкая скорость оседания эритроцитов, высокая вязкость крови), что еще больше усугубляет дыхательную недостаточность. Эти изменения более характерны для больных ХОБ.
Лечение
Лечение больных ЭЛ представляет собой сложную задачу. Терапия должна быть направлена на лечение собственно ЭЛ, ХОБ, осложнений заболевания (дыхательной и сердечной недостаточности в случае присоединения легочного сердца), а также включать мероприятия, нацеленные на повышение качества жизни больных и замедление прогрессирования болезни. Первоочередное значение имеет отказ от курения. Здесь важна активная позиция врача, направленная на борьбу с курением. В настоящее время для врачей разработаны методические рекомендации по лечению табачной зависимости [23, 28].
Методы специфического лечения собственно ЭЛ, направленные на уменьшение потери легкими эластичности, до конца не разработаны. Предлагается заместительная терапия дефицита a1-антитрипсина донорской плазмой, нативным a1-АТ из сыворотки здоровых доноров, а также a1-АТ, созданным методом генной инженерии. Пациенты с уровнем a1-АТ в плазме менее 11 mumol/L, имеющие обструкцию воздухоносных путей, должны рассматриваться как претенденты на заместительную терапию. Заместительная терапия особенно показана больным с наследственным дефицитом a1-АТ. Новые подходы к лечению предполагают назначение аэрозолей a1-АТ [37, 42]. Исследуется возможность применения низкомолекулярных синтетических ингибиторов эластазы, в том числе новых водорастворимых [38]. Действие всех этих средств направлено против ферментативного разрушения соединительно-тканной стромы легких. Большие надежды в терапии больных с наследственным дефицитом a1-АТ возлагаются на метод генной инженерии, который позволяет «исправлять» дефектный ген [20, 37]. В целях повышения синтеза a1-АТ предлагается использовать синтетический анаболический стероид деназол [9]. На стадии изучения находится направление по применению средств, восстанавливающих поврежденные эластические волокна. Экспериментально была показана возможность их восстановления, в частности при использовании ретиновой кислоты [32, 33]. Для коррекции системы протеолиз-антипротеолиз целесообразно назначение антиоксидантов (витамина Е, аскорбиновой кислоты, глутатиона, b-каротина, микроэлементов цинк и селен, тиосульфата натрия и др.). В последнее время выявлено, что муколитик ацетилцистеин обладает антиоксидантными свойствами [23], однако он не показан больным с наследственным дефицитом a1-АТ [9]. Возможно применение средств, влияющих на сурфактантную систему легких, восстанавливающих поверхностно-активные свойства альвеолярной выстилки. С этой целью используются различные вещества для интратрахеального введения: эвкалиптовое масло, ментол, камфора, жирные кислоты, пальмитиновая кислота, дипальмитил-лецитин, фосфолипиды [3]. Имеется опыт интратрахеального введения липосом. В последние годы разработан новый липосомальный препарат на основе природных фосфолипидов — липин [26]. Имеются данные о положительном влиянии на сурфактантную систему легких антагонистов кальция при их сочетанном применении внутрь и ингаляционно [11], лазолвана, бромгексина, глицерама (особенно выраженным сурфактантпротективным действием обладает лазолван) [14]. Считается, что для восстановления сурфактантной системы наиболее перспективным является метод ингаляционного введения сурфактанта непосредственно в легкие [12]. Однако следует отметить, что методы воздействия на эластические свойства легких при эмфиземе, а также на сурфактантную систему недостаточно разработаны и внедрены в широкую практику.
В большинстве случаев буллезной ЭЛ эффективным является хирургическое лечение. Наиболее перспективными считаются видеоторакоскопические операции. Особенно широкое распространение они получили в последние 10 лет в связи с развитием эндоскопической техники [7]. В последнее время разработаны также хирургические методы лечения диффузной эмфиземы: хирургическая редукция легочного объема и трансплантация легких [15, 40].
В терапии ЭЛ важное место отводится лечению ХОБ, поскольку эти два патологических процесса нередко протекают параллельно и между ними порой бывает трудно провести грань. При этом используются бронходилятирующие и мукорегуляторные средства, иммунокорригирующая терапия, антибактериальные средства (при обострении воспалительного процесса), кортикостероиды и др. Для лечения ХОБ и ЭЛ применяются бронхорасширяющие препараты трех основных групп: b2-агонисты, антихолинергические средства, теофиллины. У больных ХОБ с ЭЛ действие ингаляционных холинолитиков по сравнению с b1-агонистами оказывается более выраженным, а число побочных реакций — минимальным. b2-агонисты должны с осторожностью использоваться у пожилых пациентов, особенно с патологией сердца, так как у них могут проявляться нежелательные кардиотоксические эффекты, характерные для этой группы препаратов. b2-агонисты целесообразно комбинировать с ингаляционными холинолитиками, когда монотерапия последними оказывается неэффективной. Возможно использование комбинированного препарата беродуала, содержащего ипратропиум бромид и фенотерол. В последнее время широкое распространение получила ингаляционная терапия через небулайзер. Преимущества небулайзерной терапии заключаются в том, что не требуется координации вдоха и ингаляции; ингаляция легковыполнима у пожилых и тяжелых больных; возможна доставка высоких доз лекарственного препарата за короткий период времени; создается высокодисперсный аэрозоль с идеальным диаметром частиц 1–5 мкм, который способен достичь периферических отделов дыхательных путей. Теофиллины обладают менее выраженным бронхолитическим эффектом, однако с их использованием связан ряд побочных эффектов, например уменьшение системной легочной гипертензии. Кроме того, они влияют на сердечный выброс, усиливают диурез, стимулируют центральную нервную систему, предотвращают и уменьшают утомление дыхательной мускулатуры. Предпочтение отдается пролонгированным формам теофиллина. Их назначение наиболее показано в ходе комплексной терапии ХОБЛ, когда предшествующая сочетанная терапия холинолитиками и b2-агонистами оказалась недостаточной [1, 23].
Глюкокортикостероидная терапия показана при тяжелой ЭЛ, при быстром прогрессировании болезни и в случае неэффективности максимальных доз препаратов базисной терапии (бронхорасширяющих средств). Обычно назначается пробная терапия преднизолоном в дозе 15–20 мг в сутки с оценкой эффективности в ближайшие 3–4 дня. Показания к назначению кортикостероидов противоречивы. Известно, что только 20-30% больных с ХОБЛ отвечают положительно на длительное лечение оральными кортикостероидами [1, 23, 28]. Следует учитывать миопатическое действие кортикостероидов на скелетную мускулатуру, а также возможность усугубления остеопороза, который развивается при ЭЛ. Для лечения остеопороза целесообразно использовать витаминные препараты, особенно витамин D3, минеральные соли, содержащие кальций, а в более тяжелых случаях показана курсовая терапия кальцитонином [23].
Важным направлением в лечении ЭЛ является коррекция дыхательной недостаточности, которая достигается путем оксигенотерапии и тренировкой дыхательной мускулатуры. Оксигенотерапия показана при снижении РаО2 до 60 мм рт. ст. и менее, SaO2