Ацетат натрия что это такое
Ацетаты натрия (Е262)

Характеристика химических свойств и способа получения добавки Е262
По своей структуре ацетаты натрия – это соли уксусной кислоты, так как именно из этого сырья её и получают: карбонаты или гидроксиды натрия подвергают реакции с кислотой. Как ни странно, часть производство вещества связано с перегонкой и обработкой древесины.
Добавка имеет вид кристаллического порошка, которое имеет слабый запах уксуса. Может иметь белесоватый, светло-жёлтый или коричневый оттенок. Вещество хорошо растворимо в воде, хуже – в спиртах и эфире. Кроме того, оно не подвержено горению.
Основные свойства ацетатов натрия, за которые его так ценят промышленники – это способность к регуляции уровня кислотности химической среды, консервации и стабилизации веществ. Добавка помогает сохранить форму и текстуру продуктов, их вкусовые и ароматические характеристики, способна улучшить консистенцию сырья.
Немногие добавки могут похвастаться тем, что они встречаются в живой природе. Как раз ацетаты натрия могут: они существуют как элемент клеток животных и растений, как составляющая кислот во фруктах, присутствует в кисломолочных продуктах как результат ферментации бактерий.
Области применения вещества человеком
Существует несколько видов ацетатов натрия: технический и пищевой. Первую разновидность используют в производстве химических грелок и обогревателей, как составную часть смеси “горячий лёд”. В сфере строительства ацетаты натрия дают противоморозный эффект для бетона, используются при возведении монолитных конструкций.
Текстильная промышленность применяет вещество при окрашивании тканей и дублении кожи. Также добавка используется в сфере фотографии и гальванотехники, в производстве красящих продуктов, средств гигиены, в химической отрасли.
По своей структуре технический ацетат натрия – это тригидрат натриевой соли уксусной кислоты, который имеет вид чешуек или кусочков различных форм.
Вообще человеку знакомы два типа добавки Е262:
Вещества имеют различные химические формулы, но мало отличаются друг от друга по своим свойствам.

В медицинской промышленности добавка применяется в изготовлении мочегонных препаратов и других лекарств.
Требования к упаковке добавки Е262
В любом из видов упаковки внутри должен быть дополнительный подклад из плотного пищевого полиэтилена. Так как вещество очень подвержено реакции с водой, на таре обычно ставят отметку “Беречь от влаги”.
Чаще всего ацетаты натрия хранятся и транспортируются в пищевых мешках из ткани (в таких обычно можно видеть муку и крупы). Также для этих целей используются ящики из гофрированного картона или многослойные бумажные пакеты, бочки, контейнеры.
Влияние на здоровье человека
По различным данным, вред от употребления продуктов с ацетатами натрия в составе колеблется от крайне незначительного уровня до среднего.
На сегодня официально добавка разрешена в США, Канаде, Европейском союзе, Украине, России, Австралии. Нет никаких официальных данных по поводу возможной связи между её применением и появлением онкологических заболеваний, генных мутаций, бесплодия, отравлений, по крайней мере, при потреблении в тех количествах, в которых вещество используется в пищевых продуктах.
Зафиксировано несколько случаев появления аллергической реакции у людей, страдающих аллергией на уксус.
Тем, кто имеет проблемы с функционированием вегетативной системы, жёлчного пузыря, кишечника, в частности, дисбактериоз, печени, почек, сердечно-сосудистой системы, лучше воздержаться от питания едой с добавкой в составе.
Превышение нормальной суточной дозировки ацетатов натрия для взрослого человека может обернуться некоторыми неприятными симптомами: головной болью и головокружением, нарушением координации, болями и спазмами в животе, судорогами, удушьем, изменением цвета кожных покровов и слизистых на более бледный.
По некоторым неподтверждённым данным, вещество всё-таки имеет свойства канцерогена по причине того, что в кишечнике оно превращается в нитраты, которые могут провоцировать появление злокачественных опухолей, или, как минимум, мощной аллергии. Официального подтверждения этой информации мировому сообществу предоставлено не было, поэтому ацетаты натрия не признаны онкогенной или опасной добавкой.
Некоторые специалисты советуют ограничить поступление вещества в организм ребёнка, чтобы не вызвать у него появление аллергии.
Натрия ацетат считается безвредным веществом, и имеет широкую сферу применения, от производства кожаных изделий до приготовления картофельных чипсов. Он обладает выраженными свойствами консерванта и стабилизатора, однако от других консервантов отличается тем, что не угнетает рост и развитие бактерий, и выступает как фермент, образующийся в процессе жизнедеятельности этих бактерий в веществах.
Существуют некоторые ограничения в употреблении продуктов с веществом в составе для аллергиков, детей и людей с нарушениями в работе внутренних органов.
Процессы исследований действия ацетатов натрия на человека продолжаются до сих пор, а пока, в силу отсутствия значительного негативного влияния на организм здорового человека, мировым сообществом не было установлено нормы суточного потребления добавки Е262.
Ацетат натрия
| Ацетат натрия | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | sodium acetate (ИЮПАК) sodium ethanoate (систематическое) ацетат натрия натрия этаноат |
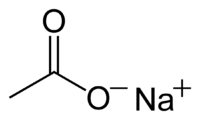
| Химическая формула | CH3COONa |
| Эмпирическая формула | C2H3O2Na |
| Физические свойства | |
| Состояние (ст. усл.) | белый гигроскопичный порошок |
| Молярная масса | 82.03 грамм/моль (безводная форма) 136.08 грамм/моль (тригидрат) г/моль |
| Плотность | 1,45 г/см³ |
| Термические свойства | |
| Температура разложения | 324 °C |
| Удельная теплота плавления | 264—289 к Дж/кг |
| Химические свойства | |
| Растворимость в воде | 76 г/100 мл |
Ацетат натрия CH3COONa, — натриевая соль уксусной кислоты, производится и широко применяется в промышленных масштабах.
Содержание
Область применения
Ацетат натрия используется в текстильном производстве для нейтрализации отработанной серной кислоты в сточных водах и как фоторезист при использовании анилиновых красителей. Также используется при дублении солями хрома (для протравливания), и замедляет процесс вулканизации хлоропрена при производстве синтетических резин.
Ацетат натрия известен как пищевая добавка E262 и применяется как консервант.
В растворе ацетат натрия (будучи солью слабой кислоты) и уксусная кислота могут применяться как буфер, для сохранения относительно постоянного pH. Это особенно полезно в биохимии в pH-зависимых реакциях.
На этом свойстве основан довольно красивый опыт — «горячий лёд»
Способы получения
Ацетат натрия недорог и его легче приобрести в хим. магазинах, чем синтезировать в лабораторных условиях. В лабораторных условиях получается при взаимодействии уксусной кислоты, например, с карбонатом натрия, гидрокарбонатом натрия или гидроксидом натрия.
Это — хорошо известная реакция «гашения» пищевой соды и винного уксуса, происходящая в тесте. 84 грамма гидрокарбоната натрия реагируют с 750 граммами 8 % винного уксуса (или же с 86 граммами 70 % уксусной эссенции) с образованием 82 грамм ацетата натрия в растворе. Выпариванием воды можно получить чистый кристаллический ацетат натрия или его концентрированный раствор.
Характерные реакции
Ацетат натрия может быть использован для образования эфира с алкил галогенидами такими как бромэтан:
При сильном нагревании (более 324 °C) ацетат натрия разлагается на карбонат натрия и ацетон:
Одновременно может проходить разложение до оксида натрия, ацетона и диоксида углерода:
Галерея
Химический обогреватель, содержащий перенасыщенный раствор ацетата натрия, выделяющего тепло при фазовом переходе в кристаллическую форму тригидрата ацетата натрия.
Натрия Ацетат
Химическое название
Натриевая соль уксусной кислоты, натрия этаноат.
Химические свойства
Белый гигроскопичный мелкий порошок, растворимый в воде. Разлагается при 324 градусах Цельсия. Молекулярная масса = 82 грамма на моль для безводной формы, 136,1 грамм на моль – для тригидрата. Формула Натрия Ацетата: CH3COONa; рацемическая формула: C2H3O2Na; формула тригидрата: C2H3O2Na х 3H2O.
Химические свойства
Вещество можно получить с помощью реакции уксусной кислоты с карбонатом или гидрокарбонатом натрия, с NaOH. В домашних условиях — это реакция винного уксуса с пищевой содой, к 1 грамму соды добавляют 9 грамм уксуса.
Реакция электролиза Ацетата Натрия. Во время превращения происходит диссоциация CH3COONa до CH3COO- и Na+. У анода выделяется этан и углекислый газ. Далее углекислый газ вступает в реакцию с гидроксидом бария или натрия (NaOH), во втором случаев пробирке останется чистый этан.
Достаточно популярна в химии реакция гидролиза Ацетата Натрия. Для наглядности, образованную слабой к-ой и сильным основанием соль, смешивают с индикатором-фенолфталеином. Смесь нагревают, при этом соль частично плавится и в расплаве появляются гидроксид-ионы. Затем пробирку охлаждают, соль кристаллизуется, и смесь утрачивает фиолетовую окраску. Соединение также реагирует с алкилгалогенидами, бромэтаном с образованием сложных эфиров.
Качественная реакция на Ацетат Натрия проводится в два этапа. Сначала определяют наличие в соединении ионов Na, а затем – кислотного ацетат-остатка. Натрий будет гореть ярко желтым пламенем, если небольшое количество раствора (или сухого вещ-ва) внести в пламя спиртовой горелки. Качественную реакцию на ацетат ион можно провести с помощью любой растворимой соли трехвалентного железа. Раствор станет красно-коричневого цвета, а при нагревании выпадет темно-коричневый осадок Fe(OH)3.
Химическое соединение используют при производстве текстиля; в качестве фоторезиста после применения анилиновых красителей; при вулканизации и в кожевенном производстве. Вещество получило широкое применение в виде пищевой добавки E262, используется в качестве консерванта; его применяют для сохранения стабильного рН в биохимии. Соединение используют при производстве химических обогревателей и грелок, («горячий лёд»). В медицине также используют тригидрат Натрия Ацетата.
Фармакологическое действие
Восстанавливает водно-солевой баланс.
Фармакодинамика и фармакокинетика
Натрия Ацетат применяют в комбинации с другими хим. соединениями. Вещество используют для дезинтоксикации и регидратации. Средство обладает способностью восстанавливать водный и электролитный баланс во время обезвоживания. Стимулирует диурез и предотвращает развитие метаболического ацидоза. Обладает дезинтоксикационным, регидратирующим и плазмозамещающим действием.
Показания к применению
Применяется при регидратации, интоксикации, гиперкалиемии, обезвоживании у пациентов с пищевыми инфекциями, холерой, острой дизентерией и так далее.
Противопоказания
Побочные действия
Редко при применении растворов для внутривенного введения с данным лекарственным средством возникает отечность, тахикардия, озноб.
Инструкция по применению (Способ и дозировка)
Натрия Ацетат в составе различных препаратов для внутривенного введения применяется в условиях стационара, под контролем лабораторных показателей. Растворы вводят струйно или капельно. Дозировка зависит от состояния пациента и тяжести состояния. Как правило, если пациент находится в тяжелом состоянии, то сначала вводят лекарство струйно, затем переходят на инфузии.
Передозировка
Нет сведений о передозировке средством.
Взаимодействие
Вещество часто применяют в комбинации с другими электролитами.
Ацетат Натрия можно сочетать с натрия хлоридом и натрием фумаровокислым, при этом необходимо визуально следить за совместимостью растворов.
Условия продажи
Может потребоваться рецепт.
Особые указания
Лечение препаратом проводят под контролем уровня электролитов крови и гематокрита.
Список опасных и безопасных Е-кодов продуктов питания
Вредны ли эти добавки? Специалисты-пищевики считают, что буква «Е» не так страшна, как ее малюют: применение добавок разрешено во многих странах, большинство из них не дает побочных эффектов. Но у медиков часто иное мнение.
Но медики все же настаивают на таком выводе: даже те пищевые добавки, которые производятся из натурального сырья, все же проходят глубокую химическую обработку. А поэтому последствия, сами понимаете, могут быть неоднозначными. Так что лучше есть то, что выращено своими руками без всяких химикатов и сохранено без консервантов. Жаль только, что не все мы садоводы и огородники.
Пищевые добавки, запрещенные к применению в РФ:
Пищевые добавки, не разрешенные к применению в РФ:
E103, E107, E125, E127, E128, E140, E153-155, E160d, E160f, E166, E173-175, E180, E182, E209, E213-219, E225-228, E230-233, E237, E238, E241, E252, E253, E264, E281-283, E302, E303, E305, E308-314, E317, E318, E323-325, E328, E329, E343-345, E349, E350-352, E355-357, E359, E365-368, E370, E375, E381, E384, E387-390, E399, E403, E408, E409, E418, E419, E429-436, E441-444, E446, E462, E463, E465, E467, E474, E476-480, E482-489, E491-496, E505, E512, E519-523, E535, E537, E538, E541, E542, E550, E552, E554-557, E559, E560, E574, E576, E577, E579, E580, E622-625, E628, E629, E632-635, E640, E641, E906, E908-911, E913, E916-919, E922-926, E929, E942-946, E957, E959, E1000, E1001, E1105, E1503, E1521.
Некоторые характеристики других пищевых добавок:опасны E110, E123, E127, E129, E150, E151, E173-175, E210, E212, E216-219, E227, E228, E235, E242, E339-341, E400-403, E450-452, E521-523, E541-556, E559, E574-579, E620-625, E900, E912, E951, E954, E965, E967, E999, E1200-1202
сомнительны E102, E104, E120, E122, E124, E141, E150, E161, E173, E180, E241
канцерогены E131, E142, E210-217, E239
разрушают витамин B12 E220
нарушают деятельность желудочно-кишечного тракта E221-226
нарушают функцию кожи E230, E231, E233
вызывают сыпь E311, E312
содержат много холестерина E320, E321
нарушают пищеварение E338, E340, E341, E407, E450, E461-463, E466, E468
Перечень химических обозначений пищевых добавок в алфавитном порядке:
Классификация пищевых добавок:
ААгар-агар, 1)РК РЖ E406
Адипаты натрия E356
Адипаты калия Е357
Адипиновая кислота E355
Азорубин, кармазин С E122
Аллура красная AC О E129
Алюминий (порошкоподобный)О E173
Алюмосиликат О Е559
Алюмосиликат кальция О Е556
Алюмосиликат калия О E555
Алюмосиликат натрия О E554
Алюмофосфат натрия О Е541
Альгинат амония О E403
Альгинат калия О E402
Альгинат кальция О E404
Альгинат натрия E401
Альгинова кислота О E400
Амарант ОР Ведет к накоплению извести в почках! E123
Аннато, биксин, норбиксин E160b
Аскорбат кальция E302
Аскорбат натрия E301
Аскорбинова кислота E300
Аспартам 2)ОО ГМ E951
Ацесульфам калия E950
Ацетаты калия E261
Ацетаты кальция E263
Ацетаты натрия E262
Ацетилированый дикрахмаладипат E1422
Ацетилированый дикрахмалфосфат E1414
Ацетилированый крахмал E1420
Ацетатизобутират сахарозы Е444
1) Натуральное, растительное желирующее вещество из красных водорослей. Неудобоваримое. Препятствует усвоению минеральных веществ организмом. В больших дозах оказывает слабительный эффект.
ББензоат калия ОС E212
Бензоат кальция E213
Бензоат натрия ОС E211
Бензойна кислота ОС E210
Бета-апо-8′-каротинал (C 30) E160e
Бета-апо-8′-каротиновой кислоты (C 30) этиловый эфир E160f
Бифенил, дифенил ВК E230
Борная кислота E284
Бутилгидроксианизол (BHA) РС Х E320
Бутилгидрокситолуол, ионол (BHT) С Х E321
ВВинная кислота (L(+)-винная кислота) E334
Воск канделильский E902
Воск карнаубский E903
Воск оксидированый полиэтиленовый E914
Воск пчелиный, белый и желтый E901
Гваяковая смола Е314
Гидроксид амония E527
Гидроксид калия E525
Гидроксид кальция E526
Гидроксид магния E528
Гидроксид натрия E524
Гидросульфит калия E228
Глутамат магния О E625
Глутаминова кислота О E620
Глутамат натрия I-замещенный О Е621
Глутамат калия I-замещенный О Е622
Глутамат аммония I-замещенный О Е624
Гуанилат кальция E629
Гуаниловая кислота E626
Гуарова камедь С E412
2) Искусственное вещество, производится из аммониака и формальдегида. В Западной Европе допущен только в сырах Provalone. Применяется в лекарственных препаратах, для дезинфекции кожи и мочевыводящих путей, а также в качестве консерванта в косметике
Динатрий 5′-рибонуклеотид E635
Дифенил С О 3) Е230
Диметилдикарбонат О Е242
Диоксид кремния аморфный (кремневая кислота) Е551
Двуокись углерода E290
Двуокись кремния E551
Двуокись титана E171
Додецилгалат С E312
3) Разрешен, как консервант против плесени и грибков для обработки кожуры цитрусовых, может быть перенесен пальцами на мякоть самого фрукта. Рекомендуется, после чистки, тщательно вымыть руки. У животных в больших дозах вызывает внутреннее кровотечение и изменения органов.
ЖЖирные кислоты E 570
ИИзоаскорбинат натрия Е316
Изоаскорбиновая (эриторбовая) кислота Е315
Инозиновая кислота Е630
KКамедь рожкового дерева С E410
Камедь карайи О Е416
Камедь гваяковая П Е241
Камедь ксантановая Е415
Камедь тары С Е417
Камедь геллановая Е418
Каррагинан О РК Е407
Карбамид (мочевина) Е927b
Краситель синий блестящий E133
Краситель черный ВК E151
Краситель пищевой оранжево-желтый ‘солнечный закат’ ОС E110
Краситель пищевой зеленый-S E142
Краситель пищевой ‘золото’ Е175
Краситель пищевой ‘индиго-кармин’ Е132
Краситель пищевой куркумин Е100
Краситель пищевой рибофлави Е101
Краситель пищевой тартразин ОС Е102
Краситель пищевой алканет (алканин) Е103
Краситель пищевой желтый хинолиновый С Е104
Краситель пищевой кармин (из насекомых щитовок!) C Е120
Краситель пищевой азорубин (кармуазин) С Е122
Краситель пищевой амарант С Е123
Краситель пищевой пунцовый С Е124
Краситель пищевой красный С Е128
Краситель пищевой красный ‘очаровательный’ (аллура) С Е129
Краситель пищевой синий патентованный Е131
Краситель пищевой индигокармин Е132
Краситель пищевой синий блестящий Е133
Краситель пищевой хлорофилл Е140
Краситель пищевой медные комплексы хлорофиллов Е141
Краситель пищевой зеленый S Е142
Краситель пищевой cахарные колеры простые Е150a
Краситель пищевой cахарные колеры сульфитные Е150b
Краситель пищевой cахарные колеры аммония О Е150с
Краситель пищевой cахарные колеры аммоний-сульфитные О Е150d
Краситель пищевой черный блестящий О Е151
Краситель пищевой уголь растительный Е153
Краситель пищевой коричневый FK С Е154
Краситель пищевой коричневый HT С Е155
Краситель пищевой каротины Е160a
Краситель пищевой экстракты аннато Е160b
Краситель пищевой маслосмолы паприки Е160c
Краситель пищевой ликопин Е160d
Краситель пищевой бета-апокаротиновый альдегид Е160e
Краситель пищевой эфиры бета-апо-8′-каротиновый кислоты Е160f
Краситель пищевой флавоксантин Е161b
Краситель пищевой красный свекольный Е162
Краситель пищевой антоцианы Е163
Краситель пищевой углекислые соли кальция Е170
Краситель пищевой титана диоксид Е171
Краситель пищевой окиси железа Е172
Краситель пищевой алюминий О Е173
Краситель пищевой серебро О Е174
Краситель пищевой золото О Е175
Краситель пищевой литолрубин BK С Е180
Концентрат токоферолов Е306
Краситель из паприки, капсантин, капсорубин E160c
Карбонаты натрия Е500
Карбонаты калия Е501
Карбонаты аммония Е503
Карбонаты магния Е504
Квасцы алюмо-натриевые О Е521
Квасцы алюмо-калиевые О Е522
Квасцы алюмо-аммиачные О Е523
ЛЛецитины, фосфатиды Е322
Лактат натрия Е325
Лактат кальция Е327
Лактат аммония Е328
Лимонная кислота Е330
Лактилаты натрия Е481
Лактилаты кальция Е482
ММуравьиная кислота Е236
Молочная кислота Е270
Малат аммония Е349
Малаты натрия Е350
Малаты кальция Е352
Мета-винная кислота Е353
Моно- и диглицериды жирных кислот Е471
Нитрит калия О Е249
Нитрат натрия О Е251
Нитрат натрия О Е252
ООрто-фенилфенол ВК О Е231
Орто-фенилфенола натриевая соль О Е232
Октилгаллат С О Е311
Орто-фосфорная кислота О РК Е338
Оксид кальция Е529
Пропионовая кислота О Е280
Пропионат натрия О Е281
Пропионат кальция О Е282
Пропионат калия О Е283
Пропилгаллат О Е310
Боровая кислота О Е284
Полиоксиэтиленсорбитан тристеарат О Е436
Пирофосфаты О Е450
Полифосфаты О Е452
Полидиметисилоксан О Е900
Полидекстрозы О Е1200
РРибонуклеотиды-5′ кальция Е 634
Сорбиновая кислота Е200
Сорбат натрия Е203
Сорбит и сорбитовый сироп Е420
Соли жирных кислот Е470
Сорбитанмоностеарат О Е491
Сорбитантристеарат О Е492
Сорбитанмонолаурат, СПЭН 20 О Е493
Сорбитанмоноолеат, СПЭН 80 О Е494
Сорбитанмонопальмитат, СПЭН 40 О Е495
Сорбитантриолеат, СПЭН 85 О Е496
Соляная кислота Е507
Серная кислота О Е513
Сульфаты натрия Е514
Сульфаты калия Е515
Сульфаты кальция Е516
Сульфаты аммония Е517
Сульфат алюминия О Е520
TТиабендазол ВК О Е233
Тартраты натрия Е335
Тартраты калия Е336
Тартраты калия-натрия Е337
Тартрат кальция Е354
Твин (полисорбат 20) О Е432
Твин (полисорбат 80) О Е433
Твин (полисорбат 40) О Е434
Твин (полисорбат 60) О Е435
Тиосульфат натрия Е539
УУголь растительный E153
Уксусная кислота ледяная Е260
Углерода диоксид Е290
ФФумаровая кислота Е297
Фосфаты натрия О Е339
Фосфаты калия О РК Е340
Фосфаты кальция О РК Е341
Фосфаты аммония Е342
Фосфаты аммония О Е343
Ферроцианид натрия Е535
Ферроцианид калия Е536
Ферроцианид кальция Е538
ХХлорид калия Е508
Хлорид кальция Е509
Хлорид аммония Е510
Хлорид магния Е511
ЦЦитраты натрия Е331
Цитраты калия Е332
Цитраты кальция Е333
Цитрат магния Е345
Цитраты аммония Е380
Цикламовая кислота и ее соли О Е952
Эфиры глицерина и смоляных кислот E445
(c) Федеральное бюджетное учреждение здравоохранения «Центр гигиены и эпидемиологии в Рязанской области», 2006-2021 г.
Адрес: 390046, Рязанская область, город Рязань, ул. Свободы, дом 89