Ацетилхолин что это такое где содержится
Ацетилхолин и его функции
Содержание
Холинергический синапс [ править | править код ]
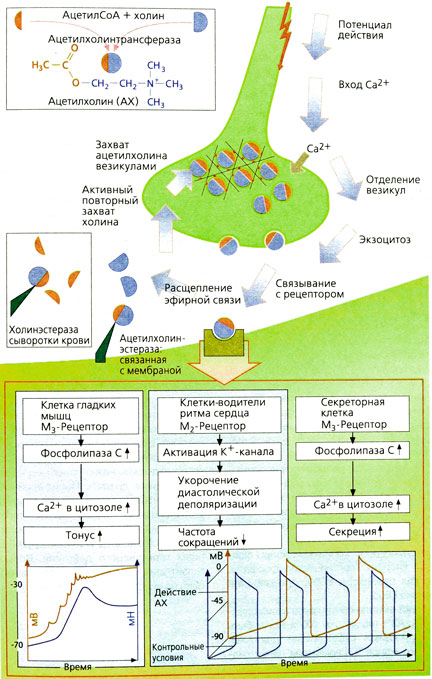
Ацетилхолин (АХ) — медиатор в постганглионарных синапсах — накапливается в высокой концентрации в везикулах аксоплазмы нервного окончания. АХ образуется из холина и активированной уксусной кислоты (ацетилкофермент А) под действием фермента ацетилхолинтрансферазы. Высокополярный холин активно захватывается аксоплазмой. На мембране холинергического аксона и нервных окончаний имеется специальная транспортная система. Механизм высвобождения медиатора до конца не раскрыт. Везикулы закреплены в цитоскелете при помощи белка синапсина таким образом, что их концентрация около пресинаптической мембраны высокая, однако контакт с мембраной отсутствует. При возникновении возбуждения повышается концентрация Са2+ в аксоплазме, активируются протеинкиназы, и происходит фосфорилирование синапсина, приводящее к отсоединению везикул и связыванию их с пресинаптической мембраной. Затем содержимое везикул выбрасывается в синаптическую щель. Ацетилхолин мгновенно проходит сквозь синаптическую щель (молекула АХ имеет длину около 0,5 нм, а ширина щели составляет 30-40 нм). На постсинаптической мембране, т. е. мембране целевого органа, АХ взаимодействует с рецепторами. Эти рецепторы возбуждаются также алкалоидом мускарином и поэтому называются мускариновыми ацетилхолиновыми рецепторами (М-холинорецепторы). Никотин имитирует действие ацетилхолина на рецепторы ганглионарных синапсов и концевой пластинки. Никотин возбуждает холинорецепторы ганглионарных синапсов и концевой пластинки мотонейрона, поэтому этот тип рецепторов назван никотиновыми ацетилхолиновыми рецепторами (N-холинорецепторы).
В синаптической щели ацетилхолин быстро инактивируется специфической ацетилхолинэстеразой, находящейся в щели, а также менее специфической сывороточной холинэстеразой (бутирилхолинэстеразой), находящейся в сыворотке крови и интерстициальной жидкости.
По своему строению, способу передачи сигнала и сродству к различным лигандам М-холинорецепторы подразделяются на несколько типов. Рассмотрим M1, М2- и М3-рецепторы. M1-Рецепторы находятся на нервных клетках, например ганглиях, и их активация способствует переходу возбуждения с первого на второй нейрон. М2-Рецепторы расположены в сердце: открытие калиевых каналов приводит к замедлению диастолической деполяризации и уменьшению частоты сердечных сокращений. М3-Рецепторы играют роль в поддержании тонуса гладких мышц, например, кишечника и бронхов. Возбуждение этих рецепторов приводит к активации фосфолипазы С, деполяризации мембраны и повышению тонуса мышц. М3-Рецепторы расположены также в клетках желез, которые активируются посредством фосфолипазы С. В головном мозге имеются разные типы М-холинорецепторов, играющие роль во многих функциях: передаче возбуждения, памяти, обучаемости, болевой чувствительности, контроле активности ствола мозга. Активация М3-рецепторов в эндотелии сосудов может приводить к высвобождению оксида азота N0 и таким образом расширять сосуды.
Ацетилхолин [ править | править код ]
Ацетилхолин (лат. Acetylcholinum) — медиатор нервной системы, биогенный амин, относящийся к веществам, образующимся в организме.
Ацетилхолину принадлежит важная роль как медиатору центральной нервной системы. Он участвует в передаче импульсов в разных отделах мозга, при этом малые концентрации облегчают, а большие — тормозят синаптическую передачу. Изменения в обмене ацетилхолина могут привести к нарушению функций мозга.
Ацетилхолин является посредником передачи нервного импульса к мышце. При недостатке ацетилхолина снижается сила сокращений мышц.
Окончания нервных волокон, для которых он служит медиатором, называются холинергическими, а рецепторы, взаимодействующие с ним, называют холинорецепторами. Холинорецепторы постганглионарных холинергических нервов (сердца, гладких мышц, желез) обозначают как м-холинорецепторы (мускариночувствительные), а расположенные в области ганглионарных синапсов и в соматических нервномышечных синапсах — как н-холинорецепторы (никотиночувствительнные). Такое деление связано с особенностями реакций, возникающих при взаимодействии ацетилхолина с этими биохимическими системами: мускариноподобных в первом случае и никотиноподобных — во втором; м- и н-холинорецепторы находятся также в разных отделах ЦНС.
Хранение и высвобождение ацетилхолина [ править | править код ]
При микроэлектродной регистрации электрических потенциалов постсинаптической мембраны нервно-мышечного синапса Фетт и Катц (Fatt and Katz, 1952) выявили спонтанные небольшие (0,1—3 мВ) деполяризующие потенциалы, возникающие случайным образом примерно 1 раз в секунду. Авторы назвали эти потенциалы миниатюрными потенциалами концевой пластинки. Их амплитуда была существенно ниже пороговой для развития потенциала действия. Они увеличивались под действием ингибитора АХЭ неостигмина и блокировались тубокурарином (конкурентным блокатором N-холинорецепторов); следовательно, они были обусловлены выделением ацетилхолина. В связи с этим было высказано предположение, что ацетилхолин выделяется из пресинаптических окончаний дробными постоянными порциями — квантами. Вскоре был обнаружен и морфологический субстрат квантов — синаптические пузырьки (De Robertis and Bennett, 1955). Когда в окончание аксона мотонейрона приходит потенциал действия, выделяется 100 и более квантов (пузырьков) ацетилхолина (Katz and Miledi, 1965). Закономерности хранения и выделения ацетилхолина, изученные на нервно-мышечном синапсе, применимы и к другим холинергическим синапсам с быстрой передачей.
Предполагается, что в каждом пузырьке содержится от 1000 до 50 000 молекул ацетилхолина, а в пресинаптическом окончании мотонейрона содержится 300 000 и более пузырьков. Кроме того, не исключено, что достаточно существенное количество ацетилхолина диффузно растворено в аксоплазме. Запись токов одиночных каналов постсинаптической мембраны нервно-мышечного синапса при постоянной аппликации ацетилхолина показала, что одна молекула этого медиатора вызывает потенциал порядка 3 х 10”7 В. Из этого следует, что даже минимальное (по расчетам) количество ацетилхолина в одном пузырьке — 1000 молекул — достаточно для того, чтобы вызвать миниатюрный потенциал концевой пластинки (Katz and Miledi, 1972).
Экзоцитоз ацетилхолина и других медиаторов из пресинаптических окончаний подавляется ботулотоксином и столбнячным токсином — ядами Clostridium botulinum и Clostridium tetani соответственно. Этими анаэробными спорообразующими организмами вырабатываются одни из самых сильных из известных токсинов (Shapiro et а. 1998). Токсины Clostridium, состоящие из связанных дисульфидными мостиками тяжелой и легкой цепей, соединяются с неизвестным пока рецептором на холинергическом окончании и затем посредством эндоцитоза переносятся в цитозоль. Легкая цепь представляет собой цинксодержащую эндопептидазу, которая после активации гидролизует компоненты ядра комплекса SNARE, участвующего в экзоцитозе. Различные типы ботулотоксина разрушают разные белки пресинаптической мембраны (синтаксин-1 и SNAP-25) и синаптических пузырьков (синаптобревин). Ботулотоксин А как лекарственное средство рассматривается в гл. 9 и 66.
Топ-10 добавок ацетилхолина, улучшающих работу мозга
Ацетилхолин и его действие на организм.
Добавки, повышающие уровень ацетилхолина и холина
Вы не можете получать ацетилхолин напрямую, но можете принимать добавки, увеличивающие его выработку организмом, замедляющие его распад, провоцирующие обратный захват, стимулирующие его рецепторы или предоставляющие ресурсы для его создания. Вещества, лекарства или добавки, увеличивающие синтез ацетилхолина, называют холинергическими.
Лучшие холинергические добавки делятся на три основные категории — на основе холина, травяные средства и питательные вещества. Некоторые из них настолько сильны, что их иногда назначают в качестве лекарств.
Холин битартрат является одним из витаминов B-комплекса и предшественником ацетилхолина. Примерно 90% из нас не получают достаточное его количество из рациона. Содержится он главным образом в яичном желтке, говядине и морепродуктах. Добавки холина являются отличным средством, предотвращающим дефицит, по крайней мере в теории. Однако не все из них увеличивают количество холина в головном мозге или повышают уровень ацетилхолина.
Как и в случае со всеми нейромедиаторами, его переизбыток так же вреден, как и нехватка. Общим симптомом передозировки является чувство депрессии. Некоторые люди жалуются на головные боли. Пациенты также могут столкнуться с напряжением в мышцах и судорогами, тошнотой и интенсивной усталостью. Если вы страдаете от этих симптомов, просто сделайте перерыв и дайте организму время приспособиться. Будьте особенно осторожны с такими мощными добавками, как гиперзин и галантамин, но имейте в виду, что любое средство, применяемое в качестве лекарства, является достаточно сильным, чтобы вызывать побочные эффекты или негативно взаимодействовать с другими веществами.
Молекула здравого ума
Автор
Редактор
Ацетилхолин — не самое знаменитое вещество, но он играет важную роль в таких процессах, как память и обучение. Давайте приоткроем завесу тайны над одним из самых недооцененных нейромедиаторов нашей нервной системы.
Первый среди равных
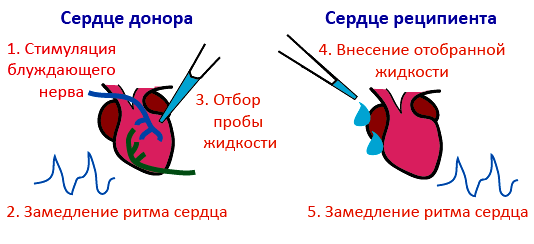
Рисунок 1. Классический опыт Отто Лёви по выявлению химических посредников передачи нервных импульсов (1921 год). Объекты — изолированные и погруженные в солевой раствор сердцá двух лягушек (донора и реципиента). Описание приведено в тексте. Рисунок с сайта en.wikipedia.org, адаптирован.
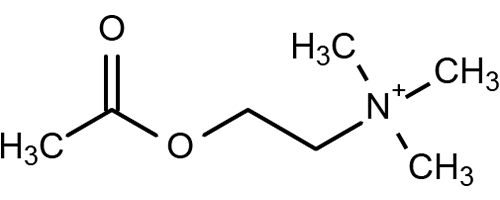
Рисунок 2. Структурная формула ацетилхолина. Рисунок с сайта www.curezone.org.
В научно-популярной литературе медицинской и нейрофизиологической направленности чаще всего речь заходит о трех нейромедиаторах: дофамине [1], серотонине [2] и норадреналине [3]. Во многом это объясняется тем, что нормальные и болезненные состояния, связанные с изменением уровня этих нейротрансмиттеров, доступнее для понимания и вызывают больше интереса у читателей. Об этих веществах я уже писал, теперь настало время уделить внимание еще одному медиатору.
Речь пойдет об ацетилхолине, и это будет символично, учитывая, что он был первым открытым нейромедиатором. В начале XX века между учеными велся спор, каким способом передается сигнал от одной нервной клетки на другую. Одни считали, что электрический заряд, пробежав по одному нервному волокну, передается на другое по каким-то более тонким «проводам». Их оппоненты утверждали, что существуют вещества, которые переносят сигнал от одной нервной клетки к другой. В принципе, обе стороны оказались правы: существуют химические и электрические синапсы. Однако сторонники второй гипотезы оказались «правее» — химические синапсы преобладают в организме человека.
Чтобы разобраться в особенностях передачи сигнала от одной клетки к другой, физиолог Отто Лёви проводил простые, но изящные опыты (рис. 1). Он стимулировал электрическим током блуждающий нерв лягушки, что приводило к уменьшению частоты сердечных сокращений*. Затем жидкость, находящуюся вокруг этого сердца, Лёви собирал и наносил на сердце другой лягушки — и оно тоже замедлялось. Это доказывало существование некоего вещества, передающего сигнал от одних нервных клеток другим. Загадочное вещество Лёви назвал vagusstoff («вещество блуждающего нерва»). Сейчас мы знаем его под названием ацетилхолин. Вопросом химической синаптической передачи занимался и британец Генри Дейл, который обнаружил ацетилхолин еще раньше Лёви. В 1936 году оба ученых получили Нобелевскую премию по физиологии и медицине «за открытия, связанные с химической передачей нервных импульсов».
* — О том, как сокращается наше сердце — об автоматизме, дирижирующих пейсмейкерах и даже смешных каналах, — читайте в обзоре «Метроном: как руководить разрядами?» [4]. — Ред.
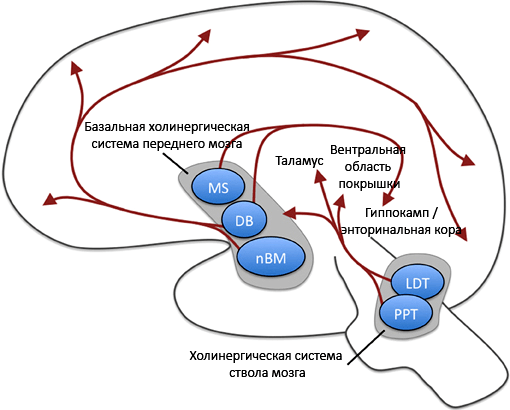
Ацетилхолин (рис. 2) производится в нервных клетках из холина и ацетилкофермента-А (ацетил-КоА). За разрушение ацетилхолина отвечает фермент ацетилхолинэстераза, находящийся в синаптической щели; об этом ферменте будет подробный разговор позже. План строения ацетилхолинергической системы головного мозга схож со строением других нейромедиаторных систем (рис. 3). В стволе мозга существует ряд структур, выделяющих ацетилхолин, который поступает по аксонам в базальные ганглии головного мозга. Там есть свои ацетилхолиновые нейроны, чьи отростки расходятся широко по коре и проникают в гиппокамп.
Рисунок 3. Ацетилхолиновая система мозга. Мы видим, что в глубоких отделах головного мозга находятся скопления нервных клеток (в переднем мозге и стволе), которые посылают свои отростки в различные отделы коры и подкорковых областей. В конечных пунктах из нейронных окончаний выделяется ацетилхолин. Местные эффекты нейромедиатора различаются в зависимости от типа рецептора и его расположения. MS — медиальное ядро перегородки, DB — диагональная связка Брока, nBM — базальное магноцеллюлярное ядро (ядро Мейтнера); PPT — педункулопонтийное тегментальное ядро, LDT — латеральное дорсальное тегментальное ядро (оба ядра — в ретикулярной формации ствола мозга). Рисунок из [8], адаптирован.
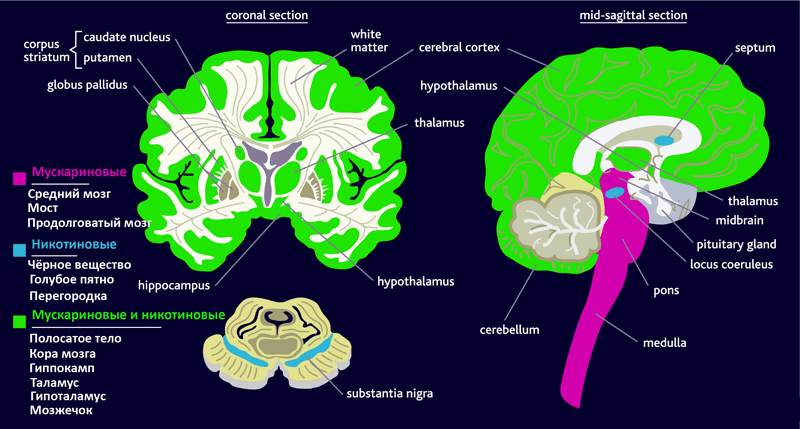
Рецепторы ацетилхолина делятся на две группы — мускариновые и никотиновые. Стимуляция мускариновых рецепторов приводит к изменению метаболизма в клетке через систему G-белков* (метаботропные рецепторы), а воздействие на никотиновые — к изменению мембранного потенциала (ионотропные рецепторы). Это происходит благодаря тому, что никотиновые рецепторы связаны с натриевыми каналами на поверхности клеток. Экспрессия рецепторов различается в разных участках нервной системы (рис. 4).
* — О пространственных структурах нескольких представителей громадного семейства GPCR-рецепторов — мембранных рецепторов, действующих через активацию G-белка, — доступно рассказано в статьях: «Рецепторы в активной форме» (об активной форме родопсина) [5], «Структуры рецепторов GPCR „в копилку“» (о дофаминовом и хемокиновом рецепторах) [6], «Рецептор медиатора настроения» (о двух серотониновых рецепторах) [7]. — Ред.
Рисунок 4. Распределение мускариновых и никотиновых рецепторов в головном мозге человека. Рисунок с сайта www.cnsforum.com, адаптирован.
Медиатор памяти и обучения
Ацетилхолиновая система головного мозга напрямую связана с таким явлением как синаптическая пластичность — способность синапса усиливать или снижать выделение нейромедиатора в ответ на увеличение или уменьшение его активности. Синаптическая пластичность является важным процессом для памяти и обучения, поэтому ученые стремились обнаружить его в отделе мозга, отвечающем за эти функции — в гиппокампе. Большое количество ацетилхолиновых нейронов направляет свои отростки в гиппокамп, и там они влияют на высвобождение нейромедиаторов из других нервных клеток [8]. Способ осуществления этого процесса довольно простой: на теле нейрона и его пресинаптической части расположены различные никотиновые рецепторы (в основном, α7— и β2-типов). Их активация будет приводить к тому, что прохождение сигнала по иннервируемой клетке упростится, и он с большей вероятностью перейдет на следующий нейрон. Наибольшее влияние такого рода испытывают на себе ГАМК-ергические нейроны — нервные клетки, чьим нейромедиатором является γ-аминомасляная кислота [9].
ГАМК-ергические нейроны являются важной частью системы, генерирующей электрические ритмы нашего мозга. Эти ритмы можно записать и изучить при помощи электроэнцефалограммы — широкодоступного метода исследования в нейрофизиологии. Ритмы различной частоты обозначаются греческими буквами: 8–14 Гц — альфа-ритм, 14–30 Гц — бета-ритм и так далее. Использование стимуляторов ацетилхолиновых рецепторов приводит к тому, что в мозге возникает тета- (0,4–14 Гц) и гамма-ритм (30–80 Гц). Эти ритмы, как правило, сопровождают активную когнитивную деятельность. Стимуляция постсинаптических мускариновых ацетилхолиновых рецепторов, расположенных на нейронах гиппокампа (центра памяти) и префронтальной коры (центр сложных форм поведения), приводит к возбуждению этих клеток и генерации упомянутых выше ритмов. Они сопровождают различную когнитивную деятельность — например, выстраивание временнόй последовательности событий [10].
Гиппокамп и префронтальная кора играют важную роль в обучении. С точки зрения рефлексов любое обучение происходит двумя путями. Допустим, вы экспериментатор, и объектом вашего эксперимента является мышь. В первом случае в ее клетке зажигается свет (условный стимул), и грызун получает кусочек сыра (безусловный стимул) еще до того, как свет погаснет. Формирующийся рефлекс можно назвать задержанным. Во втором случае свет также зажигается, но мышь получает лакомство через некоторое время после выключения лампочки. Этот тип рефлекса называется следовым. Рефлексы второго типа зависят от осознанности стимулов больше, чем рефлексы первого типа. Угнетение активности ацетилхолинергической системы приводит к тому, что у животных не вырабатываются следовые рефлексы, хотя с задержанными проблем не возникает [11].
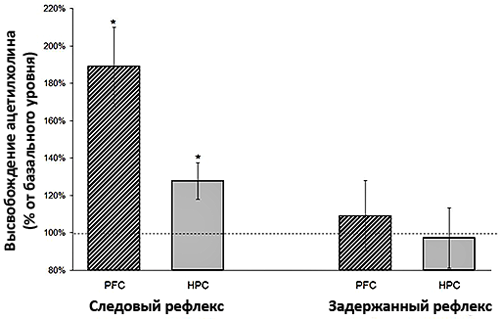
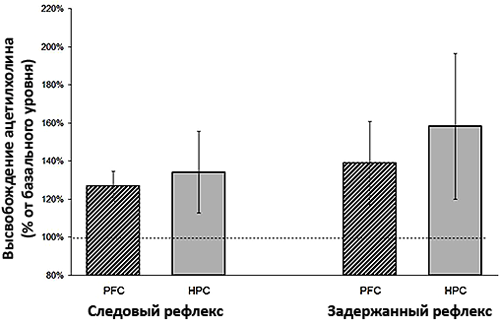
При сравнении секреции ацетилхолина в мозге крыс, у которых вырабатывали оба вида рефлексов, были получены интересные данные [12]. У крыс, которые успешно справлялись с усвоением временнόй связи между условным и безусловным стимулом, обнаруживалось значительное увеличение уровня ацетилхолина в медиальной префронтальной коре (рис. 5) по сравнению с гиппокампом. Особенно существенной была разница в уровнях ацетилхолина у крыс, которые выработали следовый рефлекс. Те грызуны, которые не справились с обеими задачами, обнаруживали приблизительно равные уровни нейромедиатора в исследуемых отделах мозга (рис. 6). Исходя из этого можно заключить, что непосредственно в обучении бóльшую роль играет префронтальная кора, а гиппокамп сохраняет полученные знания.
Рисунок 5. Выброс ацетилхолина в гиппокампе (HPC) и префронтальной коре (PFC) крыс при успешной выработке рефлексов. Максимальный уровень ацетилхолина наблюдается в префронтальной коре при выработке следового рефлекса. Рисунок из [12].
Рисунок 6. Выброс ацетилхолина в гиппокампе (HPC) и префронтальной коре (PFC) крыс в случае «провала» в обучении. Регистрируется почти одинаковое содержание ацетилхолина в двух зонах вне зависимости от рефлекса. Рисунок из [12].
Рецепторы внимания
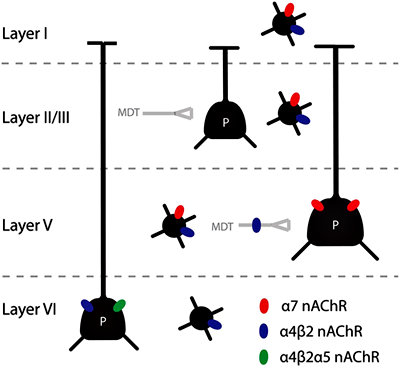
Рисунок 7. Многообразие ацетилхолиновых рецепторов (nAChR) в слоях префронтальной коры головного мозга. Рисунок из [15].
Для обучения важен не только интеллект или объем памяти, но и внимание. Без внимания даже самый успешный ученик будет двоечником. Ацетилхолин участвует также в процессах, регулирующих внимание.
Внимание — сфокусированное восприятие или обдумывание проблемы — сопровождается повышенной активностью в префронтальной коре. Ацетилхолиновые волокна направляются в лобную кору из глубоких отделов мозга. В связи с тем, что часто нам требуется быстрое переключение внимания, вполне логично, что в регуляции внимания участвуют никотиновые (ионотропные) рецепторы ацетилхолина, а не мускариновые, которые вызывают более медленные и преимущественно структурные изменения в нейронах. Повреждение ацетилхолиновых структур глубоких отделов мозга снижает активность медиальной префронтальной коры и нарушает внимание [13]. Кроме того, взаимодействие глубоких ацетилхолиновых структур с префронтальной корой не ограничивается восходящими сигналами. Нейроны лобной коры также отправляют свои сигналы в нижележащие отделы, что позволяет создавать саморегулирующуюся систему поддержания внимания [14]. Внимание поддерживается за счет воздействия ацетилхолина на пресинаптические и постсинаптические рецепторы (рис. 7).
При разговоре о никотиновых рецепторах и внимании возникает вопрос об улучшении когнитивных функций при помощи курения, то есть введения дополнительной дозы никотина, пусть и в виде сигаретного дыма [16]. Ситуация здесь довольно ясная, и результаты не дают курильщикам лишнего аргумента в пользу их пагубного пристрастия. Никотин, пришедший извне, нарушает нормальное развитие мозга, что может приводить к расстройствам внимания (на долгие годы) [17]. Если сравнивать курильщиков и некурящих, то у первых показатели внимания хуже, чем у их оппонентов [18]. Улучшение внимания у курильщиков возникает в случае выкуривания сигареты после долгого воздержания, когда их плохое настроение и когнитивные проблемы улетучиваются вместе с дымом.
Лекарство для памяти
Если в норме ацетилхолинергическая система нашего мозга отвечает за память, внимание и обучение, то заболевания, при которых нарушается этот тип трансмиссии в нашем мозге, должны проявляться соответствующими симптомами: потерей памяти, снижением внимания и способности учиться новому. Здесь надо сразу оговориться, что в ходе нормального старения у подавляющего большинства людей снижается и способность к запоминанию нового, и живость ума в целом. Если эти нарушения выражены настолько, что мешают пожилому человеку заниматься повседневной деятельностью и удовлетворять свои повседневные потребности (обслуживать себя), то тогда врачи могут заподозрить деменцию. Если вы хотите узнать о деменции больше, то рекомендую начать с изучения информационного бюллетеня ВОЗ, посвященного этой патологии [19].
Строго говоря, деменция — это не отдельное заболевание, а синдром, встречающийся при ряде заболеваний. Одной из самых частых болезней, которая приводит к деменции, является болезнь Альцгеймера. Считается, что при болезни Альцгеймера в нервных клетках накапливается патологический белок β-амилоид [20, 21], который и нарушает деятельность нервных клеток, что в итоге приводит к их гибели. Кроме этой теории существует ряд других, которые имеют свои доказательства. Вполне вероятно, что при болезни Альцгеймера в клетках головного мозга разных пациентов происходят неодинаковые процессы, но приводят они к схожим симптомам. Однако β-амилоид интересен тем, что он может подавлять эффект, производимый ацетилхолином на клетку через никотиновые рецепторы [22]. Если у нас получится интенсифицировать ацетилхолинергическую передачу, то мы можем уменьшить проявления болезни и продлить самостоятельную жизнь человеку с деменцией.
К препаратам, используемым при деменции, относятся ингибиторы ацетилхолинэстеразы (АХЭ) — фермента, разрушающего ацетилхолин в синаптической щели. Применение ингибиторов АХЭ приводит к повышению содержания ацетилхолина в межнейронном пространстве и улучшению передачи сигнала. Исследование эффективности ингибиторов АХЭ при болезни Альцгеймера определило, что они способны уменьшить симптомы заболевания [23] и замедлить его прогрессирование [24]. Три наиболее применяемых препарата из этой группы — ривастигмин, галантамин и донепезил — сравнимы по эффективности и безопасности. Также существует небольшой, но успешный опыт применения ингибиторов АХЭ в лечении музыкальных галлюцинаций у пожилых людей [25].
При помощи ацетилхолина наш мозг обучается, фокусирует внимание на разных объектах и явлениях окружающего мира. Наша память «работает» на ацетилхолине, а его дефицит можно компенсировать при помощи лекарств. Надеюсь, что вам понравилось знакомство с ацетилхолином.
Нейромедиаторы, часть 2
Аденозин, ацетилхолин, глутамат и гамма-аминомасляная кислота
Первую часть рассказа о нейромедиаторах «Атлас» посвятил молодежным дофамину, норадреналину и серотонину. Во втором посте речь пойдет о менее известных медиаторах, которые выполняют важную невидимую работу: стимулируют и тормозят другие нейромедиаторы, помогают нам учиться и запоминать.
Ацетилхолин
Это первый нейромедиатор, который открыли ученые. Он отвечает за передачу импульсов двигательными нейронами – а значит, за все движения человека. В центральной нервной системе нейромедиатор берет на себя стабилизирующие функции: выводит мозг из состояния покоя, когда необходимо действовать, и наоборот, тормозит передачу импульсов, когда необходимо сосредоточиться. В этом ему помогают два типа рецепторов – ускоряющие никотиновые и тормозящие мускариновые.
Ацетилхолин играет важную роль в процессе обучения и формирования памяти. Для этого требуется как способность фокусировать внимание (и тормозить передачу отвлекающих импульсов), так и способность переключаться с одного предмета на другой (и ускорять реакцию). Активная работа мозга, например, при подготовке к экзамену или годовому отчету, приводит к повышению уровня ацетилхолина. Если мозг долгое время бездействует, специальный фермент ацетилхолинэстераза разрушает медиатор, и действие ацетилхолина слабеет. Идеальный для учебы, ацетилхолин будет плохим помощником в стрессовых ситуациях: это медиатор размышления, но не решительных действий.
Переизбыток ацетилхолина в организме вызывает спазм всех мышц, судороги и остановку дыхания – именно на такой эффект рассчитаны некоторые нервно-паралитические газы. Недостаток ацетилхолина приводит к развитию болезни Альцгеймера и других видов старческой деменции. В качестве поддерживающей терапии пациентам назначают препарат, блокирующий разрушение ацетилхолина – ингибитор ацетилхолинэстеразы.
Ген CHRNA3 кодирует никотиновый рецептор ацетилхолина, на который может воздействовать никотин. На первом этапе вещество действует на симпатическую систему организма, которая отвечает за спазм гладкой мускулатуры и сокращение сосудов. Поэтому у начинающих курильщиков сигареты вызывают скорее тошноту и бледность кожи, чем восторг. Но со временем никотин достигает клеток головного мозга и активизирует рецепторы ацетилхолина. Так как этим занимается и никотин, и ацетилхолин одновременно, мозг пытается скорректировать «двойную подачу», и через некоторое время нейроны головного мозга сокращают нормальное производство ацетилхолина. С этого момента никотин будет нужен курильщику по каждому поводу – с утра чтобы взбодриться, после совещания наоборот, чтобы успокоиться, после обеда – чтобы хоть немного подумать о вечном.
Полиморфизм гена CHRNA3 влияет на скорость формирования никотиновой зависимости и, как следствие, на риск развития рака лёгких, вызванного курением.
Все химические реакции в организме требуют затраты энергии. В качестве валюты в этом процессе используется молекула аденина с несколькими основаниями фосфорной кислоты. Сразу после «зарплаты» у вас на карточке окажется «триста рублей» – молекула аденозинтрифосфат с тремя остатками фосфорной кислоты. На каждую транзакцию уходит по сто рублей, соответственно, после первой «покупки» на счету останется всего двести рублей (аденозиндифосфат), после второй – сто рублей (аденозинмонофосфат), после третьей – ноль рублей.
Купюра в ноль рублей – и есть аденозин. Как нейромедиатор он отвечает за чувство усталости и засыпание. Во время сна купюрам в ноль-ноль рублей дорисовывают троечки, аденозин трансформируется в аденозинтрифосфат, и мы с новыми силами готовы вернуться к работе.
Есть способ обмануть «банковскую систему»: заблокировать рецепторы аденозина и уйти в кредит. Именно этим и занимается кофеин – позволяет игнорировать усталость и продолжать работать. При этом он не приносит настоящей энергии, а только дает тратить деньги, как если у вас всё ещё есть триста рублей. Как и за любой кредит, за перерасход приходится расплачиваться – большей усталостью, заторможенностью внимания, привыканием. Тем не менее, кофеиносодержащие кофе, чай и шоколад – самый популярный стимулятор в мире.
Всего известно четыре вида рецепторов аденозина, которые активируются и блокируются аденозином. Ген ADORA2A кодирует рецепторы аденозина второго типа, которые участвуют в активации противовоспалительных процессов, формировании иммунного ответа, регуляции боли и сна. От работы этого рецептора зависит скорость реакции организма на ранение и травму.
Глутаминовая кислота в форме глутамата – пищевая аминокислота, которая содержится в продуктах животного происхождения. Вкусовые рецепторы воспринимают глутамат как индикатор белковой пищи – а значит питательной и полезной – и оставляют заметку, что было вкусно, и надо повторить. В двадцатом веке японские ученые выяснили принцип восприятия этого вкуса (они назвали его «умами» – вкусный), и со временем глутамат натрия стал популярной пищевой добавкой. Именно благодаря ему иногда сложно устоять перед соблазном съесть лапшу доширак. Как пищевая добавка глутамат не влияет напрямую на работу нейронов, поэтому его «передозировка» в худшем случае обойдется головной болью.
Глутамат – это не только пищевая аминокислота, но и важный нейромедиатор, рецепторы которого есть у 40% нейронов головного мозга. Он не имеет собственной «смысловой нагрузки», а только ускоряет передачу сигнала другими рецепторами – дофаминовыми, норадреналиновыми, серотониновыми и т.д. Эта функция позволяет глутамату формировать синаптическую пластичность – способность синапсов регулировать свою активность в зависимости от реакции постсинаптических рецепторов. Этот механизм лежит в основе процесса обучения и работы памяти.
Снижение активности глутамата приводит к вялости и апатии. Переизбыток – к «перенапряжению» нервных клеток и даже их гибели, как если бы на электрическую сеть дали большую нагрузку, чем она способна выдержать. «Перегорание» нейронов – эксайтотоксичность – наблюдается после приступов эпилепсии и при нейродегенеративных заболеваниях.
Две группы генов кодируют белки-транспортеры глутамата. Гены группы EAAT отвечают за натрий-зависимые белки – те самые, которые участвуют в процессе запоминания. Мутации в генах этой группы повышают риск инсульта, болезни Альцгеймера, болезни Гентингтона, бокового амиотрофического склероза. Мутации в генах везикулярных белков-транспортеров группы VGLUT ассоциированы с риском шизофрении.
У каждой инь есть свой ян, и у глутамата есть вечный его противник, с которым он тем не менее неразрывно связан. Речь идет о главном тормозном нейромедиаторе – гамма-аминомасляной кислоте (ГАМК или GABA). Так же как и глутамат, ГАМК не вносит новых цветов в палитру мозговой активности, а только регулирует активность других нейронов. Так же как и глутамат, ГАМК охватил сетью своих рецепторов около 40% нейронов головного мозга. И глутамат, и ГАМК синтезируются из глутаминовой кислоты и по существу являются продолжением друг друга.
Для описания эффекта ГАМК идеально подходит поговорка «тише едешь – дальше будешь»: тормозящий эффект медиатора позволяет лучше сосредоточиться. ГАМК снижает активность самых разных нейронов, в том числе связанных с чувством страха или тревоги и отвлекающих от основной задачи. Высокая концентрация ГАМК обеспечивает спокойствие и собранность. Снижение концентрации ГАМК и нарушение баланса в вечном сопротивлении с глутаматом приводит к синдрому дефицита внимания (СДВГ). Для повышения уровня ГАМК хорошо подходят прогулки, йога, медитации, для снижения – большинство стимуляторов.
У гамма-аминомасляной кислоты два типа рецепторов – быстрого реагирования GABA-A и более медленного действия GABA-B. Ген GABRG2 кодирует белок рецептора GABA-A, который резко снижает скорость передачи импульсов в головном мозге. Мутации в гене связаны с эпилепсией и фебрильными судорогами, которые могут возникать при высокой температуре.
Если дофамин, серотонин и норадреналин – голливудские актеры большой нейронной киноиндустрии, то герои второй части рассказа о нейромедиаторах скорее работают за кадром. Но без их незаметного вклада большое кино было бы совсем другим.
В следующей части «Атлас» расскажет о пептидах и опиоидиах – эта тема требует отдельного разговора.