Ацикловир чем вреден в будущем
Итак, начнем с того, что герпес возникает не только на губе, вирусные заболевания поражают различные участки человеческого тела. Поэтому Ацикловир реализуется в следующих формах, у каждой из которых свои показания к приему: крем и мазь для местного применения 5%, таблетки (200 мг, 400 мг, 500 мг), раствор для внутривенных инъекций Лиофилизат 250 мг, глазная мазь 3%.
Показания к применению
Ацикловир показан при следующих заболеваниях:
Противопоказания
Так как Ацикловир лекарственное средство, то существуют и противопоказания:
Курс Ацикловира, который назначил врач, прерывать нельзя, даже если симптомы заболевания исчезли.
Дозы и способ применения
Дозировка лекарства Ацикловир
Дозировка
Дозировка зависит от болезни и тяжести ее протекания.
Способ применения Ацикловира
Способ применения Ацикловира зависит от формы выпуска. Таблетки глотают, не разжевывая, вне зависимости от приема пищи, обильно запивая водой. Мазь и крем с помощью ватной палочки наносят на пораженные участки тонким слоем 5 раз в день (раз в 4 часа плюс ночной перерыв). Лиофилизат (внутривенно) сначала нужно развести до нужной концентрации. Глазную мазь закладывают полоской 1 см за нижнее веко 5 раз в день через 4 часа.
Мазь и крем Ацикловир предназначены для наружного использования, а нанесение на поверхности слизистых оболочек (носовая и ротовая полости) не рекомендуется, но не противопоказано. Необходимо помнить о некоторых правилах нанесения лекарственных средств на слизистую и проконсультироваться с врачом!
Если же мазь все равно нужно нанести, то перед применением Ацикловира ротовую или носовую полости очищают. Желательно промыть их солевым раствором или другим средством для промывания или полоскания, а потом промокнуть поверхность марлевым тампоном или ватным шариком. Затем точечно нанести небольшое количество крема или мази. Возможно появится жжение и боль. Если они проходят, то нанесите остатки крема или мази. Если же боль усиливается, то это аллергическая реакция, и применение средства необходимо прекратить. Помните о том, что через ротовую полость крем и мазь будут попадать в пищевод, при небольших количествах это не опасно, но лучше воспользоваться другой формой Ацикловира.
Можно ли ветрянку мазать препаратом Ацикловир?
С помощью Ацикловира можно бороться с ветрянкой
В инструкции Ацикловира среди показаний к применению фигурирует ветряная оспа (varicella zoster), или попросту ветрянка. Ацикловир активно борется с ней, но все зависит от иммунитета конкретного человека и характера протекания болезни. При средней и тяжелой формах ветрянки Ацикловир назначают как в виде таблеток, так и виде крема или мази. Взрослым препарат назначается на ранней стадии болезни, а детям до 12 лет — только при непереносимости болезненного состояния или при тяжелом течении болезни. Схема приема следующая: взрослым показано 1-2 таблетки по 400 мг. каждые 4-е часа 3-5 раз в сутки. Детская доза составляет половину от взрослой, а временной интервал между приемом увеличивается на 1 час, но не более 4 раз в сутки. Крем или мазь наносятся точечно, на места поражения до 5 раз в день. Если при ветряной оспе поражены слизистые глаз, в этом случае используется глазная мазь, закладываемая за нижнее веко до 5 раз в сутки. Ацикловир применяют на протяжении 5 дней, но лечащий врач может внести корректировки в терапию.
Можно ли Ацикловир при простуде?
Ацикловир можно назначать при ОРВИ
Ацикловир успешно борется с вирусами герпеса, но иногда терапевт назначает Ацикловир при ОРВИ. Почему? Не секрет, что при ОРВИ и простуде в целом иммунитет ослаблен, и это благодатная почва для проявления герпеса, который на фоне все того же ОРВИ ситуацию не облегчает. Хоть Ацикловир малоэффективен в борьбе с вирусами, которые вызывают респираторные заболевания, однако он используется как профилактическое средство, предупреждающее развитие герпеса.
Ацикловир при беременности
Иммунитет беременной женщины ослаблен и может быть подвержен гепертическим инфекциям. Поэтому будущие мамы и те, кто проходит период лактации задаются вопросом “А можно ли Ацикловир при беременности?” Согласно инструкции применение ацикловира в период беременности допустимо, но с осторожностью. Причем эта формулировка означает, что применение возможно, во-первых, только по назначению врача, во-вторых, только, когда терапевтический эффект больше риска. Это касается всех лекарственных форм. Что касается периода лактации, то препарат проникает в грудное молоко. Поэтому сначала консультация врача, а потом прием препарата. При негативных реакциях необходимо изменить терапию, либо на время прекратить ГВ.
Взаимодействие с другими лекарственными средствами и алкоголем
Ацикловир и алкоголь
Когда доктор назначает тот или иной препарат, возникает вопрос о совместимости не только с другими лекарствами (об этом ниже), но и с алкоголем. Ведь часто простуда выскакивает не вовремя, а в планах посещение мероприятия, где будут крепкие напитки. Как поступить в такой ситуации? Несмотря на отсутствие прямых противопоказаний, спиртное и лекарство несовместимы.
Не рекомендуется принимать Ацикловир с алкоголем
Во-первых, алкоголь, подавляя активность лейкоцитов и выработку антител, снижает защитные силы организма. Во-вторых, любой препарат нагружает печень и почки, и алкоголь обладает схожим эффектом. И когда печень не справляется с переработкой, происходит выброс ферментов, которые подавляют действие Ацикловира. То есть эффект от иммуномодулятора будет равен нулю. Также, это способно спровоцировать интоксикацию организма и увеличить риск появления побочных эффектов таких, как тошнота, рвота; судороги, нарушения сознания; тремор и галлюцинации; аллергия (зуд, высыпания на коже, крапивница, ангионевротические виды отечности); жидкий стул; анемия; одышка, болевой синдром в грудине, учащение сердцебиения; расстройство глотательных и дыхательных функций; цефалгия, головокружение, сонливость.
Если после выпитого вас мучает похмельный синдром, это не самое подходящее время для приема Ацикловира. При возникновении похмелья организм уже испытывает стресс. Прием препарата может спровоцировать ухудшение общего состояния.
Ацикловир и антибиотики
Может так получиться, что Ацикловир принимается в то же время, что и антибиотики. При лечении вирусных заболеваний одновременный прием антибиотиков не рекомендуется, так как они попросту будут мешать друг другу. То есть лечение будет малоэффективно как со стороны Ацикловира, так и со стороны другого препарата. Единовременное применение медикаментов не ускорит выздоровление пациента, да и печень не скажет вам “спасибо”, так как на нее создается дополнительная нагрузка, что может привести к негативным последствиям. В исключительных случаях, по назначению врача, единовременный прием возможен, но он сопряжен с рисками. Обязательно проконсультируйтесь с лечащим врачом.
Аналоги
Наравне с Ацикловиром пациентам с вирусными заболеваниями назначают Ремантадин. Можно ли одновременно принимать Ацикловир и Ремантадин? Что лучше? Ремантадин препятствует размножению клеток вируса, укрепляет иммунитет, а также используется в качестве профилактического средства во время эпидемий гриппа.
Показаниями к приему Ремантадин являются:
Применяться препарат может детьми от 7-ми лет и более.
Основное же предназначение Ацикловира – лечение герпеса, ветряной оспы и противовирусная терапия. Встраиваясь в структуру ДНК вирусов, Ацикловир не дает им размножаться и развиваться. При необходимости лекарство может быть назначено детям.
Принимать одновременно Ремантадин и Ацикловир не следует, так как оба этих лекарства схожи. Точно определиться с необходимым препаратом и рассчитать дозировку может исключительно лечащий врач.
Профилактический прием
Нередко возникает вопрос, как предотвратить такую неприятную ситуацию, как проявление герпеса. Какой должна быть профилактика? Рекомендации просты:
Актуальные вопросы тяжелой герпетической инфекции у взрослых
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная. Многие вопросы патогенеза и терапии тяжелого и крайне-тяжелого течения герпесвирусной инфекции по-прежнему не решены.
Вид ВПГ относится к семейству Herpesviridae, подсемейству L-Herpesviridae, виду ВПГ. Различают два основных типа вируса — ВПГ 1 и ВПГ 2. Инфицирование возможно как одним, так и двумя типами возбудителя. ВПГ способен внедряться в различные клетки организма человека: в клетки кожи, слизистых оболочек урогенитального и желудочно-кишечного трактов (ЖКТ), дыхательных путей, центральной и периферической нервной системы, печени, эндотелия сосудов, а также в клетки крови — лимфоциты и др. [1]. Место постоянного обитания (пожизненного персистирования) ВПГ — паравертебральные сенсорные ганглии. ВПГ передается прямым контактным путем, возможна передача возбудителя контактно-бытовым и вертикальным путем (от матери к плоду), а также трансфузионным и парентеральным путями через инструменты при оперативных вмешательствах, стоматологических процедурах и т. д.
Как известно, большинство людей инфицированы ВПГ. Первичный иммунный ответ на инфекцию протекает латентно или с герпетическими высыпаниями с местной и общей воспалительной реакцией. У лиц с нормальным иммунным ответом размножение (репликация) ВПГ находится под иммунологическим контролем, и рецидивы бывают крайне редко или не возникают в течение всей жизни. В противовирусной защите организма участвуют факторы неспецифической защиты, уничтожающие или блокирующие вирусы: макрофаги и другие клетки-продуценты интерферонов (ИФН) α, β и γ, ряд интерлейкинов (ИЛ) (фактор некроза опухоли (ФНО), ИЛ-6 и др.), естественные киллеры и факторы, формирующие специфический иммунный ответ против конкретного вируса: цитотоксические Т-лимфоциты (ЦТЛ) (CD 8+ Т-лимфоциты) и В-лимфоциты, ответственные за продукцию специфических антител, блокирующих репликацию вируса и расположенные вне клетки вирусы. Для адекватного функционирования этих клеток и поддержания иммунного ответа необходима соответствующая продукция ИФН и ИЛ.
Под влиянием различных экзогенных и эндогенных факторов, повреждающих иммунную систему, возможно ослабление контроля над репликацией вируса и соответственно развитие рецидива. Рецидив ВПГ-инфекции могут спровоцировать другие инфекционные заболевания, переохлаждение, чрезмерная инсоляция, психические или физические стрессы, интоксикации различного генеза, в том числе употребление алкоголя, циклические изменения гормонального статуса (менструации), особенно при дисбалансе уровня гормонов у женщин, резкая смена климатических поясов и др.
При длительной хронической инфекции вирусы оказывают многостороннее неблагоприятное действие на иммунную систему человека. ВПГ прямо повреждают клетки иммунной системы (лимфоциты, макрофаги и естественные киллеры). Синтезируя белки-супрессоры и химерные белки, вирусы угнетают многие реакции иммунитета: ВПГ могут блокировать действие ИФН, нарушать распознавания инфицированных клеток и другие защитные реакции. Кроме того, высокая мутационная активность вирусного генома также способствует ускользанию вируса от иммунологического контроля.
Хроническая, часто рецидивирующая ВПГ-инфекция может провоцировать развитие аутоиммунных состояний (антифосфолипидный синдром, аутоиммунный тиреоидит, аутоиммунные васкулиты и др.). Кроме того, при интеграции ВПГ в генетический аппарат клеток возможна неопластическая трансформация клеток. Так, ВПГ является одним из факторов повышенного риска развития рака тела и шейки матки и других онкологических заболеваний. Также ВПГ-инфекция является одной из ведущих причин самопроизвольных абортов, преждевременных родов, рождения детей с патологией центральной нервной системы и внутренних органов. ВПГИ ассоциирована со многими «болезнями цивилизации» — атеросклерозом, ишемической болезнью сердца у лиц моложе 50 лет и др. Тяжелое течение ВПГИ может быть маркером онкологических заболеваний и СПИДа [7].
В зависимости от числа и выраженности рецидивов, выделяют легкое, среднетяжелое и тяжелое течение болезни (табл. 1).
При тяжелом течении ВПГ-инфекции возможно одновременное появление нескольких очагов поражения (например, в области половых органов, губ, крыльев носа), а также последовательное возникновение высыпаний разной локализации (один рецидив на фоне другого), продолжительность обострения при этом может достигать 16–20 дней. В месте высыпания больные ощущают жар, жжение, боль, напряжение и/или зуд кожи. На инфильтрированной коже появляется группа пузырьков, заполненных прозрачным содержимым. Пузырьки могут сливаться в сплошной многокамерный элемент. Прозрачное их содержимое затем мутнеет. Пузырьки в дальнейшем вскрываются, образуя мелкие эрозии, или подсыхают и превращаются в корочки. Возможно наслоение вторичной бактериальной инфекции. При рецидивах ВПГ часто поражает одни и те же участки кожи. Как правило, при тяжелом течении инфекции значительно ухудшается физическое и психическое состояние больных. У части пациентов в период рецидива увеличиваются или появляются слабость, лихорадка, озноб, миалгии, цефалгии, артралгии, раздражительность, нарушение сна, эмоциональная лабильность, также могут развиваться тяжелые депрессивные состояния, требующие медикаментозной коррекции. По данным органов здравоохранения США, ВПГ-инфекция аногенитальной локализации является примерно в 10% случаев причиной депрессий и суицидов. Тяжелое течение генитальной формы ВПГ-инфекции с частыми рецидивами приводит к нарушению нормальной половой функции пациента, болезнь нередко создает конфликтные ситуации в семье, на работе. Лечение больных с тяжелым течением ВПГ-инфекции представляет собой сложную задачу и должно включать как медикаментозную терапию, так и психологическую адаптацию пациента.
У больных с тяжелой ВПГ-инфекцией в большинстве случаев не наблюдается стойкого и значимого клинического эффекта в ответ на эпизодические курсы комбинированной терапии (противовирусные и иммунотропные средства, общеукрепляющие препараты). Как правило, такие больные меняют много лечебных учреждений в поисках адекватной помощи.
С течением заболевания появляется много побочных реакций на медикаменты или их непереносимость, в ряде случаев развивается устойчивость ВПГ к ацикловиру, ИФН a, другим средствам. Иммуностимуляторы, используемые эмпирически, могут приносить облегчение в период их приема, но во многих случаях они оказываются неэффективными и даже ухудшают клиническое течение болезни. Усугубляются проявления вторичного иммунодефицита, присоединяются другие инфекции, субдепрессивные состояния переходят в стойкие нарушения психики, теряется вера больных в выздоровление, в возможность современной медицины им помочь.
Для разработки современных подходов к лечению и контролю над ВПГ-инфекцией и более углубленного понимания патогенеза заболевания нами было изучено состояние различных звеньев противовирусной защиты и системы цитокинов у больных с тяжелым и крайне тяжелым течением ВПГ-инфекции аногенитальной и лабиальной локализации, а также степень инфицированности (системности заболевания) и частота сочетания с другими герпесвирусными инфекциями.
Обследовано 102 больных, страдающих тяжелой ВПГ-инфекцией более 2 лет (28 мужчин и 74 женщины, средний возраст — 34 ± 1,5 года) и имеющих частоту рецидивов более шести в год.
При этом у 60 больных наблюдалось от 6 до 11 рецидивов ВПГ-инфекции в год, а у 42 больных — от 12 до 20 рецидивов. У большинства пациентов преобладала аногенительная или смешанная локализация герпеса. Средняя длительность тяжелого течения заболевания составила 9,3 ± 1,2 года. Группу контроля составили 32 практически здоровых добровольца (14 мужчин и 18 женщин, средний возраст — 32 ± 1,6 года). Анализ ряда изучаемых параметров включал результаты обследования пациентов с легким течением заболевания (36 человек — 10 мужчин, 26 женщин, средний возраст — 33,4 ± 2,1 года, с частотой рецидивов 2,9 ± 0,8 в год). При рецидивах жалобы больных были характерными. Часто встречались депрессия, раздражительность, снижение памяти и другие нарушения физического и психического состояния и познавательных функций.
У многих больных в анамнезе были указания на повторные курсы противовирусной и/или иммунотропной терапии, оказывавшей неоднозначное влияние: или кратковременное положительное влияние на течение ВПГ-инфекции, или ухудшение и развитие рецидива на фоне или после отмены иммунокоррекции. Такие анамнестические данные отражают тяжесть иммунной недостаточности и неадекватность проводимой эмпирической терапии без оценки иммунного статуса и индивидуального подбора иммунокорректоров, а также восстановительной терапии — иммунореабилитации [5].
При обследовании больных с тяжелым течением ВПГ-инфекции выявлялись многие маркеры вторичного иммунодефицита в виде хронических инфекционно-воспалительных заболеваний различной локализации, со смешанным характером микрофлоры и в большинстве случаев ее устойчивостью к повторным курсам антибиотикотерапии. Из 102 больных хронической ВПГ-инфекцией тяжелого течения выявлены:
Эти данные свидетельствуют о необходимости комплексного подхода к лечению ВПГ-инфекции тяжелого течения с учетом осложнений вторичного иммунодефицита.
Кроме того, проводили ПЦР-исследование биологических материалов на наличие ДНК ВПГ 1 и 2 типа и других вирусов герпес-группы: цитомегаловируса, вируса герпеса человека (ВГЧ) 6 типа, вируса Эпштейна–Барр. Используемые нами программы амплификации позволяли выявлять ДНК вирусов на уровне, соответствующем активной их репликации. Наличие активной репликации вирусов подтверждали полуколичественным ПЦР-исследованием и серологическими тестами.
В результате исследования у больных с тяжелым течением ВПГ-инфекции обнаружены лабораторные признаки вторичного иммунодефицита.
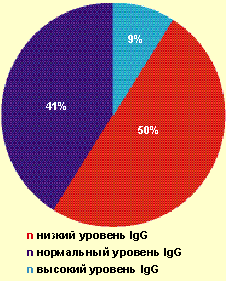 |
| Рисунок 1. Частота выявления различных значений IgG у больных с тяжелым течением ВПГ-инфекции |
Так, у большинства пациентов (91%) отсутствовало адекватное повышение продукции IgG в ответ на рецидив ВПГ-инфекции (рис. 1). При частоте рецидивов ВПГ-инфекции 6–11 рецидивов в год низкий уровень IgG выявлялся у 25% больных, при частоте — 12–20 рецидивов в месяц — уже у 64,3% больных. Более чем у 70% больных был повышен уровень ЦИК в 1,5–2,0 раза от показателей нормы. Известно, что длительная циркуляция ЦИК может приводить к отложению их на эндотелии сосудов и служить одним из факторов формирования аутоиммунной патологии.
У большинства больных с ВПГ-инфекцией тяжелого течения (70%) были обнаружены нарушения в системе естественной и/или специфической цитотоксичности (рис. 2) — снижение содержания зрелых активированных естественных киллеров CD16 + (менее 11%), Т-киллеров и/или ЦТЛ CD8 + (менее 27%). Важно отметить, что выраженное снижение уровня CD8 + (в состав которых входят также и супрессорные клетки) в большинстве случаев сочеталось с повышением уровня CD4 + и иммунорегуляторного индекса, что является фактором риска в отношении формирования аутоиммунных процессов. Как известно, системы естественной и специфической цитотоксичности играют ведущую роль в противовирусной защите.
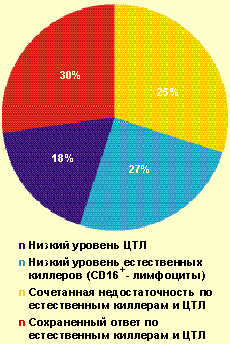 |
| Рисунок 2. Частота выявления нарушений в системе естественной и специфической цитотоксичности у больных с тяжелым течением ВПГ-инфекции (n = 102) |
Обнаруженные нарушения в системах цитотоксичности и их активационных маркерах при ВПГ-инфекции косвенно свидетельствуют о недостаточном уровне продукции Т-хелперами 1 типа ИЛ-2 — одного из важнейших звеньев цитокиновой сети, необходимого для полноценного противовирусного иммунного ответа.
При исследовании функционального состояния нейтрофилов у больных с тяжелым течением ВПГ-инфекции повышение спонтанного НСТ-теста было выявлено почти в половине случаев. Однако показатели стимулированного НСТ-теста и индекса стимуляции, напротив, были существенно снижены у большинства больных, что свидетельствует об истощении у них резервных способностей нейтрофилов.
Н. А. Дидковский, доктор медицинских наук, профессор
И. К. Малашенкова, кандидат медицинских наук
Ж. Ш. Сарсания, кандидат биологических наук
А. Н. Танасова, И. Н. Зуйкова, И. А. Зуйков, Н. М. Хитрик
НИИ физико-химической медицины, ММА им. И. М. Сеченова, Москва
Герпес-вирусная инфекция: расставляем акценты.
– Следующая, очень актуальная тема – «Герпесвирусная инфекция». И я с удовольствием предоставляю слово Игнатовскому Андрею Викторовичу.
Андрей Викторович Игнатовский, кандидат медицинских наук:
– Добрый день, дорогие коллеги. Мы продолжаем разговор об инфекционных агентах. На сегодняшний день герпесвирусная инфекция остается одной из наиболее актуальных проблем для врачей практически всех специальностей. Мы очень часто обсуждаем негативное влияние герпесвирусной инфекции в отношении влияния на репродуктивный тракт – эта проблема чрезвычайно интересна акушерам-гинекологам, урологам. Я думаю, что эта презентация покажет актуальность данной проблемы и для врачей общей практики, врачей-терапевтов.
Обычно мы говорим о вирусах герпеса простого – первого и второго типа, и о вирусе третьего типа – это варицелла зостер вирусной инфекции. И начать мне, конечно, хотелось бы сегодня с варицелла зостер вирусной инфекции, ибо эта инфекция, наверное, в аспекте общей врачебной практики имеет невероятное количество интересных и важных аспектов.
Итак, вирус герпеса третьего типа. Вы видите, что первая встреча с вирусом герпеса третьего типа приводит к развитию ветряной оспы. Это первичная инфекция, вызванная вирусом третьего типа. Определенным важным аспектом является то, что в этом случае при первичной инфекции встреча произошла впервые, антител у пациента нет, и пациент не защищен перед этим инфекционным агентом. Отсюда – достаточно легкомысленное отношение к ветряной оспе может закончиться летальными случаями, которые в России мы периодически видим и которые регистрируются. И, конечно же, разбираясь практически во всех случаях, мы видим, что пациент получал стандартную терапию для легкой формы, и не было принято во внимание то, что пациент не был защищен, и существуют этиотропные препараты, которые практически во всех летальных случаях не были назначены врачом. Далее вирус у пациентов, переболевших ветряной оспой, сохраняется в спинальных ганглиях, и рецидивы герпесвирусной инфекции возникают в виде герпес зостера.
Для кого пациент с герпес зостер опасен? Он опасен для тех пациентов, которые ветряной оспой не болели или от нее не привиты. На сегодняшний день существует вакцинация, и мы знаем, что можем профилактировать возникновение ветряной оспы. Что касается клинического понимания, мне хотелось бы, чтобы в отношении вируса третьего типа оно тоже было. Первичную инфекцию мы называем «ветрянкой», первая встреча с вирусом – антитела отсутствуют. А вот реактивация герпесвируса из спинного ганглия уже носит названия герпес зостер или опоясывающий лишай, или опоясывающий герпес. Это слайд с одной из конференций, где проводился разбор летальных случаев, и лекторы представляли, в том числе, наше легкомысленное отношение к герпесвирусной инфекции, вызванной вирусом третьего типа. Действительно, кажется, что проще переболеть, если в детском коллективе вспышка ветряной оспы – туда, может быть, лучше отвести детей, которые не болели, считают многие родители. Ребенок, столкнувшись с вирусом, переболеет. Я бы предостерег от такой опрометчивой тактики. Лучше ребенка вакцинировать в этом случае, а тех детей, которые заболели ветрянкой, внимательно наблюдать, дабы вовремя определить показания к назначению системных этиотропных противовирусных препаратов. Профессор Таточенко сказал, на мой взгляд, очень красивую и правильную фразу: «Инфекция – это всегда риск. Задача врача – свести его к минимуму». Что касается ветряной оспы, что касается вирусной инфекции, на сегодняшний день мы можем в ряде случаев это сделать и полностью избежать тяжелых осложнений, а иногда и летальных случаев.
Надо помнить, что этиотропные противовирусные препараты, которые эффективны в отношении вируса первого и второго типа, то есть в отношении вируса простого герпеса, почти так же эффективны против варицелла зостер вирусной инфекции. Есть различия, мы сегодня о них, я думаю, успеем сказать, между влиянием ацикловира и пенцикловира на вирус герпеса первого, второго и третьего типа. Но, тем не менее, эти препараты являются этиотропными по отношению к вирусу герпеса первого, второго и третьего типа.
Какой опасности ждать беременным женщинам, которые заболели ветрянкой? Ситуация, наверное, не так часта, но отсюда и масса проблем. С акушерами-гинекологами мы на своих круглых столах всегда обсуждаем этот, достаточно большой, блок вопросов. Но для врача общей практики важно помнить о том, что риск ветряночной пневмонии составляет около 10%.
Возвращаясь к дальнейшему течению герпесвирусной инфекции, нужно, конечно, затронуть вопрос герпес зостер. Традиционное представление, которое многие запоминают со студенческой скамьи, это то, что герпес зостер появляется в зоне грудных дерматомов, грудных сегментов. Конечно же, да, но надо помнить, что на дерматомы разделено практически все человеческое тело, и мы можем увидеть реактивацию герпесвирусной инфекции в виде герпес зостер в зоне любого дерматома.
Вот традиционные клинические проявления – это грудной дерматом. Классические проявления – эритема, отек и сгруппированные микровезикулы, пузырьковая сыпь. Но надо помнить о том, что, если мы видим поражения в зоне нескольких дерматомов, то, конечно, речь идет о том, что герпесвирусная инфекция приобретает, или имеет в данном случае у пациента, тяжелое течение. Дерматомы могут быть в разных локализациях, в частности, генитальная локализация может быть, это могут быть проявления в области крестца и здесь необходимо дифференцировать данные проявления с зостерефорным течением герпесвирусной инфекции, которую может давать вирус герпеса простого, но второго типа.
Если мы говорим о тяжелых, атипичных формах, то, конечно, нужно помнить, что такие формы имеются и у вируса третьего типа. И здесь мы видим у пациента пузыри, заполненные геморрагическим содержимым. Это геморрагическая форма. Могут быть высыпания типичные, но в области молочной железы. Если пациентку не осмотреть полностью и не увидеть вот эту линейность высыпаний, то можно подумать, что у нее некие проявления на молочной железе. Однако, полный осмотр пациента дает представление и позволяет правильно и своевременно поставить диагноз.
Я бы обратил внимание, что прежде традиционным считалось возникновение герпес зостер у пациентов пожилого возраста. Однако (и мы даже на нашей кафедре написали статью, наблюдая пациентов в институте акушерства и гинекологии имени Отта), контингент пациентов как раз помолодел. Мы видели и молодых женщин, как раз в периоде беременности, в периоде кормления.
Надо не забывать об особых локализациях, которые чрезвычайно опасны, прежде всего, жизнеугрожающими состояниями. Это офтальмогерпес. Офтальмогерпес опасен тем, что путь развития этого воспалительного процесса затрагивает и сосуды, и оболочки мозга. И здесь риск осложнения колоссально выше. Начиная от острого некроза сетчатки и заканчивая инсультом. Вот почему, встретившись с таким пациентом, врач практически любой специальности должен не перенаправлять его, выполняя роль некоего «стрелочника», а взять первоначальный этап ведения пациента на себя, а дальше привлекать специалистов нужного профиля – офтальмологов, неврологов. Но этиотропный противовирусный препарат должен быть назначен сразу, как только пациент пришел к вам на прием. Можете считать это неотложным состоянием.
Начальные проявления очень интересны. Всегда это эритема, отек. Микровезикул может не быть, но принципиально важным моментом является то, что (мы можем вернуться и к предыдущему слайду, и посмотреть на этом слайде) поражается четко половина лица, как будто по линейке прочерчен очаг. Но всегда верхушка носа вовлекается, если она у пациента затронута. А здесь четко мы видим одностороннее поражение, что позволяет легко определиться с диагнозом. Ни аллергический процесс так протекать не будет, четко прочерчено, ни один другой.
Надо помнить, что у 10% больных с нормальным иммунитетом при опоясывающем герпесе возможно гематогенное распространение инфекции с развитием диссеминированной формы, что тоже должно настораживать врача и сделать его особо внимательным к таким пациентам. Надо помнить о том, что клиническими проявлениями являются не только высыпания, но еще и боль. Она, как правило, сопровождает данный процесс и присутствует в разных формах. О вариантах боли мы тоже сегодня с вами поговорим.
Как раз постгерпетическую невралгию считают одним из грозных осложнений среди всех основных групп, мы видим – их много: кожные, висцеральные, неврологические, глазные осложнения. Но постгерпетическая невралгия труднее всего поддается именно медикаментозному воздействию. Иногда, даже при правильной и своевременно назначенной терапии, избежать такого осложнения невозможно.
Что же собой представляет постгерпетическая невралгия, и у кого риск выше? Это пациенты пожилого и старшего возраста. Область высыпаний имеет значение: максимальный риск – это зона тройничного нерва и плечевого сплетения. Другие зоны имеют умеренный или меньший риск, но это не исключает возникновения такого болевого синдрома. Конечно, боль в продроме, предшествующая высыпаниям, и выраженная сыпь.
Надо помнить о том, что, чем старше возраст пациента, тем выше риск развития постгерпетической невралгии. Что мы подразумеваем под постгерпетической невралгией? Пожалуй, вот эта классификация Дворкина – наиболее приемлема, и она наиболее правильно показывает нам, что постгерпетической невралгией мы можем считать ту боль, которая существует четыре месяца и длительнее. Все, что до четырех месяцев, делим либо на острую герпетическую невралгию, либо на подострую герпетическую невралгию. Принципиально важным моментом этой классификации являются и лечебные подходы. Они различны. В начальном этапе заболевания, наряду с воспалительной болью, вызванной влиянием вируса, зарождается и боль нейропатическая. Принципиальной разницей является то, что на боль воспалительную мы прекрасно повлияем нестероидными противовоспалительными препаратами и анальгетиками. А вот на боль, которая называется нейропатической, к сожалению, противовоспалительными препаратами и анальгетиками мы повлиять не сможем, и с течением времени, как раз к четвертому месяцу, значение воспалительной боли практически снижается, а вот значение и роль нейропатической боли колоссально возрастает. Вот почему пациентам, которые болеют долго, у которых боль сохраняется после перенесенного герпеса четыре месяца и больше, назначение анальгетиков бесполезно, нужно назначать совершенно иные классы препаратов, привлекая для консультации врача-невролога. Без невролога грамотное лечение такого пациента невозможно.
Вы видите, что варианты боли могут быть совершенно разными – это и острая, и рвущая боль. Иногда это может быть аллодиния – боль при легком прикосновении. Но, тем не менее, все это доставляет чрезвычайные страдания нашим пациентам. Как избежать этой боли? Как избежать постгерпетической невралгии? Раннее назначение – до 72 часов. Нередко врачи неправильно понимают 72 часа. Пациент пришел через 74 часа, но у него есть высыпания, имеется активность процесса – мы обязательно должны все равно такую терапию назначить. Мы говорим об идеальных условиях – чем раньше такая терапия началась, тем более лучшие результаты мы с вами получим. Конечно, назначение высокоэффективных противовирусных препаратов, я, прежде всего, говорю о фамцикловире, адекватное обезболивание в острой стадии. Неплохие предварительные результаты получены об эффективности вакцинации. Какие же принципы лечения на сегодняшний день существуют для герпесвирусной инфекции? Конечно, это этиотропная терапия. Нужно помнить, что аналоги нуклеозидов – это препараты выбора на сегодняшний день для лечения всех форм герпесвирусной инфекции. Иммуномодулирующая терапия – это терапия патогенетическая. Мы без нее обойтись можем. Она ни в один протокол – международный и отечественный – не входит. Симптоматическая терапия, конечно же, имеет определенное значение.
И, несомненно, нужно помнить то, что этиотропные препараты – это препараты ацикловира, его валиново- и фервалоцикловир и фамцикловир. (00:12:30) Симптоматическая терапия потребуется, скорее всего, пациенту с опоясывающим герпесом. Это анальгетики, нестероидные противовоспалительные препараты и, на этапе борьбы с болью, физиотерапия, но не ультрафиолет. Нужно помнить, что ультрафиолет – это фактор агрессивный, повреждающий. А загар – это защитная функция кожи.
Выбирая препарат, необходимо помнить, что наиболее чувствительный к ацикловиру – вирус простого герпеса первого и второго типа варицелла зостер – более, чем в 20 раз, а цитомегаловирус – в 470 раз менее чувствителен к ацикловиру, чем вирус простого герпеса первого типа. Если говорить о препаратах, то, конечно, нужно помнить о том, что на сегодняшний день и препараты ацикловира (это ацикловир и валацикловир, и фамцикловир) различаются биодоступностью. Биодоступность препаратов различна, обусловлена их фармакокинетическими особенностями и, прежде всего, накоплением в определенных структурах. И нам важно, говоря и обсуждая герпесвирусную инфекцию, вызванную вирусом простого герпеса и вирусом герпеса третьего типа, накопление в шванновских клетках, ибо распространение вируса из спинального ганглия идет периневрально, перриаксонально и, как раз, по шванновским клеткам. Концентрация пенцикловира – это действующее вещество фамцикловир – они во много раз превышают концентрацию ацикловира.
И еще один важный момент – мы говорим, что аномальные нуклеозиды становятся активными под влиянием ферментов самого герпесвируса и накапливаются только избирательно в инфицированных клетках. Надо помнить о том, что все препараты ацикловира (это касается ацикловира, валацикловира) находятся внутриклеточно меньше часа или около часа. Если мы говорим о фамцикловире, то вы видите, исходя из таблицы, которая, по сути, построена на данных многочисленных исследований, что вирус варицелла зостер позволяет препарату находиться в инфицированной клетке от 7 до 11 часов.
Путь выведения – почки. Мы должны сейчас запомнить этот очень важный аспект, ибо в завершение своей презентации я покажу вопросы, и коснемся мы вопросов лекарственной безопасности применения этих препаратов. Если говорить о сравнительном анализе и о дозировках препаратов, то, несомненно, такие исследования также были проведены. И вы видите на данной схеме сравнительные дозировки фамцикловира в дозе 250 мг три раза в сутки, по 500 мг три раза в сутки. И сравнение с ацикловиром – традиционно известной нам дозы 800 мг пять раз в сутки.
Мы видим, конечно же, что ацикловир отстает. Его фармакокинетические, фармакодинамические особенности отличаются от фамцикловира. И, конечно же, мощный эффект с более современной формой фамцикловир обеспечивает и лучшие терапевтические показания, поэтому он на сегодняшний день и считается препаратом номер один для лечения герпесвирусной инфекции, вызванной, в частности, вирусом герпеса третьего типа.
Если мы с вами обсуждаем показания, то, конечно, в этом случае герпес зостер для нас важен. Накопление в шванновских клетках мы уже обсуждали. И дозировки будут различаться: у пациентов с нормальным иммунитетом дозировка 250 мг три раза в сутки, либо 500 мг два раза в сутки. Единственным отличием, когда дозировку нужно будет удвоить, повысить, это офтальмогерпес. По сути, мы должны сказать, что у пациентов со сниженным иммунитетом всегда дозировки будут удвоены. И пациенты с офтальмогерпесом, даже при нормальном иммунитете, все-таки требуют высоких дозировок. Это дозировка 500 мг три раза в сутки. Если мы говорим про опоясывающий герпес у пациентов со сниженным иммунитетом, то здесь фамцикловир назначается также в удвоенной дозировке, и продолжительность терапии – 10 дней.
Обратите внимание на этот слайд – это пациент с офтальмогрепесом. Здесь дозировка должна быть также 500 мг три раза в сутки. Несомненно, нужно привлекать для консультации врача-невролога и врача-офтальмолога.
Говоря о пациентах иммунокомпромисных, с недостаточностью иммунитета, нужно, конечно, не забыть о пациентах с вирусом иммунодефицита. Здесь нужно помнить о том, фамцикловир – это единственный препарат, одобренный FDA для лечения и опоясывающего герпеса, и генитального герпеса у ВИЧ-положительных пациентов.
Если коснуться вопроса лечения постгерпетической невралгии, нужно отметить, что как раз эффективными в отношении влияния на нейропатическую боль будут такие препараты, как габапентин, прегабалин. И, мы обсуждали этот аспект, обязательно необходимо привлечение специалиста-невролога. Именно он должен назначить такие препараты. Они могут быть назначены одновременно с фамцикловиром или с другим аномальным нуклеозидом, либо могут быть назначены в ближайшее время. То есть, по сути, не надо дожидаться развития постгерпетической невралгии и постановки такого диагноза. Последние исследования показали, что, чем раньше мы назначим такие препараты, тем лучше эффективность в лечении этого состояния. Вы видите, что есть препараты для лечения второго ряда, и, конечно, есть определенные подходы. Прежде всего, мы ориентируемся на визуально-аналоговую шкалу боли. И, понимая, что мы получили или не получили эффект от проводимой терапии, мы можем эту терапию скорректировать. Значит, нужно понимать, что терапия не однозначна. Она сложна для пациента, ее переносимость не всегда бывает легкой и простой. Здесь требуется особое внимание, и, повторюсь еще раз, лучше профилактировать – ранним адекватным назначением этиотропного противовирусного препарата.
Вторым блоком хотелось бы обсудить герпесвирусную инфекцию, вызванную вирусом простого герпеса первого и второго типа. Традиционно мы разделяли: условно мы считали, что вирус первого типа поражает верхнюю часть туловища, локализуясь в области лица, губ. А вирус второго герпеса считали генитальным. Однако лабораторная диагностика совершенствуется, и на сегодняшний день мы знаем, что эти вирусы давно уже не имеют той четкой анатомической привязки, которую мы с вами прежде различали.
Надо, конечно, помнить, что мы разделяем первичный герпес и рецидивирующие формы герпесвирусной инфекции. Особенности клинические: острое начало первичной инфекции, симптомы интоксикации, увеличение регионарных лимфоузлов – вот, по сути дела основные клинические признаки. А лабораторными будут нарастания уровня антител. Чаще мы сталкиваемся с первичной инфекцией именно у детей. И такой формой является герпетический гингивостоматит, герпетические проявления в области губ – лабиальный герпес. Если мы говорим о генитальной локализации, о том периоде, когда человек в детстве не встретился с данным вирусом, а, уже начав половую жизнь, получил вирус – в этом случае, конечно, развивается первичный генитальный герпес. Возможны и другие проявления.
Если мы говорим с вами о симптомах рецидива – они хорошо известны. Продромальные явления в виде боли, зуда, жжения, дискомфорта в зоне высыпаний, и в дальнейшем уже проявления клинические. Они могут быть не всегда в виде эритемы и отека, возможно появление как типичных форм, так и атипичных. В случае атипичного течения мы с вами не увидим пузырьков, как мы обсуждали, либо эти пузырьки будут заполнены геморрагическим содержимым, либо это будут, может быть, даже уже пузыри.
Конечно, необходимо различать и степени тяжести – легкое, среднетяжелое и тяжелое течение. Именно от этого аспекта будет зависеть подход врача, планируемые мероприятия и, конечно же, аспект консультирования пациента. Если говорить о клинических проявлениях – они хорошо знакомы. Однако требуется уточнить – это первичная герпесвирусная инфекция или это рецидив. Клинические проявления могут быть несколько похожи, лишь лабораторные тесты позволят нам различить первичную инфекцию и рецидив. В случае присоединения осложнения, как вы видите на данном слайде, потребуется обсуждение вопроса применения топических или, может быть, даже системных антибактериальных препаратов.
В случае герпетического глоссита – поражения слизистой рта – топические препараты, несомненно, невозможно применить, и здесь обязательно будут обсуждаться только системные этиотропные противовирусные препараты. Ну, а в данном случае следует, конечно, не забыть о том, что имеется риск развития офтальмогерпеса, развития герпетического кератита, и здесь чрезвычайно важным вопросом будет, опять-таки, обсуждение не только применения глазных капель, обладающих противовирусным действием, а и обязательно в назначение системных этиотропных противовирусных препаратов.
Говоря о стратегиях терапии герпесвирусной инфекции, нужно помнить о том, что существует лечение, оно различается дозировками, первичная инфекция рецидива и два варианта супрессивной терапии – эпизодическая супрессивная терапия в преддверии медицинских манипуляций и длительная супрессивная терапия для профилактики рецидивов и профилактики передачи партнеру. Что важно? Важно то, что применение наружных форм на сегодняшний день следует ограничивать. Европейское руководство по ведению пациентов с генитальным герпесом в 2010 году, ссылаясь на работу, опубликованную ранее, показало, что применение местных препаратов способствует формированию устойчивости к данному препарату. Следовательно, нужно ограничить применение топических форм. Если же мы говорим о применении препарата при первичной инфекции, здесь я скажу о том, что на сегодняшний день различается – это дозировки. Для фамцикловира они как были 250 мг три раза в сутки, так и остались, а вот для валацикловира CDC с 2010 года, а Всемирная организация здравоохранения с 2003 года дозировку увеличила. Эта дозировка для лечения первичной инфекции составляет 1000 мг два раза в сутки. Если мы говорим о применении валацикловира и ацикловира, нужно помнить, что действующей субстанцией остается тот же самый ацикловир. За счет соединения с аминокислотой валин получается комплекс, который, да, хорошо всасывается, но действующим веществом остается ацикловир. Дозировки, которые применяются для лечения рецидивирующей инфекции, представлены на слайде. Наименьшие дозировки имеет фамцикловир – это 125 мг два раза в сутки, для валацикловира эта дозировка – 500 мг два раза в сутки, для ацикловира эта дозировка может варьироваться, составляя от 200 мг до 400 мг на однократный прием, и количество таких приемов – от трех до пяти.
Новая дозировка для фамцикловира, для фамвира, зарегистрированная в инструкции, это короткие курсы. По сути дела, весь мир борется за такие короткие курсы. Применение препарата при частых рецидивах способствует быстрому купированию симптомов, при этом нарастает уровень антител, способствующий в дальнейшем более легкому течению герпесвирусной инфекции. И вот такая трехдневная схема лечения достаточно удобна для наших пациентов. Необходимо, конечно, помнить различие в препаратах, ибо развитие ацикловир резистентных штаммов сегодня, наверное, будет потихоньку выходить на одну из ведущих лидирующих позиций.
Как же препараты работают? Итак, вирус проник в клетку, дальше начинается сборка вирусной ДНК под влиянием двух вирусных ферментов – вирусной тимидинкиназы и вирусной полимеразы. А препараты, которые попадают в клетку, – ацикловир и пенцикловир – сходны с гуанозином, с одним из компонентов вирусной ДНК. Далее тимидинкиназа вируса делает активным ацикловир, и эта молекула ацикловира остается, условно говоря, в одиночестве. Если мы говорим про пенцикловир, то ситуация следующая: тимидинкиназа вируса также активизирует пенцикловир, однако тимидинкиназа вируса имеет в сто раз больший сросток пенцикловира, и количество молекул пенцикловира во много раз выше внутриклеточное. А дальше – вирусная полимераза ошибочно встраивает пенцикловир в терминальные участки ДНК, так как они аномальные, нет комплиментарного хвоста и, соответственно, прекращается сборка вирусной ДНК. Таким образом, препараты работают только в тех клетках, где есть вирус. Там, где вируса нет, где вирус не реплицируется, препарат работать не будет. Вот это чрезвычайно важно. Ну, и концентрация пенцикловира на левых графиках – они высокие и стабильные и с течением времени не снижаются. А вот ацикловир трифосфат, к сожалению, очень быстро уходит из плазмы, и его терапевтические концентрации быстро падают.
Говоря о лабиальном герпесе, завершая наш разговор, нужно сказать, что существует короткая схема однократного приема – три таблетки по 500 мг, удобная импульсная схема, и надо, конечно же, не упускать такой возможности, ибо нередко лабиальный герпес для некоторых пациентов является стартом в развитии осложнений со стороны нервной системы. Об этом необходимо помнить.
И в завершение хотелось бы привести ту работу, которая опубликована в 2008 году. Меня она поразила своей аннотацией – мы не так часто уделяем внимание побочным эффектам и вопросам лекарственной безопасности, однако аннотация достаточно интересна. В инструкции к препаратам ацикловира обозначено, что нужно обеспечивать даже в таблетированных формах адекватную гидратацию пациента. Но, обратите внимание, в данной статье обсуждаются вопросы, когда пациентам был применен внутривенно ацикловир, дозировки требовались высокие, по тяжести течения данного процесса, и были получены осложнения в виде острой почечной недостаточности. Чем такие осложнения вызваны? Прежде всего, молекулярной структурой ацикловира. Он имеет кристаллическую структуру, и эти кристаллы способны повреждать тубулярный аппарат почки и, по сути, приводить к развитию острой почечной недостаточности. Впоследствии такие пациенты были переведены на фамцикловир и успешно выздоровели. Как раз таки, применяя препараты ацикловира, нужно помнить, что и при внутривенном введении, и назначая таблетированные формы, необходимо проводить пациенту хорошую гидратацию.
