Аудиторная нейропатия у детей что это
Аудиторная нейропатия у детей что это
а) Слуховой скрининг новорожденных. Программы по слуховому скринингу всех новорожденных детей на настоящий момент приняты в большинстве штатов США. Но поскольку многие программы подразумевают исследование ОАЭ, но не СВП, диагностика СН/ЗГСН в ходе слухового скрининга возможна не всегда. Как следует из согласительного документа 2007 года, разработанного Объединенной рабочей группой по слуху, СН/ЗГСН должна входить в список заболеваний, которые нужно исключать у детей, поступающих в отделение реанимации новорожденных.
Также в этом документе говорится о том, что с целью диагностики слуховой нейропатии (СН) всем детям, которые находятся в отделении реанимации более пяти суток, необходимо исследовать слуховые вызванные потенциалы (СВП). Тем не менее, у значительного числа детей, у которых слуховая нейропатия (СН) была диагностирована в возрасте до двух лет, отсутствуют какие-либо факторы риска. Следовательно, шанс на то, что заболевание так и останется недиагностированным, остается высоким.
б) Дифференциальная диагностика слуховой нейропатии. Протокол диагностики слуховой нейропатии (СН) подразумевает использование междисциплинарного подхода к диагностике, с уклоном в аудиологические и общемедицинские методы. Набор аудиологических исследований, необходимых для исключения слуховой нейропатии (СН), включает аудиометрию, надпороговую речевую аудиометрию, тимпанометрию с определением акустического рефлекса, исследование отоакустической эмиссии (ОАЭ) и слуховых вызванных потенциалов (СВП).
Также в некоторых случаях выполняются определение разницы маскированных уровней слуха; электрокохлеография, необходимая для определения микрофонного потенциала улитки и суммационных потенциалов действия; исследование эфферентного подавления отоакустической эмиссии (ОАЭ) (оливокохлеарный рефлекс); а также исследование функции вестибулярного анализатора. И хотя нарушения вестибулярного анализатора могут сосуществовать с слуховой нейропатией (СН), сами по себе нарушения работы вестибулярного нерва или его синапсов не могут служить критерием постановки диагноза слуховой нейропатии (СН).
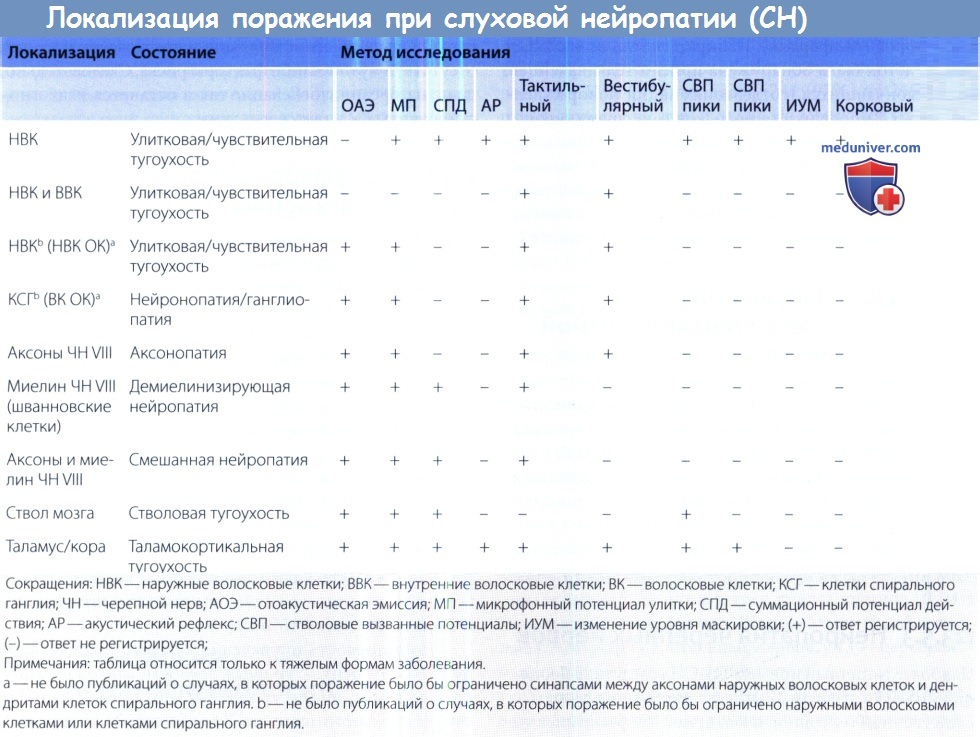
Необходимость проведения каждого исследования нужно соотносить с уровнем зрелости слухового аппарата, а также с общим уровнем когнитивных способностей конкретного пациента. В таблице ниже приведены типичные результаты разных методов исследования при различных уровнях поражения слухового анализатора.
Отоакустическая эмиссия (ОАЭ) и слуховые вызванные потенциалы (СВП) не позволяют провести дифференциальную диагностику между селективным повреждением внутренних волосковых клеток и повреждением VIII ЧН. Если однозначно убедиться в том, что поражен именно слуховой нерв, невозможно, значит, при формулировке диагноза нужно использовать термин заболеваний группы слуховой нейропатии (ЗГСН); понятие слуховой нейропатии (СН) лучше применять в том случае, если у пациента диагностирована периферическая нейропатия.
в) Аудиометрия и исследование разборчивости речи. Пороги воздушной и костной проводимости у пациентов с СН/ЗГСН могут быть разными: от нормального слуха до тяжелой тугоухости и полной глухоты. У некоторых пациентов аудиограмма может иметь «восходящий» характер или другую нехарактерную форму.
В большинстве случаев слуховой нейропатии (СН) поражаются оба уха, но, согласно данным Berlin и соавт., в 23% случаев (24 из 103) двусторонней слуховой нейропатии (СН) тугоухость носит асимметричный характер. В другом исследовании анализировались 16 детей с слуховой нейропатией (СН), из них легкое или умеренное снижение слуха наблюдалось у 5 детей, умеренное или тяжелое — у 2, тяжелое до очень тяжелого — у 7, у 2 детей тугоухость носила флюктуирующий характер. У большинства детей (63%) имелось сразу несколько факторов риска: гипербилирубинемия (24%), недоношенность (19%), тот или иной генетический синдром (10%), низкий вес при рождении (5%), гидроцефалия (5%).
Среднее снижение слуха при анализе 66 ушей составило 57 дБ ПС (на частотах 1000, 2000, 4000 Гц).
Снижение слуха при слуховой нейропатии (СН) носит либо нейросенсорный, либо смешанный характер. В последнем случае слуховая нейропатия (СН) сочетается с аномалиями наружного или среднего уха, напрямую кондуктивный компонент тугоухости с слуховой нейропатией (СН) не связан. Средний отит и другие заболевания среднего уха могут делать диагностику слуховой нейропатии (СН) крайне затруднительной, особенно у младенцев и маленьких детей, у которых средний отит встречается особенно часто.
В литературе описаны случаи несоответствия между данными субъективной аудиометрии и исследованием слуховых вызванных потенциалов (СВП).
У очень многих пациентов с слуховой нейропатией (СН) очень сильно разнятся результаты надпороговой речевой аудиометрии, проводимой в условиях шума, и речевой аудиометрии, проводимой в тихих условиях. Разборчивость речи в шумных условиях оказывается непропорционально понижена.
г) Тимпанометрия. Поскольку слуховая нейропатия (СН) является заболеванием нервной системы, результаты тимпанометрии обычно неинформативны. Высокая частота встречаемости заболеваний среднего уха (средний отит) могут сделать постановку диагноза затруднительной.
При использовании низкочастотных стимулов (226 Гц) ипсилатеральные и контралатеральные акустические рефлексы обычно отсутствуют. Тем не менее, в большей части исследований в качестве стимула использовался именно низкочастотный сигнал. В будущем необходимо будет оценить связь между слуховая нейропатией (СН) и акустическими рефлексами, вызванными стимулами средней и высокой частоты. Сокращения мышц среднего уха обычно сохранены.
д) Отоакустическая эмиссия (ОАЭ). Обычно у пациентов с слуховой нейропатией (СН) при проведении задержанной вызванной отоакустической эмиссии (ЗВОАЭ) и отоакустической эмиссии на частоте продукта искажения (ЭЧПИ) регистрируется активность наружных волосковых клеток. ЗВОАЭ сохранена при снижении слуха не более 30 дБ ПС, ЭЧПИ может регистрироваться и при более выраженном снижении слуха. Со временем отоакустическая эмиссия (ОАЭ) может ослабнуть или пропасть, либо в результате снижения слуховой чувствительности, либо вследствие присоединения заболеваний среднего уха.
Четкой корреляции между функцией волосковых клеток и степенью снижения слуха нет, поскольку при слуховой нейропатии (СН) тугоухость обусловлена либо поражением нервных волокон, либо нарушением передачи электрических сигналов в ответ на звуковой раздражитель. Согласно данным Starr и соавт., ЗВОАЭ не регистрировалась в 30% из 63 ушей с СН/ЗГСН; в 25% ЗВОАЭ отсутствовали с обеих сторон, в 5% — с одной стороны. Из тех детей, у которых ЗВОАЭ отсутствовали, у 11 человек они регистрировались в прошлом.
Если регистрация отоакустической эмиссии (ОАЭ) невозможна из-за наличия патологического процесса в среднем ухе, оценить функцию волосковых клеток можно за счет регистрации микрофонного потенциала (МП) улитки, для записи которого используются поверхностные электроды и инструментарий для регистрации слуховых вызванных потенциалов (СВП), в особенности вставные наушники. У пациентов с СН/ЗГСН, как и у здоровых лиц, пики оказываются инвертированы при изменении полярности стимулов (фаза разрежения и фаза конденсации).
Согласно некоторым исследованиям, даже при сохраненном микрофонном потенциале ОАЭ может со временем пропадать. И ОАЭ, и МП зависят от активности волосковых клеток. Тем не менее, чувствительность данных исследований в отношении повреждения наружных волосковых клеток может быть разной, также они могут отражать сохранность разных функций волосковых клеток.
Эфферентное подавление отоакустической эмиссии. Во время феномена эфферентного подавления отоакустической эмиссии (оливокохлеарный рефлекс) происходит изменение амплитуды или изменение фазы в ответ на подачу дополнительных стимулов. Феномен эфферентного подавления наблюдается у здоровых людей, но обычно отсутствует при СН/ЗГСН. Согласно сообщениям Berlin и соавт., у здоровых лиц после подачи непрерывного шумового сигнала в противоположное ухо происходит небольшое снижение ОАЭ на 2-3 дБ в течение 20 мс, а также чуть большее снижение в 6-8 дБ после прекращения стимула при проведении микроструктурного анализа.
Этот феномен отсутствовал у пациентов с предполагаемой СН/ЗГСН (близкий к норме слух, отсутствие СВП) и у пациентов с болезнью Шарко-Мари-Тута, у которых регистрировалась ОАЭ, был резко снижен слух (по данным пороговой аудиометрии), отсутствовали акустические рефлексы и СВП.
е) Стволовые вызванные потенциалы и микрофонный потенциал улитки. При обследовании пациентов с слуховой нейропатией (СН), Teagle и соавт. исследовали СВП путем подачи высокоинтенсивного стимула через вставные наушники; фаза разрежения и фаза конденсации регистрировались по отдельности. Регистрация микрофонного потенциала (МП) упрощается при использовании однополярных стимулов. МП можно отличить от СВП по следующим признакам: пик МП становится инвертированным при изменении полярности стимула (с фазы конденсации на фазу разрежения, и наоборот), в то время как латентный период МП при увеличении или уменьшении интенсивности сигнала остается практически неизменным.
Для того, чтобы определить, изменяется ли латентный период вместе с изменением интенсивности стимула, каждый однополярный стимул нужно представлять дважды с разницей в 10 дБ. Для того, чтобы исключить появление артефактов при записи, нужно повторить ее с извлеченным наушником: если пик исчезнет, значит, он действительно представлял МП, а не просто артефакт регистрации.
Некоторые исследовали сообщали о том, что у лиц с слуховой нейропатией (СН) регистрируются МП большей амплитуды и большей длительности. Например, Starr и соав. выяснили, что по сравнению со здоровыми лицами у больных СН/ЗГСН повышена амплитуда МП и его длительность (например, инвертированный по фазе МП у здоровых и у больных лиц достигал пика на 0,4 мс, но длительность его была выше у пациентов с СН (до 3 мс), чем у здоровых лиц (до 0,7 мс). У пациентов с СН/ЗГСН амплитуда МП превосходит нормальные возрастные значения в среднем на два стандартных отклонения (вычисленные по контрольной группе).
Пики слуховых вызванных потенциалов (СВП) у больных с слуховой нейропатией (СН) обычно отсутствуют или искажены. Starr и соавт. регистрировали СВП у 21% пациентов из группы в 33 человека (66 ушей). Амплитуда пика V была понижена, пик I отсутствовал. Латентный период V пика был удлинен в 62,5% из 16 случаев. Не было зарегистрировано статистически значимой разницы в амплитуде МП или порогах восприятия (1000,2000 и 4000 Гц) между пациентами с СН/ЗГСН и сохраненными СВП, и пациентами с СН/ЗГСН и отсутствием СВП.
ж) Суммационный потенциал. В одном исследовании трех взрослых пациентов с слуховой нейропатией (СН), суммационный потенциал (СП), записанный в ходе электрокохлеографии (внетимпанальная запись), был сохранен. В другом исследовании, где анализировалось 57 ушей с СН/ЗГСН, данные были противоречивы: СП отсутствовал в 50% ушей с СН и в 50% из 27 контрольных здоровых ушей.
з) Изменение уровня маскировки. Изменение уровня маскировки (ИУМ) определяется как улучшение маскированных порогов при подаче сигнала в оба уха сразу (диотически) по сравнению с подачей сигнала в одно ухо (моноотически). Например, отсутствие улучшения маскированных порогов костной проводимости при подаче низкочастотного сигнала после добавления сигнала во второе ухо, наблюдалось Starr и соав. в шести случаях пациентов с подозрением на СН/ЗГСН.
Отсутствие ИУМ позволяет отличить СН/ЗГСН от кондуктивной тугоухости или тугоухости улиткового генеза, при которых ИУМ сохранен, хотя и снижен по сравнен ию с нормативными показателями. Впрочем, диагностическая ценность измерения ИУМ может страдать при тяжелой или асимметричной тугоухости.
и) Исследование вестибулярного аппарата. Наличие повреждения вестибулярной ветви VIII пары ЧН и его окончаний наблюдалось у трех пациентов с СН/ЗГСН, у которых имелись отклонения при проведении калорических и ротационных проб. Саккады, плавные движения глаз, оптокинетический нистагм были в норме.
Для диагностики таких нарушений нужно тщательно собирать весь анамнез, проводить полный осмотр, брать лабораторные пробы. Детям для визуализации лабиринтов, внутренних слуховых проходов, VIII пары ЧН и головного мозга рекомендуется выполнять МРТ. При наличии стеноза слуховых проходов, аномалий строения височной кости, пороков развития внутреннего уха, обструкции просвета улитки также показано выполнение КТ височных костей.
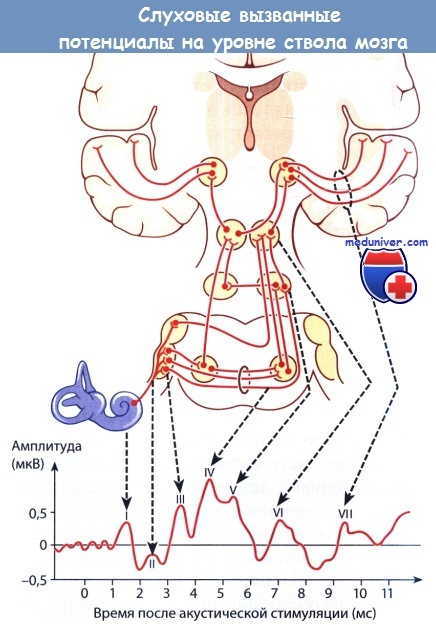
На типичной кривой имеются 5 или 7 зубцов (I—VII),
отражающих активность анатомических структур слухового анализатора,
индуцируемую акустической стимуляцией.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Слуховая (аудиторная) нейропатия
Расстройство спектра аудиторных нейропатий РСАН
Ретрокохлеарное поражение, аудиторная нейропатия – это симптомокомплекс, характеризующийся нормальным функционированием внутреннего уха и нарушением обработки звуковой информации в более глубоколежащих отделах слуховой системы. По данным мировой статистики, данным типом поражения системы слуха страдает примерно 1 из 10 детей с хронической тугоухостью.
Особенность аудиторной нейропатии и ее главное отличие от сенсоневральной тугоухости в «точке» возникновения патологии. При сенсоневральной тугоухости страдают чувствительные окончания слухового нерва – волосковые клетки, но сам нерв остается неповрежденным. Поэтому для коррекции такого вида нарушения слуха достаточно в нужной мере усилить необходимые частоты и мозг ребенка будет полностью обеспечен звуковой информацией.
А при расстройстве спектра аудиторных нейропатий окончания слухового нерва чаще всего остаются неповрежденными и могут воспринимать окружающие звуки в полном объеме. Однако при проведении нервных импульсов по слуховому нерву в головной мозг звуковая информация декодируется и искажается. Именно поэтому обнаружение и коррекция данного типа снижения слуха настолько сложны. Такие дети обычно не имеют выраженных проблем с восприятием чистого тона, но обработка речевой информации для них представляет значительные сложности. Самое коварное – что скрининговый тест может «пропустить» малыша с аудиторной нейропатией как слышащего и принципы раннего вмешательства будут нарушены.
Факторы риска развития РСАН
Если у ребенка присутствует хоть один из указанных факторов риска, ему необходимо выполнить регистрацию КСВП (скрининга КСВП) не позднее 1 месяца после рождения, вне зависимости от результатов ОАЭ.
Важно помнить, что расстройство спектра аудиторных нейропатий – чаще всего не самостоятельное заболевание, а лишь проявление одной из существующих патологий. Поэтому дети с выявленным РСАН обязательно наблюдаются у невролога, офтальмолога, проходят углубленное генетическое обследование, и их лечение, как правило, является комплексным. В большинстве случаев снижение слуха при РСАН успешно корректируется применением детских цифровых слуховых систем, при их неэффективности может применяться кохлеарная имплантация. В ряде случаев никакой слуховой коррекции при данной патологии не нужно совсем, это определит детский сурдолог во время дополнительных повторных исследований поведенческих порогов слуха (VRA, BOA, игровая аудиометрия).
Необходимо отметить, что расстройство спектра аудиторных нейропатий является междисциплинарным, и довольно сложным для реабилитации и определения прогнозов. Однако чем раньше будет установлен диагноз и назначена соответствующая коррекция, тем лучше будет общее развитие малыша.
Слуховая нейропатия (ANSD-auditory neuropathy spectrum disorder, аудиторная нейропатия)
Частота встречаемости заболевания не зависит от пола и возраста.
Люди с диагностированной слуховой нейропатией могут иметь нормальный слух или потерю слуха разной степени, но у них всегда будет нарушено восприятие речи, ее распознавание. Довольно часто врачи встречаются с ситуацией, когда у пациента восприятие речи намного хуже, чем предполагают данные о потере слуха.
К примеру, человек со слуховой нейропатией способен слышать звуки, но все равно будет трудно распознать произносимые слова. Звуки могут то появляться, то исчезать для этих людей, следовательно, речь кажется не систематизированной.
Причины слуховой нейропатии
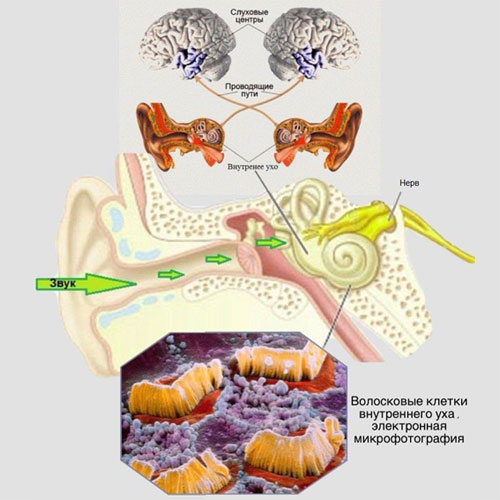
Во время процесса звукопроведения звук проходит через наружное, среднее и внутреннее ухо. Во внутреннем ухе содержатся волосковые клетки, это чувствительные клетки, которые воспринимают звуковые колебания, затем превращают его в электрический импульс, для того чтобы этот импульс в дальнейшем передался, посредством слухового нерва, в головной мозг человека.
Волосковые клетки внутреннего уха разделяются на внутренние и наружные. Наружные волосковые клетки помогают усиливать звуковую вибрацию, входящую во внутреннее ухо, а внутренние волосковые клетки преобразуют ее в электрический импульс. При слуховой нейропатии наружные волосковые клетки не повреждаются.
Аудиторные нейропатии (заболевания профиля аудиторных нейропатий): подходы к диагностике и реабилитации
Г.А. Таварткиладзе
Российский научно-практический центр аудиологии и слухопротезирования ФМБА России, Москва, Россия, 117513; Кафедра сурдологии РМАПО Минздрава России, Москва, Россия, 123395
Журнал: Вестник оториноларингологии. 2014;(2): 9-16

Рисунок 1. Разборчивость фонем в шуме в норме и у больного с аудиторной нейропатией.

Рисунок 2. Данные тональной аудиометрии, регистрации КСВП, ОАЭ и микрофонного потенциала у больного с односторонней аудиторной нейропатией.
При обследовании детей с АН рекомендуется следующий набор тестов:
— анамнез и консультация педиатра;
— отоскопия, КТ и МРТ улитки и слухового нерва;
— медицинское генетическое исследование;
— офтальмологическое исследование;
— неврологическое исследование.
При определении реабилитационных стратегий рассматриваются три основные принципа: 1) этиология заболевания позволяет определить, является ли патологическое состояние постоянным или преходящим [10, 24, 25], и сделать выбор между медикаментозным или хирургическим лечением либо электроакустической коррекцией;
2) учитывая то, что дети с АН и особенно те, кто находился в палатах интенсивной терапии, относятся к группе риска по сопутствующей патологии, раннее выявление отставания в развитии может оптимизировать дальнейшую тактику реабилитации; 3) у детей с АН могут вторично развиваться внутричерепные и периферические нейропатии.
АН может быть как двусторонней, так и односторонней. У всех детей с АН и особенно тех, у кого имеется одностороннее поражение и отсутствуют анамнестические данные, указывающие на возможность развития АН [26], а также с односторонней аномалией челюстно-лицевого скелета [27] необходимо рассматривать вероятность наличия аплазии или гипоплазии слухового нерва. С этой целью рекомендуется проведение КТ и МРТ.
Следует иметь в виду, что у некоторых детей слуховая функция восстанавливается в течение первых двух лет жизни [10].
У детей в возрасте до 24 мес следует очень осторожно относиться к результатам регистрации КСВП (при их отсутствии). Для принятия решения о реабилитации необходимо динамическое наблюдение!
Корковые ВП: среднелатентный СВП, длиннолатентный СВП, Mismatch Negativity (MMN), Р300
При невозможности определить пороги слышимости у детей, а также для определения прогноза реабилитационных мероприятий рекомендуется регистрация СВП коркового происхождения [15, 36, 37]. Больные, у которых регистрировались длиннолатентные СВП и отрицательный потенциал рассогласования (MMN), имели достоверно больший процент распознавания слов и лучшие результаты при использовании усиления [15].
Наличие MMN (рис. 3) указывает на активное кодирование акустических характеристик на корковом уровне, что способствует восприятию речи.

Рисунок 3. Регистрация MMN у больного с аудиторной нейропатией.
Отсутствие электрически вызванных средне- и длиннолатентных СВП у больных АН коррелирует с ухудшением восприятия речи.
В некоторых случаях возможна также регистрация корковых ВП у больных при отсутствии средне- и коротколатентных СВП (рис. 4), что коррелирует с данными, свидетельствующими о том, что у некоторых больных с отсутствием КСВП сохраняется некоторая способность к различению речи.

Рисунок 4. Регистрация ДСВП при отсутствии КСВП и ССВП у больного с аудиторной нейропатией.
Скрининг
При проведении скрининга, основанного на регистрации ОАЭ, АН не выявляются. Это свидетельствует о том, что для повышения эффективности универсального аудиологического скрининга необходимо проведение сочетанной регистрации ОАЭ и КСВПВ.
В соответствии с рекомендациями Joint Committee of Infant Hearing [39] новорожденным, находящимся в палатах интенсивной терапии более 5 дней, должна проводиться регистрация КСВП.
Учитывая то, что при повышенном уровне билирубина и/или низком весе при рождении может иметь место восстановление слуховой функции [10, 24], для принятия решения о реабилитации (имплантация) необходимо динамическое наблюдение. Кроме того, регистрация КСВП должна проводиться детям, в семье которых имелись нарушения слуха в детстве, а также детям с сенсорными моторными нейропатиями.
Слухопротезирование
На диагностическом этапе ситуация осложняется за счет того, что не регистрируются электрофизиологические ответы и приходится ориентироваться на поведенческие реакции ребенка на звуки и речь. При отсутствии динамики рекомендуется слухопротезирование.
При АН нарушается временная обработка и кодирование временных характеристик речи, что приводит к диссоциации результатов тональной и речевой аудиометрии. Учитывая то, что СА обеспечивают усиление, но не компенсируют дефицита временной обработки, результаты протезирования детей с АН всегда хуже, чем результаты у детей с сенсоневральной тугоухостью.
Исходя из предпосылки о том, что улучшение соотношения сигнал/шум у этих детей будет сопровождаться улучшением восприятия речи и развития языка [50], следует предусматривать использование FM-систем.
В соответствии с протоколом, принятым в 2008 г., больным рекомендуется использование линейного усиления (исключение компрессии), использование низкочастотной фильтрации или высокочастотной транспозиции.
Как было отмечено выше [9], у половины детей с АН слухопротезирование эффективно. У этих детей, в отличие от пациентов с отсутствием эффекта, регистрируются корковые СВП. В наших наблюдениях положительный эффект от электроакустической коррекции был отмечен у 38 больных (46,35%).
Современные технологии слухопротезирования определяют необходимость измерения RECD (различия в уровнях звукового давления, измеренные в реальном ухе и камере связи объемом 2 см3) и использования формул предписания усиления и выхода слухового аппарата (DSLv5, NAL), для чего обязательно измерение порогов слышимости. Однако если у детей с сенсоневральной тугоухостью пороги могут быть определены при регистрации частотно-специфичных КСВП или ССВП, то у детей с АН это невозможно. В результате этого определение поведенческих порогов производится в возрасте 6-9 мес.
Кохлеарная имплантация
При отсутствии эффекта от адекватного слухопротезирования (отсутствие прогресса в понимании речи и развитии слуховых и языковых навыков) вне зависимости от поведенческих порогов рекомендуется КИ.
Дополнительно к критериям отбора детей на КИ у больных с АН должны приниматься во внимание следующие факторы:
1. Учитывая то, что у ряда детей имеет место улучшение или восстановление слуха, наблюдаемое в возрасте до 2 лет, родители должны быть информированы об этом. Решение о КИ принимается только при отсутствии динамики поведенческих порогов и КСВП. До 2-летнего возраста должны использоваться подходы к ранней реабилитации, основанные на стимуляции восприятия и продукции речи.
2. Заключение о функциональной сохранности слухового нерва должно основываться на современных методиках МРТ.
3. Дети с отсутствием прогресса в восприятии и продукции речи должны рассматриваться в качестве кандидатов для КИ вне зависимости от порогов слышимости. КИ должно предшествовать слухопротезирование.
Особое внимание должно быть уделено предоперационному промонториальному тестированию (электрическая стимуляция). При наличии нормальных электрически вызванных КСВП исключается возможность нарушения процессов миелинизации. Процесс может быть локализован на уровне ВВК и синапсов.
КИ способствует улучшению временной обработки сигналов за счет вызывания синхронных разрядов волокон слухового нерва. Как правило, КСВП регистрируются в ответ на электрическую стимуляцию у имплантированных больных.
Во всех случаях, кроме процессов демиелинизации, методом выбора является кохлеарная имплантация [28].
Следует еще раз подчеркнуть, что у детей первого года жизни с прелингвальной глухотой вне зависимости от причин, вызвавших АН, показано слухопротезирование [15].