Аутоиммунное заболевание печени что это такое и как лечить
Аутоиммунный гепатит
Иммунолог Надежда Кнауэро патогенезе, клинике и лечении иммунного поражения печени
Аутоиммунный гепатит (АИГ) — это хроническое воспалительное заболевание печени, характеризующееся утратой иммунологической толерантности организма к тканевым антигенам [1, 2].
Впервые сведения о тяжелом поражении печени с выраженной желтухой и гиперпротеинемией появились в 30–40‑х гг. XX века. В 1950 г. шведский врач Ян Вальденстрем (Jan Waldenström) наблюдал у 6 молодых женщин хронический гепатит с желтухой, телеангиоэктазиями, повышением СОЭ, гипергаммаглобулинемией. Гепатит хорошо отвечал на лечение кортикотропином [3]. Из-за сходства лабораторных изменений с картиной системной красной волчанки (наличие антинуклеарных антител в сыворотке, положительные результаты LE-теста) одним из названий патологии стал «люпоидный гепатит».
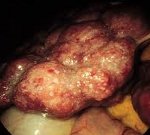
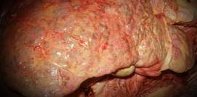
В настоящее время аутоиммунный гепатит определяют как хронический, преимущественно перипортальный гепатит с лимфоцитарно-плазмоцитарной инфильтрацией и ступенчатыми некрозами (рис. 1). Характерные проявления: гипергаммаглобулинемия, появление аутоантител в крови.
Классификация
В зависимости от вида аутоантител выделяют три типа заболевания:
Некоторые авторы объединяют АИГ 1 и АИГ 3 в силу сходства клинико-эпидемиологических особенностей [4].Существуют также перекрестные формы (overlap syndrome) различных аутоиммунных патологий печени, включающие в себя АИГ: АИГ+ПБЦ (первичный билиарный цирроз), АИГ+ПСХ (первичный склерозирующий холангит). Пока не вполне ясно, следует ли считать эти заболевания параллельно текущими самостоятельными нозологиями или частями непрерывного патологического процесса.
В качестве отдельной нозологии рассматривается АИГ, развившийся de novo после трансплантации печени, выполненной по поводу печеночной недостаточности, связанной с другими заболеваниями [1, 5].
Аутоиммунный гепатит встречается повсеместно. Распространенность АИГ в европейских странах — около 170 случаев на 1 млн населения. При этом до 80 % всех случаев составляет АИГ 1 типа. АИГ 2 типа распространен неравномерно — до 4 % в США и до 20 % в Европе.
Болеют преимущественно женщины (соотношение полов среди пациентов в странах Европы составляет 3–4:1). Возраст заболевших — от 1 года до 80 лет, средний возраст — около 40 лет [6].
Этиопатогенез
Этиология АИГ неизвестна, однако считается, что на развитие заболевания влияют как генетические факторы, так и факторы окружения.
Важным звеном патогенеза могут быть определенные аллели генов HLA II (человеческий лейкоцитарный антиген типа II, Human leucocyte antigen II) и генов, связанных с регуляцией деятельности иммунной системы [7, 8].
Отдельно стоит сказать об АИГ, входящем в клиническую картину аутоиммунного полиэндокринного синдрома (autoimmune polyendocrine syndrome, autoimmune polyendocrinopathy-candidiasis-ectodermal dystrophy, APECED). Это моногенное заболевание с аутосомно-рецессивным наследованием, связанное с мутацией в гене AIRE1. Таким образом, в данном случае генетическая детерминированность является доказанным фактом [4, 9].
Аутоиммунный процесс при АИГ представляет собой Т-клеточный иммунный ответ, сопровождающийся образованием антител к аутоантигенам и воспалительным повреждением тканей.
Факторы патогенеза АИГ:
Клиника
Примерно у четверти больных АИГ начинается остро, описаны даже редкие случаи развития острой печеночной недостаточности. Острый гепатит с желтухой чаще встречается у детей и молодых людей, у этой же группы чаще отмечается фульминантное течение заболевания [6].
Следует отметить, что у некоторых пациентов с явлениями острого АИГ в отсутствие лечения может наблюдаться спонтанное улучшение состояния и нормализация лабораторных показателей. Однако через несколько месяцев обычно наступает повторный эпизод АИГ. Гистологически также определяется персистирующий воспалительный процесс в печени [6].
Чаще клиника АИГ соответствует клинике хронического гепатита и включает в себя такие симптомы, как астения, тошнота, рвота, боли или дискомфорт в правом верхнем квадранте живота, желтуха, порой сопровождающаяся кожным зудом, артралгии, реже — пальмарная эритема, телеангиэктазии, гепатомегалия [2, 6]. При развившемся циррозе печени могут превалировать симптомы портальной гипертензии, явления энцефалопатии.
АИГ может быть сопряжен с аутоиммунными заболеваниями различных профилей:
Диагностика АИГ
Диагностика аутоиммунного гепатита основывается на:
Необходимо помнить о вероятном АИГ у пациентов с повышением уровня печеночных ферментов, а также у пациентов с циррозом печени. При наличии признаков холестаза в круг патологий для проведения дифференциального диагноза следует включить первичный билиарный цирроз и первичный склерозирующий холангит.
Клинический поиск включает в себя определение таких лабораторных показателей, как активность аланинаминотрансферазы и аспартатаминотрансферазы (АЛТ и АСТ), щелочной фосфатазы (ЩФ), уровень альбумина, гамма-глобулина, IgG, билирубина (связанного и несвязанного). Необходимо также определение уровня аутоантител в сыворотке крови и получение данных гистологического исследования [9].
Методы визуальной диагностики (УЗИ, КТ, МРТ) не имеют решающего вклада в диагностику АИГ, однако позволяют установить факт прогрессии АИГ и исход в цирроз печени, а также исключить наличие очаговой патологии.В целом диагностика базируется на 4 пунктах [10]:
Лечение аутоиммунного гепатита
АИГ относится к заболеваниям, при которых лечение позволяет существенно повысить выживаемость больных.
Показаниями для начала лечения служат:
Менее выраженные отклонения в лабораторных показателях в сочетании с менее выраженной клиникой являются относительным показанием к лечению. При неактивном циррозе печени, наличии признаков портальной гипертензии в отсутствие признаков активного гепатита, при «мягком» гепатите со ступенчатыми некрозами и без клинических проявлений лечение не показано [1, 9].
Общая концепция терапии при АИГ предполагает достижение и поддержание ремиссии. Базовой является иммуносупрессивная терапия — глюкокортикостероиды (преднизолон) в качестве монотерапии или в сочетании с азатиоприном [2, 6, 9, 11]. Терапия продолжается до достижения ремиссии, причем важно достичь именно гистологически подтвержденной ремиссии, которая может отставать от нормализации лабораторных показателей на 6–12 мес. Лабораторная же ремиссия описывается как нормализация уровня АСТ, АЛТ, гамма-глобулина, IgG [2].
Поддерживающую терапию более низкими дозами иммуносупрессантов для снижения вероятности рецидива после достижения ремиссии проводят по крайней мере в течение 2 лет.
Кроме того, обсуждается возможность применения препаратов урсодезоксихолевой кислоты (УДХК)при аутоиммунном гепатите в качестве сопутствующей терапии или даже монотерапии [11]. АИГ у пациентов, получавших препараты УДХК при моно- и комбинированной терапии, характеризовался более мягким течением и ускоренной нормализацией лабораторных показателей.
Ответ на лечение
Результаты лечения преднизолоном и азатиоприном при АИГ могут быть следующими:
О рецидиве заболевания говорят, когда после достижения полного ответа вновь появляются клинические симптомы и ухудшаются лабораторные показатели.
Обычно терапия дает хороший эффект, однако у 10–15 % больных она не приводит к улучшению, хотя и хорошо переносится. Причинами неэффективности терапии могут служить [6]:
В качестве альтернативных препаратов для лечения аутоиммунного гепатита используют и другие иммуносупрессоры: будесонид, циклоспорин, циклофосфамид, микофенолата мофетил, такролимус, метотрексат [1, 2, 6, 11].
Клинический случай
Девочка восьми лет наблюдалась по поводу кожных высыпаний (эритематозные и нодулярные элементы без какого‑либо отделяемого на нижних конечностях), беспокоящих ее в течение 5–6 мес. Два месяца использовала местные средства от экземы, улучшения не было. Позднее возникли дискомфорт в эпигастральной области, слабость, периодически — тошнота и рвота.
Высыпания локализовались на ногах. При гистологическом исследовании кожного биоптата выявлена инфильтрация подкожной жировой клетчатки лимфоцитами без признаков васкулита. Данные явления были расценены как узловатая эритема.При осмотре выявлена невыраженная гепатоспленомегалия, в остальном соматический статус — без выраженных особенностей, состояние стабильное.
По результатам лабораторных исследований:
Показатели системы гемостаза (протромбиновое время, международное нормализованное отношение), уровень общего белка, сывороточного альбумина, гамма-глобулина, уровень ферритина, церулоплазмина, альфа-антитрипсина, гамма-глутамилтранспептидазы — в пределах референсных значений.
В сыворотке крови не выявлены HBs-антиген, антитела к HBs, HBc, антитела к вирусу гепатита А и С. Также отрицательными были тесты на цитомегаловирус, вирус Эпштейна — Барр, токсоплазму, бруцеллу. Титр АСЛ-О в пределах нормы.Данных за сахарный диабет, тиреоидит, болезнь Грейвса, пролиферативный гломерулонефрит — не выявлено.
При УЗИ органов брюшной полости визуализировалась увеличенная печень с измененной эхоструктурой, без признаков портальной гипертензии и асцита. Офтальмологический осмотр не выявил наличия кольца Кайзера — Флейшера.
Титр антител anti-SMA — 1:160, ANA, AMA, anti-LKM-1 антитела не выявлены. Пациентка позитивна по гаплотипам HLA DR3, HLA DR4.
При гистологическом исследовании биоптата печени зафиксированы фиброз, лимфоцитарная инфильтрация, образование розеток гепатоцитов и другие признаки хронического аутоиммунного гепатита.
Пациентке выставлен диагноз «аутоиммунный гепатит 1 типа, ассоциированный с узловатой эритемой», начата терапия преднизолоном и азатиоприном. Счет по шкале IAIHG составлял 19 баллов до начала лечения, что характеризуется как «достоверный АИГ».
Через 4 недели терапии отмечалось купирование общеклинической симптоматики, нормализация лабораторных показателей. Через 3 месяца терапии кожные высыпания полностью регрессировали. Через 6 месяцев после окончания терапии состояние пациентки было удовлетворительным, лабораторные показатели — в пределах референсных значений.
Адаптировано из Kavehmanesh Z. et al. Pediatric Autoimmune Hepatitis in a Patient Who Presented With Erythema Nodosum: A Case Report. Hepatitis monthly, 2012. V. 12. — N. 1. — P. 42–45.
Таким образом, АИГ — это достаточно редкое и относительно хорошо поддающееся лечению заболевание. На фоне внедрения современных протоколов иммуносупрессивной терапии 10‑летняя выживаемость больных достигает 90 %. Менее благоприятен прогноз у больных с аутоиммунным гепатитом 2 типа, особенно у детей и подростков, у которых АИГ прогрессирует гораздо быстрее, а эффективность терапии в целом ниже. Следует помнить и о риске развития гепатоцеллюлярной карциномы (4–7 % в течение 5 лет после установления диагноза цирроза печени).
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.
Аутоиммунный гепатит ( Люпоидный гепатит )
Аутоиммунный гепатит – это прогрессирующее хроническое воспаление печени, протекающее с признаками перипортального или более обширного поражения и наличием аутоантител к печеночным клеткам. Клинические проявления включают астеновегетативные расстройства, желтуху, боли в правом подреберье, кожные сыпи, гепатомегалию и спленомегалию, аменорею у женщин, гинекомастию – у мужчин. Диагностика основывается на серологическом выявлении антинуклеарных антител (ANA), тканевых антител к гладкой мускулатуре (SMA), антител к микросомам печени и почек и др., гипергаммаглобулинемии, увеличения титра IgG, а также данных биопсии печени. Основу лечения составляет иммуносупрессивная терапия глюкокортикостероидами.
МКБ-10
Общие сведения
Причины
Патогенез
Основу патогенеза аутоиммунного гепатита составляет дефицит иммунорегуляции: снижение субпопуляции Т-супрессорных лимфоцитов, что приводит к неуправляемому синтезу В-клетками IgG и разрушению мембран клеток печени – гепатоцитов, появлению характерных сывороточных антител (ANA, SMA, анти-LKM-l).
Классификация
В зависимости от образующихся антител различают аутоиммунный гепатит I (анти-ANA, анти-SMA позитивный), II (анти-LKM-l позитивный) и III (анти-SLA позитивный) типов. Каждый из выделяемых типов заболевания характеризуется своеобразным серологическим профилем, особенностями течения, откликом на иммуносупрессивную терапию и прогнозом.
К вариантам атипичного аутоиммунного гепатита относят перекрестные синдромы, включающие также признаки первичного билиарного цирроза, первичного склерозирующего холангита, хронического вирусного гепатита.
Симптомы аутоиммунного гепатита
В большинстве случаев патология манифестирует внезапно и в клинических проявлениях не отличается от острого гепатита. Вначале протекает с выраженной слабостью, отсутствием аппетита, интенсивной желтухой, появлением темной мочи. Затем в течение нескольких месяцев разворачивается клиника аутоиммунного гепатита. Реже начало заболевания постепенное; в этом случае преобладают астеновегетативные расстройства, недомогание, тяжесть и боли в правом подреберье, незначительная желтуха. У части пациентов аутоиммунный гепатит начинается с лихорадки и внепеченочных проявлений.
Период развернутых симптомов аутоиммунного гепатита включает выраженную слабость, чувство тяжести и боли в правом подреберье, тошноту, кожный зуд, лимфаденопатию. Для аутоиммунного гепатита характерны непостоянная, усиливающаяся в периоды обострений желтуха, увеличение печени (гепатомегалия) и селезенки (спленомегалия). У трети женщин при аутоиммунном гепатите развивается аменорея, гирсутизм; у мальчиков может наблюдаться гинекомастия. Типичны кожные реакции: капиллярит, пальмарная и волчаночноподобная эритема, пурпура, акне, телеангиэктазии на коже лица, шеи и рук. В периоды обострений аутоиммунного гепатита могу наблюдаться явления преходящего асцита.
К системным проявлениям аутоиммунного гепатита относится рецидивирующий мигрирующий полиартрит, затрагивающий крупные суставы, но не приводящий к их деформации. Достаточно часто аутоиммунный гепатит протекает в сочетании с язвенным колитом, миокардитом, плевритом, перикардитом, гломерулонефритом, тиреоидитом, витилиго, инсулинозависимым сахарным диабетом, иридоциклитом, синдромом Шегрена, синдромом Кушинга, фиброзирующим альвеолитом, гемолитической анемией.
Диагностика
Аутоиммунный гепатит диагностируется в ходе консультации гепатолога или гастроэнтеролога. Критериями патологии служат серологические, биохимические и гистологические маркеры. Согласно международным критериям, об аутоиммунном гепатите можно говорить в случае, если:
Биопсия печени с морфологическим исследованием образца тканей позволяет выявить картину хронического гепатита с признаками выраженной активности. Гистологическими признаками аутоиммунного гепатита служат мостовидные или ступенчатые некрозы паренхимы, лимфоидная инфильтрация с обилием плазматических клеток. Инструментальные исследования (УЗИ печени, МРТ печени и др.) при аутоиммунном гепатите не имеют самостоятельного диагностического значения.
Лечение аутоиммунного гепатита
Патогенетическая терапия заболевания заключается в проведении иммуносупрессивной терапии глюкокортикостероидами. Такой подход позволяет снизить активность патологических процессов в печени: повысить активность Т-супрессоров, уменьшить интенсивность аутоиммунных реакций, разрушающих гепатоциты.
Обычно иммуносупрессивная терапия при аутоиммунном гепатите проводится преднизолоном или метилпреднизолоном в начальной суточной дозе 60 мг (1-ю неделю), 40 мг (2-ю неделю), 30 мг (3-4-ю недели) со снижением до 20 мг в качестве поддерживающей дозы. Уменьшение суточной дозировки проводят медленно, учитывая активность клинического течения и уровень сывороточных маркеров. Поддерживающую дозу пациент должен принимать до полной нормализации клинико-лабораторных и гистологических показателей. Лечение аутоиммунного гепатита может продолжаться от 6 месяцев до 2-х лет, а иногда и на протяжении всей жизни.
При неэффективности монотерапии возможно введение в схему лечения аутоиммунного гепатита азатиоприна, хлорохина, циклоспорина. В случае неэффективности иммуносупрессивного лечения аутоиммунного гепатита в течение 4-х лет, множественных рецидивах, побочных эффектах терапии ставится вопрос и трансплантации печени.
Прогноз и профилактика
При отсутствии лечения аутоиммунного гепатита заболевание неуклонно прогрессирует; спонтанные ремиссии не наступают. Исходом аутоиммунного гепатита служит цирроз печени и печеночная недостаточность; 5-летняя выживаемость не превышает 50%. С помощью своевременной и четко проводимой терапии удается достичь ремиссии у большинства пациентов; при этом выживаемость в течение 20 лет составляет более 80%. Трансплантация печени дает результаты, сопоставимые с лекарственно достигнутой ремиссией, 5-летний прогноз благоприятен у 90% пациентов.
При аутоиммунном гепатите возможна лишь вторичная профилактика, включающая регулярное наблюдение гастроэнтеролога (гепатолога), контроль активности печеночных ферментов, содержания γ-глобулинов, аутоантител для своевременного усиления или возобновления терапии. Пациентам с аутоиммунным гепатитом рекомендуется щадящий режим с ограничением эмоциональных и физических нагрузок, соблюдение диеты, отвод от профилактической вакцинации, ограничение приема лекарственных препаратов.
АУТОИММУННЫЙ ГЕПАТИТ Варианты клинического течения. Принципы лечения
Патогенез АГ сложен. Полагают, что это ответ генетически предрасположенного организма на какой-то внешний агент, который является пусковым моментом в развитии аутоиммунных процессов, вызывающих прогрессирующие воспалительно-некротические изменени
 |
Патогенез АГ сложен. Полагают, что это ответ генетически предрасположенного организма на какой-то внешний агент, который является пусковым моментом в развитии аутоиммунных процессов, вызывающих прогрессирующие воспалительно-некротические изменения, приводящие к фиброзу и циррозу печени (ЦП). Генетически детерминированная предрасположенность к этому заболеванию выявлена во многих исследованиях. Доказано, что большая часть больных АГ имеют фенотип по антигенам главного комплекса гистосовместимости HLA-B8, HLA-DR4, DR3 и DR52a. Пусковой агент пока неизвестен, однако есть некоторые данные о роли вирусов гепатита [31, 26], кори [27], Эпштейн-Барр вируса [32], а также интерферона (ИФН) [14] как инициаторов начала АГ.
| Аутоиммунный гепатит (АГ) — хроническое воспалительное заболевание печени невыясненой этиологии, характеризующееся определенными лабораторными, клиническими и гистологическими признаками. Болеют им в основном женщины молодого возраста |
АГ — это прогрессирующее воспаление печени, характеризующееся наличием некрозов в перипортальной, септальной зонах (ступенчатые некрозы) или, более широко, лобулярным гепатитом (ЛГ), гипергаммаглобулинемией и аутоантителами в сыворотке крови [7]. Портальные тракты печени на биоптатах находят расширенными с накоплением в них обширных инфильтратов, имеющих разный клеточный состав: лимфоциты, макрофаги, плазматические клетки. ЛГ — дольковый гепатит, когда некрозы выявляются во второй и третьей зонах ацинусов, а также обнаруживается внутридольковая лимфоидноклеточная инфильтрация, которая выражена значительно больше, чем инфильтрация портальных трактов. ЛГ является частью гистологической картины АГ, если он выявляется одновременно с перипортальным гепатитом. По гистологической картине на АГ может указывать, кроме вышеперечисленного, наличие многоядерных гепатоцитов [2].
Наконец, картина фиброза может присутствовать в той или иной степени даже при умеренной степени активности АГ, а в запущенных случаях, особенно при отсутствии эффективной терапии, формируются мостовидные некрозы и, в конце концов, ЦП.
Хотя гистологическая картина при АГ очень характерна, все-таки она неспецифична. Отличительной чертой АГ является обнаружение в биоптатах преимущественно плазматических клеток, так как выраженная инфильтрация в портальной, перипортальной зоне, вовлечение в процесс долек печени — в равной мере присущи и хроническому вирусному гепатиту (ХВГ).
Одной из основных клинических характеристик АГ является обнаружение аутоантител к клеточным и субклеточным структурам клеток разных органов [22]. Типичным маркером АГ являются антитела к ядрам клеток — ANA. Из других маркеров выявляются антитела к клеткам гладкой мускулатуры (SMA), антитела к микросомам клеток печени и эпителиальных клеток клубочкового аппарата почек (LKM), антитела к растворимому печеночному антигену (SLA), антитела к антигенам (цитокератины 8, 18) мембран гепатоцитов — LMA.
Клинические проявления АГ очень разнообразны [1, 3, 4]. С одной стороны, встречаются бессимптомные формы, когда случайно выявляется повышение АЛТ, АСТ, а с другой — острое начало болезни с тяжелым течением вплоть до развития фульминантного гепатита (ФГ).
Нередко заболевание начинается незаметно с астеновегетативных проявлений, болей в области правого предреберья, незначительной желтухи. Однако у большинства больных АГ начало болезни острое, как при остром вирусном гепатите (ОВГ), и при осмотре пациента врач впервые выявляет признаки хронического гепатита (ХГ) — телеангиоэктазии, пальмарную эритему, увеличение печени и селезенки, а также изменения в анализах крови — гипергаммаглобулинемию, увеличение IgG, снижение содержания общего белка, резкое увеличение СОЭ. Лейкопения и тромбоцитопения наблюдаются у больных на поздних стадиях болезни или при развившихся гиперспленизме и синдроме портальной гипертензии.
Когда АГ впервые проявляется желтухой, как при ОВГ, приходится дифференцировать его от гепатитов А, В, Е и особенно С, при котором антитела в сыворотке крови могут появляться через достаточно продолжительное время после начала болезни. Желтуха у пациентов с АГ может быть разной степени выраженности, часто появляется на поздних стадиях заболевания, бывает непостоянной и усиливается в период обострений. В общем же у большинства больных чаще всего изменяются аминотрансферазы, нежели щелочная фосфотаза (ЩФ) или билирубин.
| Аутоиммунный гепатит был выделен из группы болезней печени и впервые описан как отдельная нозология в начале 50-х годов [33]. В научной литературе существовал под разными названиями. Термин люпоидный гепатит, который часто использовался в нашей стране, ввел в 1956 году Дж. Маккей с соавторами в журнале Lancet, так как при этом заболевании нередко в сыворотке крови больных выявлялись волчаночные клетки. Потом, в последующие годы, люпоидный, или классический, АГ стали называть аутоиммунным активным хроническим гепатитом, но в 1993 году Международная группа по изучению болезней печени предложила термин АГ, а также критерии установления его диагноза [17] |
Для АГ характерно поражение кожи в виде геморрагической сыпи, оставляющей после себя пигментацию. Из других симптомов встречаются волчаночная и узловатая эритемы, очаговая склеродермия, пальмарная эритема и телеангиоэктазии. У всех больных выявляются изменения в эндокринной системе — аменорея, угри, гирсутизм, стрии. Диагностическое значение отдельных симптомов болезни при АГ неодинаково. К наиболее значимым относятся длительная лихорадка и арталгии. В большинстве случаев АГ они присутствуют одновременно, являясь наиболее частыми и постоянно встречающимися жалобами больных [4].
Один из вариантов начала АГ — появление лихорадки с внепеченочными проявлениями, из которых следует назвать аутоиммунный тиреоидит, язвенный колит, гипертиреоидизм, гемолитическая анемия, идеопатическая тромбоцитопения, сахарный диабет, целиакия, полимиозит, фиброзирующий альвеолит, гломерулонефрит и т. д. Желтуха при этом варианте появляется позже [20].
Часто АГ сопровождается бесплодием, однако при возникновении беременности и последующих родах на фоне компенсированного процесса это не влияет на течение АГ и судьбу ребенка даже при постоянном приеме преднизолона (ПР) [30]. Беременность на стадии сформировавшегося ЦП и синдрома портальной гипертензии, которые выявляются у трети больных на момент выявления АГ, нежелательна [3].
В отличие от ХВГ течение АГ у больных непрерывно прогрессирующее, без самопроизвольных ремиссий. Улучшения самочувствия бывают кратковременными, нормализации биохимических процессов не происходит. Прогноз течения АГ хуже у пациентов с острым началом болезни по типу ОВГ, с наличием признаков холестаза, асцитом, повторными эпизодами острой печеночной энцефалопатии (ОПЭ). Как правило, больные, пережившие критический период, имеют лучший прогноз.
Диагноз АГ выставляется на основании соответствия лабораторных и гистологических данных, отсутствия маркеров ВГ, исключения злоупотребления алкоголем и контактов с препаратами крови, гипотоксическими веществами, повышения гамма-глобулинов не менее чем в 1,5 раза выше нормы. Повреждение желчных протоков, отложение меди, гемосидероз, при которых также могут выявляться ЛГ и ступенчатые некрозы, предполагают другую причину ХГ и исключают диагноз АГ. ANA, SMA и LRM-1 должны быть в титрах не менее 1:80 у взрослых и 1:20 у детей (рекомендации Международной группы, 1993).
Дифференциальный диагноз между АГ и другими аутоиммунными заболеваниями, в основном первичным билиарным циррозом (ПБЦ), первичным склерозирующим холангитом (ПСХ), ХВГ основывается на клинических, гистологических и иммунологических параметрах. Однако нередко выявляется так называемый overlap-синдром, когда одновременно у пациентов выявляются признаки АГ и вышеперечисленных хронических заболеваний печени. Далее они будут описываться как варианты АГ [7, 13]. Предполагаемый диагноз АГ в данном случае подразумевает сходство с клиникой АГ (жалобы на слабость, арталгии, миалгии), а биохимический анализ крови отражает преимущественно изменения холестатического порядка, имеет место кожный зуд разной степени выраженности. Пациенты с такими вариантами АГ могут быть обоего пола, любого возраста, но все же чаще это женщины в возрасте до 40 лет и моложе. На гистологии находят перипортальный гепатит с или без ЛГ, часто с поражением желчных протоков, жировой дистрофией гепатоцитов и лимфоидной инфильтацией портальных трактов в виде гранулем [7, 10].