Аутоиммунный панкреатит что это
Аутоиммунный панкреатит
Аутоиммунный панкреатит – воспалительное заболевание поджелудочной железы с характерными клиническими и гистологическими особенностями, в развитие которого вовлечены аутоиммунные механизмы.
Аутоиммунный панкреатит – системное заболевание, при котором могут поражаться другие органы. Может иметь диффузную и очаговую форму, при очаговой форме проявления заболевания сходны с раком поджелудочной железы.

Заподозрить заболевание можно при возникновении следующих симптомов:
При обнаружении одного или нескольких таких признаков, рекомендуется обратиться к врачу. Специалист оценит ситуацию и назначит дообследование.
При подозрении на аутоиммунный панкреатит выполняют комплексную диагностику.
Для диагностики аутоиммунного панкреатита проводятся лабораторные исследования: в том числе определение иммуноглобулинов G4 в сыворотке крови, а также инструментальные исследования: ультразвуковое исследование органов брюшной полости, мультиспиральная компьютерная томография с внутривенным болюсным контрастированием, при необходимости – эндоскопическая ультрасонография, магнитно-резонансная холангиопанкреатография.
В Московском клиническом научно-практическом центре им. А.С. Логинова диагностика и лечение аутоиммунного панкреатита осуществляется совместными усилиями врачей гастроэнтерологов, эндокринологов, хирургов, специалистов лучевой диагностики и патоморфологов. Раннее обращение к нашим специалистам позволяет своевременно установить диагноз и начать лечение. Лечение аутоиммунного панкреатита провидится с применением глюкокортикостероидов и других иммуносупрессивных препаратов. В отличие от других форм панкреатита, при аутоиммунном панкреатите возможно восстановление нарушенных функций поджелудочной железы.
Не откладывайте свой визит к специалистам нашего Центра. Это поможет своевременно диагностировать заболевание и правильно выбрать тактику лечения. Врачи отделения патологии поджелудочной железы и желчевыводящих путей ГБУЗ МКНЦ имени А.С. Логинова ДЗМ всегда готовы Вам помочь.
Аутоимунный панкреатит: клинический случай
Аутоиммунный панкреатит
В нашем центре «Клиника Эксперт Курск» проведено исследование пациента со сложно диагностируемой патологией поджелудочной железы – аутоиммунным панкреатитом.
Анамнез, жалобы:
Мужчина 72 лет, активных жалоб не предъявлял. При более подробном сборе анамнеза удалось выяснить, что периодически пациента беспокоят боли в животе, уровень глюкозы крови повышается до 7-7,5 ммоль/л. Онкоанамнез отрицает. До проведения МРТ органов брюшной полости и забрюшинного пространства пациент проходил УЗ-исследование (не в нашей клинике); заключение – псевдоопухолевая форма панкреатита.
Что выявили при МРТ исследовании:
Диффузное (на всем протяжении) увеличение в размерах поджелудочной железы, сглаженность ее наружного контура, деформация формы железы по типу «сосискообразной». При этом МР-признаков наличия дополнительных объемных образований в поджелудочной железе по данным нативного и постконтрастного исследований выявлено не было. Проток поджелудочной железы неравномерно сужен на всем протяжении. Общий желчный проток (холедох) сужен в своей нижней трети и неравномерно расширен в вышележащих отделах.
Помимо этого в обеих почках были выявлены многочисленные дополнительные образования неправильно округлой формы с достаточно четкими ровными контурами, имеющими однородную низкую интенсивность во всех режимах сканирования.
При этом увеличенные лимфоузлы, объемные образования другой локализации на уровне визуализации не определялись.
Что обсуждалось нами на скайп-планерке по данному случаю:
Совместно с докторами наших операционных компаний мы провели обсуждение по данному сложному случаю. Врачами наших ОК были выявлены все вышеописанные структурные изменения, в ходе дальнейшего обсуждения нам удалось прийти к единому мнению.
Среди различных заболеваний, которые могут давать похожую МР-картину, был построен дифференциальный ряд: а) псевдоопухолевый панкреатит; б) острый панкреатит с увеличением в размерах поджелудочной железы; в) опухоль поджелудочной железы с наличием вторичных (метастатических) изменений в почках; г) псевдотуморозный панкреатит, который, в первую очередь, имеет панкреатические (в поджелудочной железе) изменения, но также и внепанкреатические – в частности, множественные очаговые изменения ткани почек.
К каким выводам пришли на скайп-планерке:
Из полученного дифференциального ряда врачи ОК последовательно исключали отдельные заболевания. Выявили, что для острого панкреатита не характерно отсутствие отека вокруг поджелудочной железы, несоответствие клинических данных предполагаемому диагнозу. Для опухоли поджелудочной железы не характерна однородность ткани железы, отсутствие данных за очаговое ее поражение, а также наличие суженного протока поджелудочной железы (при опухолях, как правило, расширен); также четкость контуров и однородность структуры очаговых изменений почек не характерна для метастатического поражения.
Что дал метод МРТ в данном случае:
Возможность с очень высокой достоверностью предположить аутоиммунный характер изменений поджелудочной железы, исключить ее опухолевое поражение. С учетом аутоиммунного характера заболевания данные пациенты нуждаются в гормональной терапии (глюкокортикостероидами), после которого наступает улучшение состояния. Такую терапию не проводят при других заболеваниях из выставленного первоначально дифференциально-диагностического ряда.
Интересно, что в данном случае наличие изменений вне поджелудочной железы (почках) помогает поставить правильный диагноз аутоиммунного поражения железы. Характер изменений в почках при этом – очаговые аутоиммунные лимфоцитарные инфильтраты.
Зачастую, по данным медицинских источников, неверно поставленный диагноз рака поджелудочной железы может привести к неоправданному оперативному вмешательству и удалению части железы (резекции) или направлению пациента на лечение к врачу-онкологу, что также необоснованно.
Что необходимо для окончательного подтверждения/верификации диагноза: биопсия и морфологическое дообследование.
На представленных Т2-изображениях в аксиальной (слева) и корональной (справа) проекциях, определяется увеличение в размерах и «сосискообразная» деформация поджелудочной железы; наличие многочисленных однотипных очаговых образований почек.
Аутоиммунный панкреатит что это
Измерение концентрации подкласса иммуноглобулина IgG4 в сыворотке крови используется для диагностики аутоиммунного панкреатита, заболевания, характеризующегося поражением ткани поджелудочной железы с развитием хронического панкреатита.
Аутоиммунный панкреатит (АИП), иммуноглобулин G4, IgG4.
Синонимы английские
Autoimmune pancreatitis (AIP), immunoglobulin G4, IgG4.
Иммуноферментный анализ (ИФА).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
В соответствии с международными согласованными диагностическими критериями (ICDC), данная форма заболевания относится к аутоиммунному панкреатиту (АИП) 1-го типа и является IgG4-ассоциированным заболеванием. В то время как для АИП 2-го типа характерна нейтрофильная инфильтрация протоков поджелудочной железы, но без инфильтрации IgG4 секретирующими плазматическими клетками и без увеличения уровня IgG4 в сыворотке крови.
К наиболее характерным симптомам АИП относятся желтуха подпеченочной этиологии, боли в животе, симптомы острого панкреатита, стеаторея, развитие сахарного диабета. Также может отмечаться поражение других органов и систем: воспалительный и фиброзирующий процесс в желчных протоках, протоках слюнных желез, ретроперитонеальный фиброз, сопровождающийся болью в спине, увеличение медиастинальных и абдоминальных лимфатических узлов, поражение почек с формированием гидронефроза.
Для выявления концентрации подкласса IgG4 в сыворотке крови пациентов с подозрением на АИП используется метод твердофазного иммуноферментного анализа (ИФА). Для АИП 1-го типа диагностическая чувствительность данного метода составляет 44-95 %. В случаях когда уровни IgG4 в норме, может быть рекомендовано дополнительное обследование на выявление антинуклеарных антител, в частности антинуклеарного фактора, и антител к цитоплазме нейтрофилов.
Следует отметить, что повышение уровня IgG4 в сыворотке крови отмечается также у больных хроническим панкреатитом, при раке поджелудочной железы, холангиокарциноме, при других IgG4-ассоциированных заболеваниях (ретроперитонеальный фиброз, синдром Микулича).
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Референсные значения: 0,1-1,35 г/л.
Что может влиять на результат?
21 Антинуклеарный фактор на HEp-2 клетках
21 Антитела к цитоплазме нейтрофилов, IgG (с определением типа свечения)
6 Амилаза общая в сыворотке
6 Амилаза панкреатическая
8 Гликированный гемоглобин (HbA 1c)
Кто назначает исследование?
Терапевт, врач общей практики, гастроэнтеролог, эндокринолог, ревматолог.
IgG4-ассоциированный панкреатит – трудности диагностики и лечения

На сегодняшний день IgG4-ассоциированный панкреатит – аутоиммунный панкреатит 1-го типа является достаточно редко встречающимся заболеванием поджелудочной железы, которое вызывает большие трудности в выборе лечебно-диагностической тактики как у хирургов,
Abstract. To date, IgG4-associated pancreatitis – type 1 autoimmune pancreatitis is a fairly rare disease of the pancreas, which causes great difficulties in the choice of therapeutic and diagnostic tactics for both surgeons and gastroenterologists. The disease is poorly understood and rarely discussed in routine clinical practice. Although, perhaps, in fact, the number of such patients is significantly greater. The prevailing etiological variant of the development of autoimmune pancreatitis remains the theory of lymphocyte activation under the influence of IgG4, which is normally one of the smallest immunoglobulins of class G, exhibiting both pro-inflammatory and anti-inflammatory activity. The inflammatory process caused by activated IgG4-positive leukocytes is characterized by the development of a diffuse or local process due to pronounced infiltration by lymphocytes and plasma cells, followed by their activation into fibroblasts and the formation of focal fibrosis. In the presented clinical case, we tried to describe all the difficulties faced by the patient, his family and friends, his attending physicians. A disease that developed over the years and led to a traumatic operation, the diagnosis – the setting of which required many years of diagnostic search, a treatment that allowed to save life and improve its quality, but due to delay, it turned out to be insufficient to fully rehabilitate the patient. For citation: Cherepnin M. A., Serova E. V., Berdnikov S. I., Chuprakov E. V., Govorina Yu. B. IgG4-associated pancreatitis difficulties of diagnostics and treatment // Lechaschy Vrach. 2021; 2 (24): 35-37. DOI: 10.26295/OS.2021.11.17.007
Резюме. На сегодняшний день IgG4-ассоциированный панкреатит – аутоиммунный панкреатит 1-го типа является достаточно редко встречающимся заболеванием поджелудочной железы, которое вызывает большие трудности в выборе лечебно-диагностической тактики как у хирургов, так и гастроэнтерологов. Заболевание является недостаточно изученным и редко обсуждаемым в рутинной клинической практике. Хотя, возможно, на самом деле число таких пациентов значимо больше. Превалирующим этиологическим вариантом развития аутоиммунного панкреатита остается теория активации лимфоцитов под действием IgG4, который в норме является одним из самых малочисленных иммуноглобулинов класса G, проявляющим как провоспалительную, так и противовоспалительную активность. Воспалительный процесс, вызванный активированными IgG4-положительными лейкоцитами, характеризуется развитием диффузного или локального процесса, обусловленного выраженной инфильтрацией лимфоцитами и плазмоцитами, с последующей активацией их в фибробласты и формированием очагового фиброза. В представленном клиническом случае мы постарались описать все сложности, с которыми столкнулись пациент, его родные и близкие, его лечащие врачи. Заболевание развивалось годами и привело к травмирующей операции, постановка диагноза потребовала многих лет диагностического поиска, лечение позволило сохранить жизнь и улучшить ее качество, но из-за несвоевременности оказалось недостаточным, чтобы полностью реабилитировать пациента.
Первые описания клинических случаев аутоиммунного панкреатита появились еще в 1892 г. в работах Mikulicz и соавторов [1]. Таким образом это заболевание получило название «болезнь Микулича». За вековую историю название заболевания трансформировалось в лимфоплазмоцитарный склерозирующий панкреатит (LPSP) – Kawaguchi и соавторы [2]. В течение последних 50 лет, с развитием иммунологии и лабораторной диагностики, IgG4-ассо-циированные заболевания обособились как класс и получили свое современное название.
Поражение поджелудочной железы также носит название аутоиммунного панкреатита (АИП) 1-го типа, так как исторически именно изучение опухолевидного фиброза поджелудочной железы дало начало исследованиям IgG4-ассоциированных заболеваний других органов. На сегодняшний день известно о возможном поражении практически любого органа заболеваниями данной этиологии [3, 4].
Согласно данным разных авторов, заболеваемость аутоиммунным панкреатитом составляет от 4,8-5,8% (0,71 случая на 100 тысяч населения) [5] до 5-7% и 3-11% [6, 7], при этом мужчины болеют в 1,5-2 раза чаще женщин с преобладающей возрастной группой старше 40-45 лет. В структуре хронических панкреатитов всех этиологий АИП 1-го и 2-го типа составляет до 5%. Примерно у 5% пациентов с подозрением на рак поджелудочной железы в итоге диагностируют АИП 1-го и 2-го типа [8].
Этиология этого заболевания до сих пор не ясна. Превалирующим этиологическим вариантом развития АИП остается теория активации лимфоцитов под действием IgG4 – одного из субклассов иммуноглобулинов класса G. IgG4 в норме является одним из самых малочисленных иммуноглобулинов класса G, его роль до конца не изучена, известно только, что он проявляет как провоспалительную, так и противовоспалительную активность. Воспалительный процесс, вызванный активированными IgG4-положительными лейкоцитами, характеризуется развитием диффузного или локального процесса, обусловленного выраженной инфильтрацией лимфоцитами и плазмоцитами, с последующей активацией их в фибробласты и формированием очагового фиброза [9].
Клиническая картина варьирует в широких пределах в зависимости от комбинации пораженных органов и выраженности симптомов. Большая часть известных случаев характеризуется хорошим ответом на терапию иммуносупрессантами.
На сегодняшний день имеются рекомендации:
Перечисленные рекомендации послужили критериями постановки диагноза и выбора тактики лечения больного в описываемом клиническом случае.
Мировая практика показывает, что первым врачом, к которому обращается пациент с этим заболеванием за помощью, будет хирург, онколог или терапевт. Поэтому осведомленность об этой патологии именно специалистов общей практики является ключевой для постановки диагноза на ранних этапах.
Также диагноз IgG4-ассоциированной патологии остается не рутинным ввиду крайне редкого применения лабораторного маркера из-за высокой стоимости: речь идет об исследовании на уровень IgG4 крови, для первичной диагностики также подходит анализ на общий IgG, который дешевле, но менее специфичен.
В представленном клиническом случае мы постарались описать все сложности, с которыми столкнулись пациент, его родные и близкие, а также лечащие врачи. Заболевание развивалось годами и привело к травмирующей операции, постановка диагноза потребовала многих лет диагностического поиска, лечение позволило сохранить жизнь и улучшить ее качество, но из-за несвоевременности оказалось недостаточным, чтобы полностью реабилитировать пациента.
Пациент 43 лет был направлен хирургом после курса стационарного лечения к терапевту-гастроэнтерологу для амбулаторного обследования и лечения.
При обращении: жалобы на боли в эпигастральной области после приема пищи с иррадиацией в спину и правое подреберье, клиника диспептического синдрома, периодически – субфебрильная температура тела, снижение его массы за последние 3 месяца на 10 кг, полифекалия, неоформленный стул, метеоризм. Профессиональные вредности исключены, пациент работает спортивным тренером, ведет здоровый образ жизни: опросник AUDIT не показал алкогольной зависимости, курение отрицает.
При расспросе выяснилось, что история заболевания уходит в далекий 1996 г., когда в связи с выраженными болями в животе пациент впервые был экстренно госпитализирован в хирургическое отделение одного из стационаров г. Красноярска, где ему был выставлен диагноз: острый идиопатический панкреатит, холангит неясной этиологии, стриктура нижней трети общего желчного протока. Из-за отсутствия эффекта от патогенетической и симптоматической консервативной терапии была выполнена хирургическая операция: лапаротомия, панкреатоеюностомия, холедоходуоденостомия. Со слов пациента, после операции оперировавший хирург сказал: «Твоя поджелудочная, как у старика 70 лет». На тот момент пациенту было всего 20 лет. После проведенного лечения отмечалась клиническая ремиссия – стойкий болевой синдром в эпигастрии отсутствовал. В последующем на диспансерном учете пациент не состоял, за медицинской помощью не обращался.
В конце августа 2019 г. боли в эпигастрии возникли вновь, столь сильные, что потребовали обращения в хирургическое отделение. Было выявлено повышение диастазы мочи до 1600 ЕД/л, амилазы крови – до 800 ЕД/л. Ультра-сонография брюшной полости: эхо-картина острого панкреатита, жидкость в сальниковой сумке. С подозрением на панкреонекроз пациента госпитализировали в хирургическое отделение. Проведена консервативная терапия – инфузионная, секретолитическая, спазмолитическая, симптоматическая. Эффект от лечения положительный – боли в животе уменьшились, но не были купированы до конца. На момент выписки показатели биохимического анализа крови нормализовалась, но боли сохранялись. Пациенту рекомендована плановая консультация терапевта-гастроэнтеролога.
Через неделю после выписки пациент был вынужден вновь обратиться за медицинской помощью из-за сохраняющегося болевого синдрома, снижения массы тела и повышения температуры до 37,5-38,5 °С. Повторно госпитализирован в другое хирургическое отделение.
При ультрасонографии брюшной полости выявлено объемное образование в проекции головки и тела поджелудочной железы с признаками деструкции и абсцедирования. В анализах крови отмечалась эритропения, С-реактивный белок – 10 мг/л, гипопротеинемия – до 58 г/л. Для уточнения диагноза выполнена магнитно-резонансная томография брюшной полости с холангиографией и забрюшинного пространства: объемное образование в панкреатодуоденальной зоне размерами 8,0 × 7,8 × 4,6 см (вероятно, соответствует инфильтрату) с признаками абсцедирования; признаки острого панкреатита, отечная форма, нарушения холединамики, признаки конкрементов в области шейки, в просвете холедоха; умеренная гепатоспленомегалия; единичные мелкие паренхиматозные кисты обеих почек.
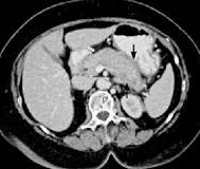
Решался вопрос о необходимости оперативного вмешательства по поводу абсцесса поджелудочной железы. Дополнительно выполнена мультиспиральная компьютерная томография и эндосонография. По результатам эндосонографии: состояние после наложения холедоходуоденоанастомоза. Эхо-эндоскопическая картина наиболее вероятно соответствует воспалительному процессу головки поджелудочной железы с деструкцией (инфильтрат с абсцедированием?) (рис.). Эхо-признаки хронического панкреатита. Конкременты, сладж желчного пузыря. Диффузные изменения печени.
Однако по результатам мультиспиральной компьютерной томографии признаков абсцесса поджелудочной железы обнаружено не было. Вопрос о дальнейшей тактике ведения пациента остался открытым.
После консультации гастроэнтеролога для уточнения генеза воспалительного процесса проведен прокальцитониновый тест, оказавшийся отрицательным, что в совокупности с положительным тестом на С-реактивный белок указывает на неинфекционную природу заболевания. Из-за имевшегося ранее в анамнезе холангита предположена аутоиммунная природа заболевания. Пациенту рекомендовано пройти тест на антитела к митохондриям АМА-М2 – тест на склерозирующий холангит, ANA (отрицательный, менее 1/40), ANCA (отрицательный) и IgG4 – маркер аутоиммунного инфильтрата забрюшинного пространства и/или маркер аутоиммунного панкреатита 1-го типа, эластазу стула: 10 мкг/г – выраженная экзокринная недостаточность поджелудочной железы.
Тесты подтвердили предварительный диагноз – антитела были в 2 раза выше нормы. Согласно международным критериям диагностики АИП 1-го типа [16, 17] был выставлен диагноз «IgG4-ассоциированная болезнь поджелудочной железы». Пациенту назначена терапия метилпреднизолоном в дозе 40 мг/сут с последующим снижением по 4 мг до полной отмены [18].
Сопутствующая терапия была обусловлена хроническим болевым синдромом (амитриптилин в дозе 50 мг в сутки по рекомендации невролога) и тяжелой экзокринной недостаточностью поджелудочной железы (панкреатин – 50 000 ЕД липазы в каждый прием пищи, урсодезоксихолевая кислота – 500 мг в сутки).
На фоне проведенной терапии через 1 месяц удалось уменьшить объем образования по данным мультиспиральной компьютерной томографии в 2 раза, экзокринная функция поджелудочной железы не восстановилась, поэтому заместительная терапия сохранена на пожизненный режим приема, болевой синдром полностью купирован на фоне приема амитриптилина через 4 месяца. За примерно годовой период наблюдения после лечения отмечается клиническая и иммунологическая ремиссия.
Представленный клинический случай является примером редкой формы хронического панкреатита – диагностика, лечение и диспансерное наблюдение этой группы пациентов требуют мультидисциплинарного подхода.
Проведенная терапия, по международным данным [8], позволяет достичь ремиссии, длительность которой индивидуальна. Диспансерное наблюдение пациента продолжается.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Литература/References
* ООО Клиника «Здоровая семья», Красноярск, Россия
** ФГБОУ ВО КрасГМУ им. проф. В. Ф. Войно-Ясенецкого, Красноярск, Россия
*** КГБУЗ Красноярская МКБ № 4, Красноярск, Россия
**** ФГБУ ФСНКЦ ФМБА России, Красноярск, Россия
# КГБУЗ ККБ, Красноярск, Россия
## КГАУЗ Красноярская МБ № 5, Красноярск, Россия
IgG4-ассоциированный панкреатит – трудности диагностики и лечения/ М. А. Черепнин, Е. В. Серова, С. И. Бердников, Е. В. Чупраков, Ю. Б. Говорина
Для цитирования: Черепнин М. А., Серова Е. В., Бердников С. И., Чупраков Е. В., Говорина Ю. Б. IgG4-ассоциированный панкреатит – трудности диагностики и лечения // Лечащий Врач. 2021; 2 (24): 35-37.
Теги: поджелудочная железа, воспаление, иммуноглобулины класса G
Аутоиммунный панкреатит
Аутоиммунный панкреатит — это редкая системная болезнь поджелудочной железы и других органов, вызванная повреждением соединительной ткани иммуноглобулинами G4. Проявляется абдоминальной болью, желтушным синдромом, диспепсией, изменениями стула и признаками недостаточности питания. Диагностируется с помощью УЗИ, МРТ панкреатической железы, копрограммы, определения уровня иммуноглобулинов и гистологического анализа. Для терапии используются кортикостероиды и моноклональные антитела. При неэффективности консервативного лечения выполняется дренирование, стентирование, стомирование панкреатических и желчевыводящих протоков.
МКБ-10
Общие сведения
Хотя аутоиммунный панкреатит считается редким заболеванием, его доля в структуре хронических воспалений поджелудочной железы достигает 4-6%. Распространенность болезни не превышает 0,0008%. Впервые патология описана французским клиницистом Г. Сарлесом в 1961 году. В качестве отдельной нозологической единицы заболевание признано в 2001 году после разработки этиологической классификации панкреатита TIGAR-O. Аутоиммунное поражение панкреатической железы у мужчин выявляется в 2-5 раз чаще, чем у женщин. До 85% пациентов заболевает после 50 лет. Болезнь зачастую сочетается с ревматоидным артритом, забрюшинным фиброзом, склерозирующим холангитом и другими аутоиммунными процессами.
Причины
Этиология аутоиммунного панкреатита не установлена. Обычно заболевание диагностируется методом исключения при выявлении иммуноглобулинов типа G4 и отсутствии других возможных причин поражения поджелудочной железы. Специалисты в сфере клинической гастроэнтерологии допускают ведущую роль наследственной отягощенности, в ходе медико-генетических исследований установлена ассоциация аутоиммунного процесса с серотипами HLA DRβ1-0405, DQβ1-0401, DQβ1-57. Из крови пациентов выделен сывороточный протеин массой 13,1 кДа, который считают специфическим антигеном.
В качестве вероятных аутоантигенов рассматриваются карбоангидраза, присутствующая в тканях пищеварительных органов, бронхиальном дереве и дистальных почечных канальцах, лактоферрин, выявляемый в панкреатических ацинусах, железах бронхов и желудка, компоненты клеточных ядер и гладкомышечных волокнах, панкреатический ингибитор трипсиногена и трипсина. Не исключена перекрестная сенсибилизация с инфекционными агентами – обнаружена молекулярная мимикрия между антителами к протеинам возбудителя хеликобактериоза и плазминоген-связывающему белку.
Патогенез
Пусковым механизмом изменений в панкреатической железе и других чувствительных органах становится связь сывороточных Ig G4 с аутоантигенами ацинарных клеток, нормальных эпителиоцитов панкреатических, желчных, слюнных протоков и др. Антигенное повреждение сопровождается нарушением апоптоза клеточных элементов иммунной системы. Ключевым звеном патогенеза аутоиммунного панкреатита считается накопление в соединительной ткани персистирующих активированных Т- и В-лимфоцитов, нейтрофилов и эозинофилов, провоцирующее фиброзно-склеротические процессы.
При цитологическом исследовании в панкреатической строме выявляются признаки фиброза и склероза при отсутствии псевдокист и конкрементов. Из-за лимфоплазмоцитарной, нейтрофильной и эозинофильной инфильтрации стенки протоков уплотнены, сужены, при длительном течении аутоиммунного процесса фрагментированы. Распространение воспалительной инфильтрации на дольки поджелудочной железы приводит к потере дольчатой структуры органа и часто сочетается с флебитом. Как и при других вариантах хронического панкреатита, возможна кальцификация паренхимы и стромы.
Классификация
При систематизации форм аутоиммунного панкреатита учитывают распространенность фиброзно-склеротического процесса, наличие сопутствующих поражений других органов, морфологические особенности воспаления. При очаговом варианте заболевания повреждены отдельные участки панкреатической паренхимы, преимущественно головка органа. Обычно поражено не менее 1/3 железы (сегментарная форма панкреатита). Для диффузной формы патологии характерно вовлечение всего органа.
При отсутствии других аутоиммунных болезней панкреатит называют изолированным. В случае системного поражения нескольких органов говорят о синдромальном аутоиммунном панкреатическом воспалении. С учетом гистологической картины различают два основных варианта заболевания, каждый из которых отличается характерными клиническими особенностями:
Симптомы аутоиммунного панкреатита
Клиническая картина заболевания отличается от типичного воспаления поджелудочной железы. При аутоиммунном варианте поражения органа боли менее интенсивные, тупые, не связаны с погрешностями в рационе питания. Болевой синдром развивается только у половины пациентов. Другой важный симптом аутоиммунного панкреатита — механическая желтуха, которая возникает в среднем у 60-80% больных и проявляется желтушным окрашиванием кожи и склер, кожным зудом, обесцвечиванием кала.
Аутоиммунная панкреатическая патология часто сопровождается диспепсическими расстройствами: тошнотой, изменением характера стула (обильный зловонный кал сероватого цвета), вздутием живота. При прогрессировании заболевания возникает нарушение всасывания и дефицит питательных веществ, который проявляется снижением массы тела пациентов, безбелковыми отеками лица и нижних конечностей. На поздних стадиях панкреатита развивается постоянная жажда, полиурия (симптомы нарушения обмена глюкозы).
Осложнения
У большинства больных аутоиммунный панкреатит протекает с вовлечением в патологический процесс других органов и тканей. Чаще всего заболевание распространяется на билиарную систему с развитием склерозирующего холангита и бескаменного холецистита. На связь этих нозологических форм с панкреатитом указывает типичная лимфогистиоцитарная инфильтрация стенок желчевыводящих путей и хороший ответ на гормональную терапию. Иногда поражается печень с формированием псевдоопухоли или цирроза.
Частым осложнением панкреатического аутоиммунного воспаления является сахарный диабет, который возникает вследствие постепенного некроза клеток островков Лангерганса, сопровождающегося резким снижением выработки инсулина. Более редкие последствия заболевания — иммунокомплексное поражение почечной паренхимы по типу тубулоинтерстициального нефрита, интерстициальная пневмония. Циркуляция антител IgG в крови приводит к склерозу тканей слюнных желез.
Диагностика
Постановка правильного диагноза представляет затруднения, что объясняется редкой встречаемостью патологии и разнообразием ее клинических проявлений. В большинстве случаев диагностический поиск при аутоиммунном панкреатите направлен на исключение других форм панкреатического воспаления. Наиболее информативными являются такие методы исследования, как:
Показатели общего анализа крови при панкреатите аутоиммунного типа обычно без изменений. В биохимическом анализе крови выявляют неспецифические признаки поражения билиарного тракта и печени: повышение уровня печеночных ферментов, липазы и амилазы, увеличение концентрации билирубина за счет конъюгированной фракции. При подозрении на аутоиммунное поражение легких проводят рентгенографию, при нарушении функции почек — анализ мочи по Зимницкому.
Прежде всего, заболевание необходимо дифференцировать с раком поджелудочной железы, особенно у пациентов старше 60 лет. В пользу аутоиммунного воспаления свидетельствует повышение специфических антител в крови, типичные УЗИ-признаки, воспалительная инфильтрация панкреатической ткани по результатам гистологии. Дифференциальную диагностику также осуществляют с первичным склерозирующим холангитом, раком желчных путей. Для обследования пациента с аутоиммунным вариантом панкреатита привлекаются врач-гастроэнтеролог, онколог, иммунолог.
Лечение аутоиммунного панкреатита
Поскольку у части больных возможно спонтанное излечение с полным восстановлением экзокринной и эндокринной панкреатических функций, медикаментозную терапию проводят только при наличии соответствующих показаний. При бессимптомном течении назначение лекарственных средств оправдано в случае выявления персистирующего образования панкреатической железы, стойком изменении печеночных показателей в сочетании с признаками склерозирующего холангита. Рекомендованные схемы лечения аутоиммунного варианта панкреатита обычно включают:
В симптоматической терапии с учетом клинических проявлений используют панкреатические ферменты, сахароснижающие средства и блокаторы протонной помпы. Для купирования болевого синдрома рекомендованы нестероидные противовоспалительные средства, миотропные спазмолитики. Пациентам со стойкой компрессией выполняется стентирование главного панкреатического протока, чрескожное транспеченочное дренирование желчных протоков, назобилиарное дренирование при РПХГ. При безуспешности малоинвазивных техник проводится панкреатоеюностомия, холецистоэнтеростомия.
Прогноз и профилактика
Исход болезни зависит от степени поражения тканей, тяжести осложнений. Хотя стероидная терапия позволяет достичь ремиссии более чем у 90% больных, прогноз аутоиммунного панкреатита относительно неблагоприятный, у части пациентов происходит необратимое снижение эндокринной и экзокринной функций органа. Из-за недостаточно изученного этиопатогенетического механизма меры специфической профилактики не разработаны. Для предупреждения осложнений важно своевременно выявлять и лечить аутоиммунные заболевания пищеварительного тракта.
.png)