Бактероиды спп что это такое
Bacteroides spp. (качественный метод)
Описание исследования
Bacteroides spp. – это анаэробные (осуществляющие процесс жизнедеятельности без доступа кислорода) грамотрицательные бактерии. Бактероиды являются частью нормальной микрофлоры определенных зон организма. Они обитают в частности:
В нормальном состоянии слизистые оболочки желудочно-кишечного тракта, исполняя роль барьера, препятствуют попаданию этих бактерий во внутреннюю среду организма. Однако при нарушении бактериального баланса болезнетворные штаммы бактериодов становятся причиной ряда заболеваний, а именно:
У пациентов с диагнозом «воспаление предстательной железы», «хронический уретит» (в 6,1% эти патологии являются осложнением после гонореи), с болезнями, характеризующимися упорным течением и регулярными обострениями, при обследовании часто выявляются бактероиды. Если Bacteroides spp. обнаружен одновременно с гарднереллой и мобилункусом, это признак бактериального вагиноза.
Bacteroides spp. могут спровоцировать свертывание крови внутри сосудов, что влечет за собой воспаление вен и тромбозы. При инфекции, протекающей в самой тяжелой форме, возможно:
Данный тест предназначен для выявления специфических фрагментов ДНК бактероидов (Bacteroides spp) в урогенитальных соскобах, сперме моче. Для проведения исследования используется метод полимеразной цепной реакции – метод молекулярной биологии, основанный на многократном увеличении количества специфических фрагментов ДНК агента инфекции в исследуемой пробе.
Аналитические показатели теста:
Подготовка к исследованию
Соскоб урогенитальный
Соскобы у женщин отбираются не ранее пятого дня от начала менструального цикла и не позже пятого дня до предполагаемой даты следующей менструации. Если наблюдаются явные признаки заболевания, отбор пробы проводится непосредственно в день обращения.
Требования по подготовке к тестированию:
Проба не отбирается:
При отборе эпителиальных клеток из мочеиспускательного канала, манипуляция проводится перед мочеиспусканием или через 1,5-2 часа после него.
Сперма
Отбор материала с целью диагностики проводится до начала противобактериального, антивирусного и противопаразитарного лечения, химиотерапии, а также до лечебных или диагностических мероприятий в месте предполагаемой локализации агента инфекции. После курса лечения проба отбирается не ранее, чем через 10-14 дней при проведении локальной терапии и через 30 дней после перорального приема антибиотиков.
На анализ собирается порция первой утренней мочи, выделенной не ранее, чем через 2-3 часа после предыдущего (ночного) мочеиспускания. Ее объем должен составлять порядка 20-30 мл. Емкость, используемая для сбора биоматериала – стерильный медицинский контейнер.
Моча собирается либо до проведения химиотерапии или лечения антибиотиками, либо через месяц после окончания курса лечения.
Перед началом манипуляции необходимо тщательно обмыть гениталии. Женщинам желательно воспользоваться гигиеническим тампоном во избежание попадания в пробу слизи из влагалища. Во время менструации материал не собирается.
После наполнения контейнера на треть-половину объема, емкость с мочой плотно закрывается крышкой, дабы избежать ее вытекания.
Доставка биоматериала должна быть организована в течение максимум 6 часов. До отправки в лабораторию моча может храниться как в холодильнике (при t⁰ от +2⁰С – замораживать ее нельзя), так и в комнате, но при этом температура не должна быть выше +25⁰С.
Показания к исследованию
Интерпретация исследования
Данный тест – качественный, результат выдается в формулировках «обнаружено» или «не обнаружено».
Нормой является отсутствие в исследуемой пробе специфических фрагментов ДНК Bacteroides spp.
Результат анализа выдается на бланке лаборатории медицинской компании «Наука». Пример результата по данному анализу представлен ниже:
Ф.И.О.: Иванов Иван Иванович Пол: м Год рождения: 01.01.0000
Дата исследования: 12.12.0000
Бактероиды
История обнаружения
Бактероиды (Bacteroides) были впервые обнаружены в 1898 году учеными Вейоном и Зюбером (A. Veillon, H. Zuber). Микроорганизмы выделены у больного с абдоминальным абсцессом и получили название Bacillus fragilis. Спустя 14 лет Дистазо (A. Distaso) обнаружил их у здоровых людей, а через семь лет Кастеллани (A. Castellani) и Чалмерс (A. J. Chalmers) дали этим палочкам название Бактероиды.
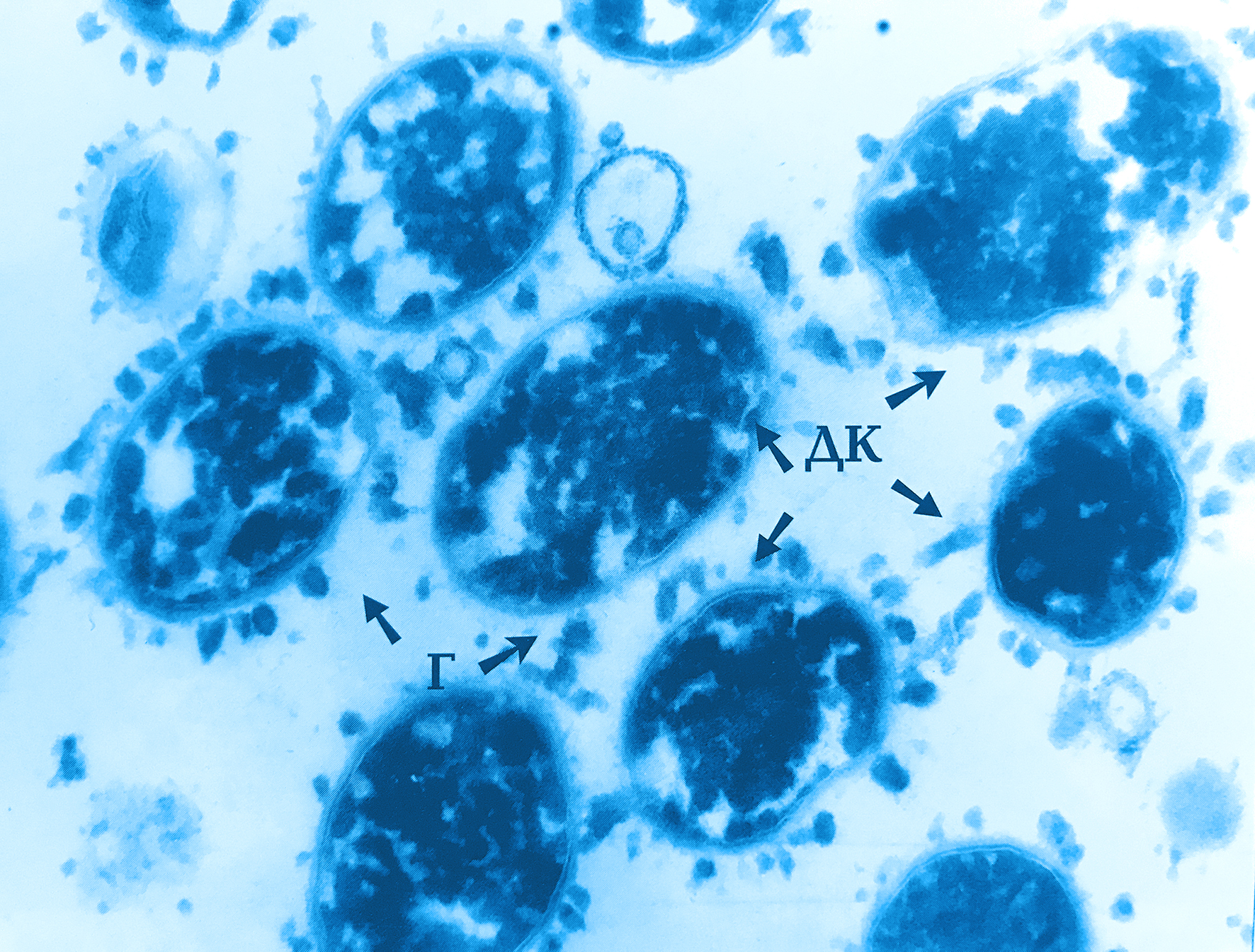
Внешний вид под микроскопом
Бактероиды при микроскопии могут иметь разную форму. Преимущественно это небольшие палочки, не окрашивающиеся по Граму. У отдельных видов эти палочки не обособляются при размножении, в результате чего получаются скопления бактерий, напоминающие ветви. Иногда у бактероидов имеются в одном из концов утолщенные вакуоли, за счет чего клетка приобретает форму кеглей или булавы. Поэтому их легко спутать с коринебактериями или спорообразующими бактериями. Бактероиды имеют жгутики и способны к образованию капсулы, позволяющей переждать неблагоприятные для жизни условия.
Где обитает
В норме представители Bacteroides у человека колонизируют толстую кишку и являются типичными представителями нормофлоры, наряду с лакто- и бифидобактериями. В фекалиях здорового человека около 40-50% всех микробных клеток составляют бактероиды.
Классификация
Царство
Bacteria
Тип
Bacteroidetes
Класс
Bacteroidia
Порядок
Bacteroidales
Семейство
Bacteroidaceae
Род
Bacteroides
Prevotella
Свойства
Бактероиды способны утилизировать сахарозу, мальтозу, глюкозу, рамнозу. Продуцируют янтарную, изовалериановую, уксусную и масляную кислоту. Вырабатывают вещества, способные инактивировать антибиотики пенициллового и цефалоспоринового ряда. Для роста необходим углекислый газ в концентрации 5-10% и температурный диапазон от +25 до +45°С. Оптимальная температура +37°С.
Функции
Биологическая роль бактероидов в толстом кишечнике изучена недостаточно. Однако доказана их антагонистическая активность по отношению к сальмонеллам, шигеллам и некоторым патологическим эшерихиям. Можно предположить, что, колонизируя толстый кишечник, представители Bacteroides защищают своего хозяина от инфекционных энтероколитов, вызванных патогенными микроорганизмами.
Вызываемые заболевания
В условиях нарушения иммунитета бактероиды проявляют свою патогенную активность. Они не вырабатывают эндотоксичные вещества, но, поскольку имеют полисахаридную капсулу, могут спровоцировать выработку антител в организме хозяина. В ассоциации с другими патогенными и условно-патогенными бактериями, Bacteroides способны вызывать перитонит, кольпит, пневмонию, пародонтоз, абсцессы, аппендицит, эндокардиты, заболевания слизистых оболочек и кожи.
Профилактика и лечение
Для подавления роста и размножения бактероидов используются антибиотики, в частности, ципрофлоксацин, офлоксацин, метронидазол, клиндамицин, левомицитин. Общеукрепляющие процедуры и элементарная гигиена, защита от стрессов и нормализация пищевого поведения (отказ от голодания и переедания), а также сбалансированный рацион питания способствуют защите от чрезмерного размножения бактероидов.
Bacteroides spp., определение ДНК (кач)
Бактероиды являются анаэробными бактериями дистального отдела тонкой кишки. Большая часть каловых масс состоит из микробов, называемых Bacteroidesfragilis. Их проникновению во внутреннюю среду человеческого организма препятствуют барьерные функции слизистых оболочек ЖКТ.
Информация об исследовании
Еще они обитают в естественной микрофлоре женской репродуктивной системы, верхних и нижних дыхательных путях. При нарушении баланса микрофлоры патогенные штаммы бактероидов могут стать возбудителями разных болезней. Чаще всего это воспаление шейки матки, эндометриты, воспаления яичников и маточных труб, инфекции в малом тазу у женщин.
У мужчин эти бактерии находят при простатите или осложненном уретрите (у 6,1%, страдающих постгонорейным уретритом ), перешедшем в хроническую форму, а также когда заболевание не отступает или случаются рецидивы.
Для исследования требуется сдать такие анализы, как соскоб эпителиальных клеток с шейки матки и мочеиспускательного канала, со стенок влагалища, периуретральной зоны, крайней плоти, секрет простаты.
Показания
Анализы необходимо сдавать в следующих случаях:
если проявляются симптомы бактериального вагиноза у представительниц женского пола;
при острых воспалениях органов мочеполовой системы;
при воспалениях у женщин органов урогенитальной системы, имеющих хронический характер;
при возвращающихся простатитах и уретритах у мужского пола.
Материалы для исследования у женщин берутся после 5 дня менструального цикла, в первой его половине.
Подготовка
За 10 дней до исследования требуется прекратить лечение и прием медикаментов.
Мазок у женщин не берется во время менструации.
Мужчинам перед взятием мазка необходимо воздержаться от мочеиспускания около 2 часов.
Bacteroidesspp., определение ДНК (кач) в Ростове
Провести исследование Bacteroidesspp. в Ростове можно в нашем центре «Да Винчи», оснащенном новым качественным оборудованием, при помощи которого можно получить максимально быстрые и достоверные результаты. Звоните по указанным телефонам, чтобы записаться на прием или получить ответы на интересующие вопросы.
Состояние микробиоценоза влагалища, бактериальный вагиноз и возможности его лечения
Опубликовано в журнале:
«CONSILIUM MEDICUM», 2013, ТОМ 15, № 10, с. 22-24
А.В.Ледина, В.Н.Прилепская
ФГБУ Научный центр акушерства, гинекологии и перинатологии им. В.И.Кулакова Минздрава РФ
Бактериальный вагиноз (БВ) – широко распространенное патологическое состояние, встречающееся у женщин детородного возраста, которое включает комплекс изменений вагинального биотопа, характеризующегося снижением количества нормальной кислородпродуцирующей лактофлоры и повышением концентрации других микроорганизмов, особенно грамотрицательных анаэробов типа Prevotella Porphyromonas spp., Peptostreptococcus spp., Fusobacterium spp., Mobiluncus spp. и GV [5, 18].
Известно, что микрофлора влагалища здоровых женщин репродуктивного возраста представлена широким спектром микроаэрофилов, а также факультативных и облигатных анаэробов [4], присутствие которых не нарушает нормального состояния, не вызывает развития воспалительной реакции и патологических симптомов, характерных для вульвовагинита или БВ. В основном нормальная микрофлора представлена микроорганизмами рода Lactobacillus spp. – микроаэрофильными, продуцирующими перекись водорода палочками (71–100%), реже – анаэробными грамположительными палочками (5–30%).
Кроме лактобактерий, микроаэрофильная флора влагалища здоровых женщин представлена Gardnerella vaginalis (по данным разных авторов, в 6–60% случаев), а также включает облигатные анаэробы Peptostreptococcus spp. (30–90%), грамположительные анаэробные кокки, грамположительные палочки – строгие анаэробы Bifidobacterium spp. (у здоровых женщин примерно в 12% случаев), Clostridium spp. (10–25%), Propionibacterium spp. – P. acnes (до 25%), значительно реже выявляются Mobiluncus spp. (0–5%). Все эти микроорганизмы являются типичными представителями нормальной микрофлоры генитального тракта.
В нормальном биотопе также могут обнаруживаться грамотрицательные строго анаэробные палочковидные бактерии бактероиды Bacteroides spp.: B. urealyticum, B. fragilis, B. vulgatus, B. ovatus, B. distasonis, B. uniformis, B. coccae, B. multiacidus (9–13%), Fusobacterium spp. (14–40%), Porphyromonas spp. (31%), Prevotella spp. (60%) и генитальные микоплазмы M. hominis, U. urealyticum (у 2–15% сексуально активных женщин).
Из представителей факультативных анаэробных микроорганизмов часто выделяют каталазопозитивные, коагулазонегативные Staphylococcus epidermidis, новобиоцинрезистентные Staphylococcus saprophyticus, Streptococcus spp. Это стрептококки группы viridans – «зеленящие» (а или g), гемолитические, стрептококки серологической группы В (Streptococcus agalactie), стрептококки серологической группы D (энтерококки); непатогенные коринебактерии – Corynebacterium minutissimum, C. equi (новое название – Rhodococcus equi), C. aquaticum, C. xerosis; Escherichia coli.
Микробиоценоз влагалища при БВ характеризуется резким снижением уровня перекись продуцирующих лактобактерий, вплоть до их полного исчезновения, и замещением их гарднереллами, которые способствуют росту колоний аэробных и анаэробных микроорганизмов. Кроме G. vaginalis, характерными представителями микрофлоры при БВ являются Prevotella spp., Porphyromonas spp., Bacteroides spp., Peptostreptococcus spp., Mycoplasma hominis, Ureaplasma urealyticum, Mobiluncus spp., а также Fusobacterium spp. и Atopobium vaginae.
Концентрация микроаэрофильных бактерий (G. vaginalis) при БВ может повышаться в сотни раз, а анаэробных микроорганизмов Bacteroides spp., Peptococcus spp. – в тысячи раз и более [1, 9]. В некоторых случаях на фоне абсолютного преобладания микроорганизмов, ассоциированных с БВ, могут присутствовать и лактобактерии в низком титре, но, как правило, это анаэробные лактобактерии, неспособные продуцировать перекись водорода.
В сложной цепи патогенеза различных заболеваний женских половых органов существенная роль отводится иммунным реакциям организма. Снижение неспецифической резистентности у пациенток с БВ [2], а также то, что до 90% G. vaginalis находятся на поверхности вагинального эпителия в виде биопленок [21], способствует росту резистентности анаэробной вагинальной флоры [13] к современным лекарственным препаратам и длительному рецидивирующему течению патологического процесса.
Клиника
Основными клиническими проявлениями БВ являются гомогенные выделения из влагалища, пенистые, слегка тягучие, белого или серого цвета со специфическим «рыбным» запахом. Другие жалобы, такие как зуд, дизурические расстройства, диспареуния, встречаются реже, могут совсем отсутствовать или появляться периодически. Бессимптомное течение инфекционного процесса наблюдается более чем у 1/2 всех женщин с БВ, и у них какие-либо субъективные жалобы могут вообще отсутствовать [16]. При длительно текущем процессе выделения приобретают желтовато-зеленоватую окраску, становятся более густыми, нередко напоминают творожистую массу, равномерно распределяются по стенкам влагалища без выраженного его воспаления [8].
Наиболее опасны осложнения БВ, которые возникают при беременности, во время родоразрешения (преждевременный разрыв плодных оболочек, хориоамнионит, аномалии родовой деятельности), в послеродовом или послеоперационном периоде в случае оперативного родоразрешения (послеродовый эндометрит). БВ может оказывать неблагоприятное влияние на развитие плода (гипотрофия) или новорожденного (пневмония), поэтому чрезвычайно важным является лечение этого заболевания в период планирования и во время беременности [1].
Диагностика
С 1983 г. и по настоящее время для постановки диагноза БВ применяются критерии, предложенные R.Am-sel и соавт. (1983 г.), которые включают наличие обильных выделений из влагалища с неприятным запахом; появление запаха «гнилой рыбы» при проведении аминного теста; повышение значения pH вагинального содержимого до 4,5; присутствие «ключевых клеток» в мазках, окрашенных по Граму. Диагноз БВ можно поставить в случае выявления 3 из 4 указанных критериев.
Микроскопия вагинального мазка, окрашенного по Граму, – наиболее информативный, достоверный и доступный метод диагностики БВ, который дает возможность объективно оценить состояние вагинальной микроэкологии, причем позволяет оценить не только морфологические особенности и соотношение отдельных компонентов вагинальной микрофлоры, но и получить информацию о состоянии слизистой влагалища и наличии лейкоцитарной реакции [5]. Полимеразная цепная реакция позволяет провести не только типирование, но и количественное определение микроорганизмов в режиме реального времени и в последние годы широко применяется в клинической практике.
Лечение
Успешное лечение БВ, как и любого заболевания, зависит от правильной и своевременной постановки диагноза и проведения патогенетически обоснованной эффективной терапии.
Цель лечения БВ – восстановить нормальную микрофлору влагалища, задержать рост микроорганизмов, не свойственных этому микроценозу. Как правило, на первом этапе лечения для пациентки подбирается терапия, которая обеспечивает высокую концентрацию лекарственного вещества во влагалище, что обусловливает эффективность использования малых доз антимикробного препарата и быстрое купирование симптомов заболевания. Второй этап лечения включает стимуляцию нормальной лактофлоры влагалища за счет применения биологических бактерийных препаратов – эубиотиков и пробиотиков [6].
Основными препаратами для лечения БВ являются метронидазол, клиндамицин и тинидазол. Эти препараты могут применяться как в таблетированной форме для приема внутрь, так и в виде вагинальных таблеток, гелей, свечей. Хотя пероральный путь приема ассоциируется с большей частотой побочных эффектов, он является более приемлемым для большинства пациенток.
Метронидазол рекомендуется назначать в дозе 500 мг 2 раза в день в течение 7 дней или 1-кратно в дозе 2 г, но такой режим считается менее эффективным. При приеме метронидазола могут возникать побочные эффекты со стороны желудочно-кишечного тракта в виде металлического вкуса во рту и тошноты (до 10%), а также транзиторная нейтропения (7,5%), периферическая нейропатия. Тошнота, другие гастроинтестинальные эффекты менее выражены при интравагинальном пути введения метронидазола. Вагинальный гель в дозе 5 г, вводимый ежедневно в течение 5 дней, не уступает по эффективности пероральному пути введения и с успехом может применяться для лечения БВ [17].
Тинидазол – препарат нитроимидазольного ряда, применяется в таблетках по 1 г 1 раз в день в течение 5 дней или по 2 г в течение 2 дней.
Сравнимым по эффективности с метронидазолом, но имеющим меньшее количество побочных эффектов является клиндамицин (Клиндацин ® ) – антибиотик группы линкозамидов, обладающий широким спектром действия, оказывающим в основном бактериостатический эффект. Клиндамицин активен в отношении Staphylococcus spp. (в том числе Staphylococcus epidermidis, продуцирующих пенициллиназу), Streptococcus spp. (исключая Enterococcus spp.), Streptococcus pneu-moniae, Corynebacterium diphtheriae, в отношении споро- и неспорообразующих анаэробов и микроаэрофильных грамположительных кокков (включая Peptococcus spp. и Peptostreptococcus spp.), Clostridium perfringens, Clostridium tetani, Mycoplasma spp., Bacteroides spp. (включая Bacteroides fragilis и Prevotella melaninogenica), Fusobacterium spp., Propionibacterium spp., Eubacter spp., Actinomyces spp., т.е. против большинства микроорганизмов, вызывающих дисбиоз влагалища и БВ.
Предпочтительным режимом является местное применение препарата в течение 3–7 дней. При этом вагинальные суппозитории вводятся по 1 на ночь или 2% вагинальный крем при помощи аппликатора (5 г) на ночь 3–7 дней. Перорально клиндамицин назначается 2 раза в день по 300 мг в течение 7 дней.
Местный клиндамицин является наиболее эффективным по сравнению с метронидазолом препаратом при лечении рецидивирующего БВ, особенно ассоциированного с A. vaginae; клиническое излечение при его применении наступает в 83,3% случаев (рПобочные эффекты (псевдомембранозный колит, тошнота) при приеме клиндамицина встречаются редко, что значительно повышает комплаентность терапии.
Применение клиндамицина (Клиндацин ® ), что очень важно, возможно при беременности или в подготовительном к родам периоде (только местно) в обычных терапевтических дозировках.
Эффективность, быстрое достижение положительного результата лечения, хорошая переносимость клиндамицина при лечении, в том числе беременных женщин, доказана при проведении многочисленных рандомизированных плацебоконтролируемых сравнительных клинических исследований [1, 7, 14].
Вторым этапом лечения, а также с целью профилактики рецидивов БВ назначаются эубиотики, пробиотики, которые могут применяться в комплексе с антибактериальными препаратами или как основное средство лечения. В первом случае назначение пробиотиков целесообразно проводить не ранее чем через 3 дня после окончания антибактериальной терапии БВ в виде интравагинальных суппозиториев; длительность лечения должна составлять менее 7–10 дней [6, 12].
После проведенного лечения примерно у 1/3 пациенток возникает рецидив заболевания в течение первых 3 мес, а более чем у 1/2 симптоматика возобновляется в течение 12 мес [19, 20]. Это вероятнее всего происходит в связи с неэффективностью проведенного лечения, так как от 65 до 80% [15] патогенов находится в составе биопленок, матрикс которых может связывать или не пропускать, и/или инактивировать антибиотики [3, 10, 11] и приводить к снижению эффективности лечения. Другой возможной причиной частых рецидивов является то, что не происходит достаточно полного восстановления нормальной микрофлоры влагалища и на этом фоне вновь активизируется патогенная микрофлора [12, 23].
Вопрос о целесообразности назначения лечения партнерам женщин, получающих лечение по поводу БВ, не решен. Ряд исследователей считают, что лечение половых партнеров не влияет на успешность терапии, хотя доказана роль половых контактов в возникновении и рецидивировании БВ. Кроме того, показана эффективность использования презервативов в снижении частоты рецидивов БВ [22]. Но поскольку доказательная база для окончательных выводов остается недостаточной, для решения этой задачи необходимы новые исследования.
Таким образом, БВ, представляющий дисбиотическое состояние экосистемы влагалища, является достаточно распространенной в современной популяции патологией, требующей своевременной диагностики, комплексной адекватной терапии и профилактики. Препаратом, оказывающим быстрое положительное действие и обладающим хорошей переносимостью, а также разрешенным к применению во время беременности, является клиндамицин (Клиндацин ® ). Высокая эффективность, доказанная клиническими исследованиями, позволяет использовать Клиндацин ® в клинической практике как один из основных препаратов для лечения БВ.
Индекс лекарственного препарата: Клиндамицин: Клиндацин ® (Акрихин ОАО)
Бактерии ЖКТ: Бактероидеты, Фирмикуты и др.
КЛАССИФИКАЦИЯ ЖЕЛУДОЧНО-КИШЕЧНОЙ МИКРОБИОТЫ
ФИРМИКУТЫ , БАКТЕРОИДИЕТЫ и ДРУГИЕ
СОДЕРЖАНИЕ:
Резюме
В разделе речь пойдет об уже выявленных представителях наиболее распространенных таксономических типов в составе микробиома человека. Вопросам же непосредственного (технического) выявления (обнаружения и идентификации) микроорганизмов посвящены такие разделы сайта как « метагеномный анализ микробиоты » и « секвенирование биополимеров ». В любом случае это все взаимосвязанные понятия, объединенные задачей систематизации микроорганизмов и получения знаний об их функциональных характеристиках
Историческая перспектива
Люди, как и другие высшие организмы, живут в симбиозе совместно со своей микробиотой (Backhed et al., 2005). Большинство человеческих микроорганизмов находятся в желудочно-кишечном тракте, где, помимо того, что способствуют пищеварению, они выполняют и другие различные функции, которые важны для человека-хозяина. Эти функции включают в себя производство витаминов, формирование иммунной системы, связь с клетками кишечника и даже модуляцию поведения хозяина (Backhed et al., 2005; Cryan & Dinan, 2012; Rajili c-Stojanovi c, 2013). Первое сообщение о живых существах в желудочно-кишечном тракте человека датируется 1681 годом, когда голландский натуралист и конструктор микроскопов Антони ван Левенгук сообщил о разнообразных «маленьких животных» в своем образце стула и определили то, что сейчас называют лямблиями (Giardia spp.) при диарее (Dobell, 1932). Прошло почти два столетия, прежде чем появились первые подробные описания чистых культур желудочно-кишечных микроорганизмов, наиболее ранним из которых является описание кишечного паразита эукариального Pentatrichomonas hominis (в то время называемого Trichomonas hominis) Казимира Давейна в 1854 году (Hemmeter, 1902). Поскольку P. hominis, как и другие кишечные эукарии, имеет очень низкую распространенность, это открытие не вызвало дальнейшего анализа желудочно-кишечной микробиоты. Тем не менее, интенсивные исследования желудочно-кишечной микробиоты последовали за первым культивированием кишечной бактерии, теперь известной как Escherichia coli (кишечная палочка). С исторической точки зрения это и некоторые другие события, которые называют поворотными моментами, могут быть признаны как повлиявшие на открытие компонентов желудочно-кишечной микробиоты. И эти поворотные моменты очевидны, если учитывать количество описанных видов желудочно-кишечного тракта с точки зрения времени (см. рис. 1).
Первый поворотный момент отмечает описание желудочно-кишечной бактерии, которая представляет собой выделение Bacterium coli commune (позднее переименованное в E. coli), немецким педиатром Теодором Эшерихом (Theodor Escherich) в 1885 году (Shulman et al., 2007). Исследования, которые последовали вскоре после этого, привели к описанию представителей ряда основных желудочно-кишечных бактериальных групп, в том числе родов Bacteroides, Bifidobacterium и Bacillus, а также протеолитических кокков (Flügge, 1886; Veillon & Zuber, 1898; Moro, 1900; Tissier, 1900; Passini, 1905; Tissier, 1908; Distaso, 1911). В течение этого периода, который продолжался до конца шестидесятых годов 20-го века, Bifidobacterium и Bacteroides spp. считались доминирующими группами в желудочно-кишечном тракте человека. Аэробы, называемые колиформами, стрептококками и лактобациллами, были обнаружены в качестве второстепенных групп, в то время как клостридии, стафилококки и спорообразующие анаэробы были зарегистрированы как редкие и не всегда выявляемые (Haenel, 1970). Однако в настоящее время известно, что подавляющее большинство желудочно-кишечных микроорганизмов являются строгими анаэробами, и это было впервые показано в 1931 году (Sanborn, 1931). Таким образом, ранние исследования культивирования предоставили только частичное представление о желудочно-кишечной микробиоте и позволили выделить только меньшинство (10–25%) желудочно-кишечных микроорганизмов (Finegold, 1969).
Рис. 1. Графическое представление совокупного числа культивируемых видов из бактерий, архей и эукарий из желудочно-кишечного тракта человека в зависимости от времени. Стрелками указаны поворотные точки исследования микробиоты желудочно-кишечного тракта: (1) выделение первых видов желудочно-кишечных бактерий, (2) внедрение строго анаэробных методов и (3) внедрение молекулярных методов в области исследования микробиоты желудочно-кишечного тракта.
Усовершенствование методов анаэробного культивирования Робертом Хунгейтом (Hungate, 1969) ознаменовало второй поворотный момент в исследовании желудочно-кишечной микробиоты, примерно 50 лет назад (рис. 1). В этот второй период исследований микробиоты желудочно-кишечного тракта, который продолжался с начала семидесятых годов до молекулярной революции в начале этого столетия (рис. 1), было признано, что в микробиоте желудочно-кишечного тракта преобладают виды бактерий, принадлежащих к следующие родам: Bacteroides, Clostridium, Eubacterium, Veillonella, Ruminococcus, Bifidobacterium, Fusobacterium, Lactobacillus, Peptostreptococcus и Peptococcus (Moore & Holdeman, 1974a). Используя строгие анаэробные методы, по сообщениям, можно было культивировать до 88% общего микроскопического количества в пробах фекалий (Moore & Holdeman, 1974a). Однако из-за огромной сложности желудочно-кишечной микробиоты многие из сотен изолятов не были охарактеризованы выше уровня родов (Finegold et al., 1974; Moore & Holdeman, 1974a; Benno et al., 1986). Более того, поскольку обработка даже одного образца дала огромное количество различных изолятов, было физически невозможно сравнить их все и дать полное описание на основе морфологических, биохимических и физиологических характеристик, которые можно было определить в то время (Moore & Holdeman 1974b). Следовательно, из-за этих технических ограничений желудочно-кишечная микробиота оставалась только частично охарактеризованной.
Наконец, третий поворотный момент в исследовании микробиоты желудочно-кишечного тракта можно объяснить введением молекулярных методов около десятка лет назад (рис. 1). Они включают в себя глобальные и независимые от культуры исследования, основанные на анализе последовательности малой субъединичной рибосомальной РНК (SSU рРНК), которая обеспечила молекулярную основу для микробной таксономии, которая используется в настоящее время (Woese et al., 1990). Однако сложность микробной экосистемы желудочно-кишечного тракта препятствует быстрому применению методов, основанных на SSU рРНК, а также (мета) геномики (Zoetendal et al., 2008). Таким образом, первое исследование желудочно-кишечного тракта с использованием последовательностей SSU рРНК имело дело с одной взрослой выборкой (Wilson & Blitchington, 1996). Последующие исследования на основе SSU рРНК у нескольких взрослых продемонстрировали индивидуальность, временную стабильность и штаммоспецифичность кишечной микробиоты с разнообразием, которое только частично было учтено в исследованиях, основанных на культивировании (Zoetendal et al., 1998; Suau et al., 1999; Zoetendal et al. al., 2001). Эти новые открытия вызвали возрождение научного интереса к желудочно-кишечной микробиоте, который первоначально сравнивался с эпохой Возрождения (Tannock, 1999). Тем не менее, последующие годы показали, что это было скорее революцией, которая включила метагеномы и характеристики целого генома (Nelson et al., 2010; Qin et al., 2010; Brown et al., 2013).
В сочетании с исследованиями, основанными на культивировании, анализ последовательностей генов SSU рРНК в качестве филогенетических маркеров позволил быстро идентифицировать новые желудочно-кишечные изоляты и продемонстрировал необходимость реклассификации многих видов. Кроме того, секвенирование генов SSU рРНК позволили обнаружить еще не культивируемые микроорганизмы и их филогенетическое расположение. Наконец, область исследований расширилась до другого измерения с применением высокопроизводительных подходов, включая секвенирование следующего поколения ( NGS ) последовательностей генов SSU рРНК или всего геномного материала (Zoetendal et al., 2008). В результате последних метагеномных анализов были получены исходные данные из более чем 3 миллионов, в основном бактериальных, генов, присутствующих в желудочно-кишечном тракте человека (Qin et al., 2010; Brown et al., 2013), и продемонстрировано, что большинство желудочно-кишечных микроорганизмов содержат геномы, которые не еще не охарактеризованы (Qin et al., 2010; Le Chatelier et al., 2013).
Современный взгляд на состав микробиоты ЖКТ
Обширный период изучения желудочно-кишечной микробиоты, ее сложности и различий между индивидуумами породил огромное количество информации, которая разбросана по литературе. Чтобы объединить знания о желудочно-кишечной микробиоте, накопленные с момента ее открытия, исследователи провели поиск публикаций, охватывающих более века (рис. 1). Они нашли ссылки, которые связывают желудочно-кишечную микробиоту человека с 1057 видами микроорганизмов кишечника, относящимися к Eukarya (92), Archaea (8) и бактериям (957). Эти виды были проанализированы в программной базе данных ARB последовательностей SSU рРНК (Pruesse et al., 2007). Представленные здесь филогенетические деревья были извлечены из эталонного филогенетического дерева базы данных SILVA (Yarza et al., 2008). Из этого филогенетического и литературного анализа становится ясно, что бактерии, которые группируются в типах Actinobacteria, Bacteroidetes, Firmicutes и Proteobacteria, являются самыми разнообразными и многочисленными микроорганизмами в желудочно-кишечном тракте взрослого человека (Рис.2.).
Рис. 2. Филогенетическое древо микробиоты желудочно-кишечного тракта человека. Цифры в скобках указывают количество культивируемых видов, приведенных в каждом типе. Круговые диаграммы иллюстрируют распределение между числом видов с полной последовательностью генома (полные секторы), числом видов с частичной последовательностью генома (полузакрытые секторы) и числом видов без какой-либо последовательности генома (пустые секторы), приведенных для Архей ( Archaea ), домена Эукарий (Eukarya) и для каждого типа Бактерий. Цвет круговых диаграмм соответствует цвету филогенетического дерева.
Исследование микробиоты желудочно-кишечного тракта является очень динамичным, и за последнее десятилетие было обнаружено или описано 239 новых видов микроорганизмов желудочно-кишечного тракта, что подтверждает ранее высказанное мнение о том, что большинство ЖКТ-микробов являются культивируемыми, но еще не культивируются. В то время как традиционные среды и стратегии культивирования эффективны для получения новых видов в составе Actinobacteria, Bacteroidetes, Firmicutes и Proteobacteria phyla, для выявления желудочно-кишечных представителей типов Verrucomicrobia и Lentisphaerae необходимы разработка специфических сред и подходов к культивированию (Zoetendal et al., 2003; Derrien et al., 2004). Это говорит о том, что для культивирования желудочно-кишечных микроорганизмов, принадлежащих к типу, в которых отсутствуют какие-либо культивируемые представители кишечника человека (например, тип-кандидат TM7 или род Oscillospira), следует разработать и применить альтернативные и творческие подходы к культивированию. Некоторые новые и многообещающие разработки включают использование высокопроизводительного твердофазного роста (Ingham et al., 2007), передовые подходы к культивированию с использованием гнотобиотических мышей (Goodman et al., 2011) или культивирование гелевых микрокапель (Fitzsimons et al., 2013). Использование высокопроизводительных систем культивирования, использующих большой набор питательных сред, связанных с геномной характеристикой, оказалось очень плодотворным (Lagier et al., 2012a; Dubourg et al., 2013; Hamad et al., 2013; Pfleiderer et al., 2013). Это недавнее внимание к культивированию желудочно-кишечных микроорганизмов отражает осознанную потребность в подробных физиологических, экологических и генетических исследованиях. В то время как различные функциональные метагеномные подходы были описаны и применены, именно интеграция с подходами культивирования необходима для дальнейшего понимания функции кишечной экосистемы в отношении здоровья и болезней. Сила этой комбинации была недавно проиллюстрирована на примере обильной бактерии-утилизатора слизи, Akkermansia muciniphila в качестве парадигмы (Belzer & de Vos, 2012). В настоящее время полный геном по крайней мере одного штамма из 225 желудочно-кишечных видов был полностью секвенирован, собран и опубликован, в то время как многие другие проекты геномного секвенирования продолжаются. Физиологические и генетические характеристики этих в настоящее время признанных видов микроорганизмов ЖКТ и их связь с конкретными функциями экосистемы или заболеваниями систематизированы в обзоре «The first 1000 cultured species of the humangastrointestinal microbiota», который призван обеспечить основу для будущих сравнительных и функциональных метагеномных и других высокопроизводительных подходов, применяемых в отношении желудочно-кишечной микробиоты.
Фирмикуты (Firmicutes)
Фирмикуты (Firmicutes) являются самым разнообразным и многочисленным отделом ( типом ) желудочно-кишечной микробиоты, составляя более половины, а во многих случаях около 80% желудочно-кишечной микробиоты здоровых взрослых. Желудочно-кишечные Firmicutes распределены по четырем классам : Bacilli, Clostridia, Erysipelotrichi и Negativicutes. Традиционно считается, что в этот отдел (тип) входят грамположительные бактерии с низким содержанием гуанин-цитозинового состава ( GC ) в их ДНК, хотя недавние исследования показали, что грам-положительное окрашивание не является особенностью многих Firmicutes. Это можно проиллюстрировать на примере Фекалибактерии Faecalibacterium prausnitzii, которая является грамотрицательной бактерией, ранее классифицированной в рамках типа Fusobacteria (Duncan et al., 2002a), новых желудочно-кишечных изолятов, таких как Christensenella minuta (Morotomi et al., 2012), а также типичных грам-отрицательных бактерий, таких как члены семьи Veillonellacea (Marchandin et al., 2010).
Дополнительно о фирмикутах см. ниже по ссылке →
Бактероидеты (Bacteroidetes)
Долгое время считалось, что большинство грамм-отрицательных бактерий желудочно-кишечного тракта принадлежит к роду Bacteroides, но в последние годы многие ранее разработанные виды Bacteroides spp. были назначены на другие роды в типе (отделе) Bacteroidetes. В настоящее время только четыре желудочно-кишечных Bacteroides spp. образуют глубокие ветви в филогенетическом дереве, что позволяет предположить, что эти бактерии (B. ureolyticus, B. galacturonicus, B. pectinophilus и B. coagulans) еще должны быть реклассифицированы в другие филогенетические группы. Аналогичная ситуация применима к Anaerorhabdus furcosa, которая до сих пор классифицируется как член семейства Bacteroidaceae, но основана на кластерах генных последовательностей генов SSU в типе Firmicutes. Большая часть представителей Bacteroidetes spp. желудочно-кишечного тракта принадлежит к следующим бактериальным семействам : Bacteroidaceae, Prevotellaceae, Rikenellaceae и Porphyromonadaceae (рис. 3)
Рис. 3. Филогенетическое древо желудочно-кишечного тракта человека, относящееся к классу Bacteroidia. Регистрационные номера последовательностей генов SSU рРНК из базы данных GenBank предоставлены для каждого вида с указанием семейства. В серой области изображены глубоко укоренившиеся виды Bacteroides spp., которые основаны на кластере последовательностей генов SSU рРНК в отдаленных филогенетических группах.
Из-за их широкого метаболического потенциала роль Bacteroidetes в желудочно-кишечной микробиоте является сложной: в то время как снижение численности Bacteroidetes в некоторых случаях связано с ожирением (Ley, 2010) и синдромом раздраженного кишечника (Rajilic-Stojanovic et al., 2011), эта бактериальная группа, по-видимому, обогащена у пациентов, страдающих диабетом типа 1 и типа 2 (Larsen et al., 2010). Кроме того, как недавно было обнаружено, Bacteroides spp. в отличие от Prevotella spp. обогащены метагеномами субъектов с низким генным богатством, которые были связаны с ожирением, инсулинорезистентностью и дислипидемией, а также воспалительным фенотипом (Le Chatelier et al., 2013).
Рис. 4. Филогенетическое древо желудочно-кишечного тракта человека, относящееся к классам Cytophagia и Sphingobacteria. Регистрационные номера последовательностей генов SSU рРНК из базы данных GenBank предоставлены для каждого вида с указанием семейства.
Виды Bacteroidetes, принадлежащие к классам Flavobacteriales и Sphingobacteriales, обнаруживаются только в желудочно-кишечном тракте (рис. 4). За исключением Capnocytophaga spp. и Sphingobacterium spp. которые могут быть обнаружены в полости рта человека, другие бактерии этой группы, как правило, связаны с другими экосистемами (прежде всего почвой). Нет данных о роли этих бактерий в желудочно-кишечной микробиоте, но следует отметить, что некоторые из этих бактерий были обнаружены только в библиотеках клонов генов SSU рРНК микробиоты пациентов с воспалительными заболеваниями кишечника (Frank et al., 2007).
Дополнитеьльно о бактероидетах см. ниже по ссылке →
Заключение
Знания, полученные в течение более чем столетия изучения микробиоты желудочно-кишечного тракта человека, показали, что эта экосистема действительно является «забытым органом» человеческого организма. Множество данных о микробиоте желудочно-кишечного тракта сильно разбросано во времени и в пространстве, а потому обзорная работа по систематизации полученных знаний в этой области крайне необходима.
В представленном разделе нашего сайта описание кишечных микроорганизмов в основном ограничено двумя типами. При этом Фирмикуты также описаны очень кратко, хотя и распределены по четырем классам: Bacilli, Clostridia, Erysipelotrichi и Negativicutes. Поэтому, при желании более подробного ознакомления с этими и другими группами ЖКТ-бактерий, рекомендуем самостоятельно прочитать первоисточник, на основе которой создана эта страница (ссылка указана ниже). Указанная работа, которую проделали ученые специалисты Мирьяна Раджилич-Стоянович (Сербия) и Виллем М. де Вос (Голландия), заслуживает особого внимания и уважения.
Хотя культивирование микробиоты желудочно-кишечного тракта является трудоемким, оно является важным этапом для детальной физиологической и биохимической характеристики отдельных изолятов желудочно-кишечного тракта, что необходимо для прогресса этой области исследований. Это все больше признается, и недавние исследования культивирования с высокой пропускной способностью доказали, что культивирование может быть использовано в качестве мощной методологии для обнаружения в настоящее время неизвестных обитателей желудочно-кишечного тракта (Lagier et al., 2012a; Dubourg et al., 2013; Pfleiderer et al., 2013). Будущее культивирование оставшейся части желудочно-кишечной микробиоты, как ожидается, улучшит наше понимание этой экосистемы.
Дополнительная краткая информация о представителях наиболее распространенных таксономических типов в составе микробиома человека.
Структура и характеристики микробиома кишечника
Эволюция микроорганизмов продолжалась в кишечнике животных длительное время, что привело к формированию сложной и богатой экосистемы. Кишечник млекопитающих густо заселен триллионами бактерий, принадлежащих к нескольким сотням различных видов [4]. Выделяют два вида разнообразия микробиоты человека: альфа-разнообразие (в пределах одного образца) и бета-разнообразие (между отдельными образцами). Несмотря на значительное разнообразие видов микроорганизмов в составе микробиоты, большинство представителей принадлежит только к четырем типам в современной биологической систематике: Bacteroidetes, Firmicutes, Actinobacteria и Proteobacteria. Типы Firmicutes и Bacteroidetes составляют более 90% бактериальной популяции в толстой кишке, где плотность микробиоты наибольшая. При этом представители типов Actinobacteria и Proteobacteria практически всегда присутствуют в составе микробиоты в относительно невысоком содержании [2,5]. Ниже мы охарактеризуем подробнее представителей наиболее распространенных таксономических типов в составе микробиома человека.
1. Bacteroidetes (Бактероидеты)
Тип Bacteroidetes представлен как анаэробными, так и аэробными неспорообразующими грамотрицательными бактериями, которые колонизируют практически все пространство кишечника. Род Bacteroides является одной из преобладающих групп в кишечнике в составе данного таксономического типа. Эти бактерии эффективно разлагают сложные полисахариды, устойчивые к пищеварительным ферментам человека. Биодеградация этих сложных углеводов дает на выходе набор короткоцепочечных жирных кислот (КЦЖК), а именно ацетат, пропионат и бутират, которые реабсорбируются организмом хозяина и вовлекаются в биохимические энергетические процессы. Кроме того, КЦЖК участвуют в регулировке дифференциации эпителиальных клеток кишечника [6], созревании и стимуляции иммунной системы [7], а также ряда других важных биологических процессов.
Несмотря на то, что представители рода Bacteroides вносят важный вклад в метаболические процессы человека и в целом поддерживают комменсальные отношения с хозяином, некоторые представители обладают потенциалом патогенности при резком повышении их относительной плотности в просвете кишечника. Примером является Bacteroides fragilis, который обычно локализуется в нижних отделах кишечника и, как было ранее показано, оказывает благотворное влияние на организм человека, например стимулирует развитие иммунной системы [8]. Однако, в то же время Bacteroides fragilis является одним из облигатных анаэробов, которые чаще всего вызывают инфекционные осложнения. Наиболее распространенной клинической формой в таких ситуациях являются интраабдоминальные абсцессы и инфекции кровотока, особенно у пациентов с нарушением барьерной функции слизистой кишечника или ее перфорацией.
Большинство представителей рода Bacteroides, колонизирующих кишечник, не являются этиологическими предпосылками возникновения кишечных инфекций, за одним исключением: энтеротоксигенные штаммы В. fragilis продуцируют токсин В, fragilis, который вызывает колит, а ранее также ассоциировался с риском развития опухолей толстой кишки [9,10]. Кроме того, у представителей рода Bacteroides spp. отмечается наличие целого ряда механизмов антибиотикорезистентности и регистрируются наиболее высокие уровни устойчивости к антибиотикам среди всех облигатных анаэробов [11].
2. Firmicutes (Фирмикуты)
Тип Firmicutes представлен как облигатными, так и факультативными анаэробными бактериями. Большинство представителей типа являются грамположительными бактериями и способны формировать эндоспоры, обеспечивая экологическое преимущество для выживания в неблагоприятных условиях. В форме эндоспор данные бактерии могут выживать при отсутствии питательных веществ и являются чрезвычайно устойчивыми к воздействию кислорода, ультрафиолетовому излучению, высыханию, экстремальным температурам и дезинфицирующим средствам. Данные формы позволяют представителям типа Firmicutes длительное время находиться в состоянии покоя и возвращаться к метаболически активному состоянию в благоприятных условиях.
Один из наиболее клинически значимых классов в составе типа Firmicutes — это класс Clostridia, который в связи с высокой гетерогенностью дополнительно разделен на кластеры. Именно среди представителей кластеров Clostridium XlVa и IV были выявлены полезные микроорганизмы, принимающие участие в реализации функций ЖКТ человека. Установлено, что данные бактерии концентрируются в складках слизистой оболочки кишечника, поддерживая и регулируя функции кишечного эпителия [12]. Виды в составе данных кластеров, так же как и представители Bacteroides spp., продуцируют КЦЖК (бутират) в результате процессов ферментации, что способствует поддержанию функции кишечного эпителия. К тому же было выявлено, что представители этих кластеров поддерживают локальный иммунный гомеостаз кишечника посредством привлечения регуляторных Т-лимфоцитов толстого кишечника [13].
Стоит подчеркнуть, что другие кластеры класса Clostridia включают важные патогены, которые могут вызывать инфекционные заболевания человека, а именно: представители кластера I — С. perfringens и С. tetani, а также кластера XI — С. difficile [14]. Наконец, еще один клинически значимый класс в составе типа Firmicutes — это класс Bacilli. Известными его представителями являются кислородоустойчивые бактерии Enterococcus spp. и Streptococcus spp., которые обычно определяются в кишечнике в низком относительном содержании, но обладают потенциалом к избыточному росту при различных патологических состояниях [15].
3. Actinobacteria (Актинобактерии)
Тип Actinobacteria состоит как из аэробных, так и анаэробных грамположительных бактерий, однако отличается от типа Firmicutes более высоким содержанием гуанина и цитозина в структуре ДНК. Bifidobacteria spp. являются наиболее распространенными обитателями ЖКТ в рамках данного типа [4]. Ранее было показано, что отдельные виды в пределах этого рода, в том числе В. longum, имеют пробиотические функции. В частности, данные микроорганизмы обеспечивали защиту от кишечных патогенов с помощью ряда процессов, а именно: прямой конкуренции, активности гидролазы желчных кислот, модуляции локального иммунного ответа и способности создавать высокую пристеночную концентрацию вблизи кишечного эпителия [1,16].
4. Proteobacteria (Протеобактерии)
Тип Proteobacteria включает в себя широкий спектр грамотрицательных микроорганизмов. В то время как основную массу бактерий ЖКТ составляют облигатные анаэробы, представители типа Proteobacteria являются факультативными анаэробами. Несмотря на то, что протеобактерии являются естественными обитателями ЖКТ человека, как правило, они являются меньшинством в структуре здорового дифференцированного микробиома. В составе типа стоит отметить семейство Enterobacteriaceae (класс Gammaproteobacteria), включающее многих возбудителей инфекционных осложнений, а именно Escherichia coli и Klebsiella spp., которые обычно регистрируются в микробиоме ЖКТ в низком количестве, но имеют потенциал для чрезмерного роста и кишечного доминирования на фоне антибиотикотерапии и отдельных заболеваний [3,15].
5. Анатомическое распределение микробиоты
С точки зрения расположения микроорганизмов и условий локального биоценоза ЖКТ человека состоит из желудка, тонкой кишки, слепой кишки, ободочной кишки и прямой кишки. Имеется несколько важных показателей, претерпевающих изменения в среде вдоль этого тракта. Например, рН и концентрация кислорода значительно меняют свои уровни, начинаясь от кислой среды и аэробных условий желудка и перетекая в нейтральную и анаэробную среду толстой кишки. Кроме того, источники питательных веществ для колонизирующих микроорганизмов меняются на протяжении всей длины ЖКТ [17]. В частности, наиболее простые углеводы всасываются в терминальной подвздошной кишке, и, следовательно, в отделах ЖКТ ниже илеоцекального клапана бактерии усваивают непереваренные хозяином углеводы, сложные молекулы, а также мукопротеины. В результате комбинации вышеописанных факторов бактерии имеют специфическое распределение в кишечнике человека. В толстой кишке общая плотность бактерий больше, чем в тонком кишечнике. В целом, в составе микробима тонкой кишки преобладают представители Lactobacillales или Proteobacteria. Однако в толстом кишечнике уже Bacteroides и Clostridiales становятся доминирующими в составе микробиома [18].
6. Возрастная динамика микробиома у детей
Эволюция и созревание кишечного микробиома на ранних стадиях жизни являются важным фактором поддержания здоровья, а нарушение на ранних этапах формирования микробного сообщества у ребенка предрасполагает к развитию заболеваний, как в младенчестве, так и в зрелом возрасте, что наиболее изучено в контексте аллергических заболеваний и метаболических синдромов. Особенно интересно то, что после родов естественным путем микробиота новорожденных заселяется бактериями родового канала матери, а у новорожденных после выполнения кесарева сечения микробиота заселяется в основном бактериями, населяющими кожу взрослого человека, при этом стрептококки становятся доминирующим видом в составе микробиоты у таких детей [19]. Также было высказано предположение, что данное обстоятельство может представлять собой фактор, предрасполагающий к последующему развитию инфекций в детском возрасте [19]. Весьма значимыми являются результаты исследования, в ходе которого авторы после проведения кесарева сечения выполняли обработку кожных покровов новорожденных тампоном, смоченным в содержимом влагалища матери, что приводило к формированию адекватного состава микробиоты, сходного с характеристиками микробиоты детей после родов через естественные родовые пути [20].
Исследования, включающие тысячи детей, выявили связь между использованием антибиотиков в течение первого года жизни и риском развития бронхиальной астмы к 6-7 годам 23. Более того, отдельные авторы приводили данные о повышении риска развития бронхиальной астмы у детей дошкольного возраста, чьи матери получали антибиотики в третьем триместре беременности [25,26]. Финскими исследователями было выявлено, что назначение макролидов у детей в возрасте 2-7 лет приводит к формированию особого профиля микробиоты, характеризующегося потерей представителей Actinobacteria и увеличением плотности Bacteroidetes и Proteobacteria, индукцией генов антибиотикорезистентности и снижением активности гидролаз желчных кислот. При этом данный профиль микробиоты положительно коррелировал либо с развитием впоследствии бронхиальной астмы, либо с увеличением индекса массы тела [27]. Связь применения антибиотиков в первый год жизни и повышения индекса массы тела у мальчиков в возрасте 5-8 лет впоследствии была также отражена в британском исследовании, где авторы подчеркнули роль микробиома в регуляции массы тела [28].
В дополнение к обсервационным исследованиям с участием людей имеются экспериментальные исследования о влиянии антибиотиков на микробиоту и заболевания у мышей. В частности, исследователями было продемонстрировано, что введение антибиотиков новорожденным мышам приводило к выраженным изменениям состава микробиома и впоследствии к развитию осложненных астматических эпизодов после интраназальной нагрузки овальбумином, чего, однако, не наблюдалось при введении антибиотиков уже взрослым особям [29]. Важность вертикальной передачи микробиоты во время беременности подчеркивается в опубликованной работе о наибольшем отрицательном влиянии введения малых доз пенициллина на состав микробиома именно в ранние сроки гестации [30]. Авторы в эксперименте на мышах показали, что у животных, получивших малые дозы пенициллина во время гестации, впоследствии отмечалось увеличение массы тела, повышение содержания жировой ткани в организме, а экспрессия генов, кодирующих отдельные важные белки (дефензины и ИЛ-17 ), была снижена.
Интересным примером со стороны животного мира является инстинкт употребления новорожденными жеребятами экскрементов матери. При этом данный инстинкт проявляется у различных пород животных вне зависимости от географической зоны обитания. Долгое время в ветеринарии выдвигались предложения о восполнении таким образом дефицита отдельных нутриентов, однако в связи с внедрением молекулярно-генетических методов исследования, на сегодняшний день вполне ясно, что это инстинктивный метод заселения микробиома кишечника и стимуляции иммунной системы, которая характеризуется незрелостью механизмов даже у доношенных жеребят [31].
Таким образом, воздействие антибиотиков даже на короткие промежутки времени и особенно во время беременности и детского возраста оказывает долговременное воздействие на микробиом, что может впоследствии повышать риск развития целого ряда заболеваний. Это, очевидно, представляет собой чрезвычайно важное значение для общественного здравоохранения и стратегии назначения антибиотиков в акушерстве и гинекологии, а также педиатрии.
Состав микробиома кишечника в динамике у ребенка показан нна рисунке 5 (анализ микробиома на уровне семейств микроорганизмов). Нормальная хронология созревания и заселения микробиоты кишечника у детей выражается поэтапно: На 1-м этапе постнатального заселения бактериями (дни 3-84) микробиом кишечника у детей содержит ограниченный набор представителей типа Firmicutes. Второму этапу заселения предшествует увеличение количества представителей Proteobacteria (дни 92-100), что часто совпадает с ранее необъяснимыми эпизодами лихорадки у детей. Количество Actinobacteria и Proteobacteria увеличивается на 2-м этапе, а видовой состав Firmicutes на данном этапе выраженно отличается от первоначального. На 3-м этапе формирования микробиома введение детского питания в дополнение к грудному молоку и приобщение к «взрослому» столу ассоциируется с увеличением количества Bacteroidetes (дни 172-297), что также продолжается и на 4-м этапе (дни 454-838), однако конкретные представители типа Bacteroidetes в микробиоме отличаются между этими двумя этапами.
Период выраженного перехода в структуре микробиома между 3-м и 4-м этапами (дни 371-441) может быть обусловлен рядом факторов внешней среды, имеющих влияние на ребенка, например: первый контакт с антибиотиками, исключение грудного молока и питательных смесей из рациона питания, введение коровьего молока и полноценной взрослой диеты. Интересно, что микробиом переходного периода, предшествующего 4-му этапу, содержит микроорганизмы, типичные для уже завершенного первого этапа, которые можно трактовать как следы неонатального микробиома.
Стоит отметить, что видовой состав микробиома у ребенка относительно стабилен именно на 4-м этапе, что было подтверждено метагеномным анализом более 400 образцов [32]. Введение в рацион питания продуктов со взрослого стола приводит к выраженному сдвигу в типовом составе микробиома, а также увеличивает абсолютное количество бактерий и короткоцепочечных жирных кислот ( КЦЖК или SCFAs) в кишечнике ребенка. Резкое и устойчивое повышение уровня бактерий типа Bacteroidetes после начала регулярного прикорма ребенка вполне объяснимо: именно данные бактерии специализируются на ферментации сложных растительных полисахаридов [33]. Кроме того, в экспериментальных работах на мышах включение растительных углеводов в схему питания также незамедлительно повышало уровень Bacteroidetes в составе кишечного микробиома [34]. В то же время высокая метаболическая активность данных бактерий прямо или косвенно приводит к увеличению продукции КЦЖК (ацетата, пропионата, бутирата) в кишечнике. Более того, было продемонстрировано, что низкое содержание Bacteroidetes в кишечном микробиоме ассоциируется с ожирением, что само по себе может наблюдаться на фоне диеты, бедной сложными растительными полисахаридами [35,36]. Таким образом, вместе эти результаты подтверждают мнение о том, что диета с высоким содержанием продуктов растительного происхождения способствует созданию разнообразного и полноценного микробного сообщества кишечника, в том числе и у детей, а также адекватному производству энергетических субстратов и метаболитов, необходимых организму человека.
Ключевая информация подраздела
Микробиом кишечника человека состоит из приблизительно 100 триллионов бактерий, принадлежащих нескопьким сотням различных видов [4]. Микробиом включает в себя 4 основных типа бактерий, охватывающих более 90% общей популяции микроорганизмов, а именно типы: Firmicutes, Bacteroidetes, Actinobacteria, Proteobacteria, а также ряд более редких типов — Verrucomicrobia и Fusobacteria. Соотношение и состав данных типов бактерий значительно варьируется вдоль желудочно-кишечного тракта, а также изменяется под влиянием различных факторов внешней среды и доступности питательных веществ [2]. Эволюция и созревание микробиома у детей проходит в 4 этапа и характеризуется как количественным, так и качественным изменением состава бактерий кишечника, происходящим под влиянием перемены рациона питания и внешних факторов.
Микробиота человека: формирование через жизненные стадии и нарушения
На графике представлен общий обзор относительного обилия ключевых типов состава кишечной микробиоты человека на разных этапах жизни. Измеряется с помощью секвенирования 16S рРНК или метагеномных подходов (ДНК). Данные поступают из исследований со следующими условиями: грудное и искусственное вскармливание (Schwartz et al., 2012 ), детское твердое питание (Koenig et al., 2011 ), антибиотики для малышей (Koenig et al., 2011 ), здоровый или истощенный малыш (Monira et al., 2011 ), взрослые, пожилые и 100-летние здоровые (Biagi et al., 2010 ) и взрослые, страдающие ожирением (Zhang et al., 2009 ).
Источник: Ottman N, Smidt H, de Vos WM, Belzer C et al. The function of our microbiota: who is out there and what do they do? Front Cell Infect Microbiol. 2012 Aug 9;2:104
Различия в микробиоте у детей в Европе и Африке. (A и B) Круговые диаграммы медианных значений бактериальных родов, присутствующих в образцах фекалий детей BF и EC (>3%), найденных по классификатору RDP v. 2.1. Кольца представляют соответствующий тип (Bacteroidetes в зеленом и Firmicutes в красном) для каждого из наиболее часто представляемых родов.
Влияние рациона питания на формирование микробиоты кишечника
Микробный состав кишечника зависит от различных пищевых привычек, так же как здоровье зависит от микробного метаболизма, но связь микробиоты с различными диетами в человеческих популяциях не до конца изучена. В 2010 г. в своей работе De Filippo C. et al. сравнили фекальную микробиоту 15 здоровых европейских детей (ЕС), проживающих в городской зоне Флоренции в Италии и 14 здоровых детей из этнической группы Мосси в африканской деревне Булпон в Буркина-Фасо (BF), где диета с высоким содержанием клетчатки похожа на диету ранних человеческих поселений во время зарождения сельского хозяйства. Возраст детей составлял от 1 до 6 лет.
Используя высокопроизводительное секвенирование 16S рДНК и биохимический анализ, ученые обнаружили значительные различия в микробиоте кишечника между двумя группами. Дети BF показали значительное обогащение Bacteroidetes и истощение у Firmicutes (P
Дети из деревни Булпон были выбраны в качестве репрезентативных потребителей традиционной сельской африканской диеты. Рацион питания детей BF отличается низким содержанием жира и животного белка, богат крахмалом, клетчаткой, растительными полисахаридами и преимущественно вегетарианский.
Все продовольственные ресурсы полностью производятся на местном уровне, выращиваются и заготавливаются в окрестностях деревни женщинами. Рацион BF состоит в основном из зерновых (пшено, сорго), бобовых (черноглазый горох, называемый Ньебе) и овощей, поэтому содержание углеводов, клетчатки и неживотного белка очень высокое. Хотя потребление животного белка очень низкое, иногда они едят небольшое количество мяса (курицы) и термитов, которые являются частью рациона детей BF в сезон дождей.
Таким образом, ученые выдвинули гипотезу, что кишечная микробиота развивалась вместе с богатой полисахаридами пищей детей из Буркина-Фасо, позволяя им максимально увеличить потребление энергии из волокон, а также защищаться от воспалений и неинфекционных заболеваний толстой кишки. Исследование указывает на важность сохранения сокровища микробного разнообразия у древних сельских общин по всему миру.
Для лучшего понимания темы см. дополнительно:
См. дополнительно:
Литература к 1-8 пп.:
Литература к 9 пп.
Будьте здоровы!
ССЫЛКИ К РАЗДЕЛУ О ПРЕПАРАТАХ ПРОБИОТИКАХ