если в крахмал добавить йод что будет
Если в крахмал добавить йод что будет
Описание:
Одно из свойств крахмала – это способность давать синюю окраску при взаимодействии с йодом. Эту окраску легко наблюдать, если поместить каплю раствора йода на срез картофеля или ломтик белого хлеба. Крахмал в качестве резервного питания накапливается в клубнях, плодах, семенах растений. Так, в клубнях картофеля содержится до 24 % крахмала, в зёрнах пшеницы — до 64 %, риса — 75 %, кукурузы — 70 %.
С помощью йода можно открыть самые незначительные количества крахмала.
йод + крахмал => соединение темно-синего цвета
К разбавленному раствору крахмала добавляем немного раствора йода. Появляется синее окрашивание. Нагреваем синий раствор. Окраска постепенно исчезает, так как образующееся соединение неустойчиво. При охлаждении раствора окраска вновь появляется. Данная реакция иллюстрирует обратимость химических процессов и их зависимость от температуры.
Если более подробно, то.
Крахмал представляет собой природный полимер. Причем крахмал не индивидуальное вещество, а смесь двух полимеров состава (С6Н10О5)n –амилозы (10–20 %) и амилопектина (80–90 %), состоящих из остатков a-D-глюкозы.
В целом крахмал – это белое твердое вещество без запаха и вкуса, малорастворимое в холодной воде.
Являясь многоатомным спиртом, крахмал образует простые и сложные эфиры. Характерной качественной реакцией на крахмал является его реакция с йодом.
При взаимодействии йода с крахмалом образуется соединение включения (клатрат). Клатрат – это комплексное соединение, в котором частицы одного вещества («молекулы-гости») внедряются в кристаллическую структуру «молекул-хозяев». В роли «молекул-хозяев» выступают молекулы амилозы, а «гостями» являются молекулы йода. Попадая в спираль, молекулы йода испытывают сильное влияние со стороны своего окружения (ОН-групп), в результате чего увеличивается длина связи до 0,306 нм (в молекуле йода длина связи 0,267 нм). Данный процесс сопровождается изменением бурой окраски йода на сине-фиолетовую (lмакс 620–680 нм).
Амилопектин, в отличие от амилозы, дает с йодом красно-фиолетовое окрашивание (lмакс 520–555 нм). Хотя содержание амилопектина в зернах крахмала в несколько раз превышает количество амилозы, тем не менее синее окрашивание, возникающее при действии йода на амилозу, перекрывает красно-фиолетовую окраску амилопектина. Окраска исчезает при нагревании и восстанавливается при охлаждении крахмального клейстера.
Крахмал широко распространен в растениях и является для них резервным источником энергии. В основном он содержится в клубнях, семенах и корнях в виде зерен.
Крахмал используют как пищевой продукт, компонент лекарственных средств и для накрахмаливания белья. Его применяют для получения патоки, глюкозы и этилового спирта, а также в аналитической химии для обнаружения йода.
Йодная проба на крахмал
В этой статье мы разъясним, для чего выполняется йодная проба затора/сусла (тест на крахмал), как это работает и как лучше всего выполнять.
Цветовая реакция между йодом и глюкозными цепями (декстрины и крахмал) используется для определения их присутствия в сусле. Помимо производства сусла желаемой ферментируемости, целью затирания является уменьшение максимальной длины декстринов в сладком сусле до менее 9 молекул глюкозы для неразветвленных и менее 60 для разветвленных цепей. В этом случае они больше не проявляют реакцию с йодом, а сусло или затор называют йодоотрицательным. Если это не будет сделано, и эти длинные цепи глюкозы будут перенесены в пиво, то в нем может развиться так называемое «крахмальное помутнение». Несмотря на свое название, в большинстве случаев эта муть не вызвана самим крахмалом, а вызвана длинными декстринами, которые становятся менее растворимыми и выпадают в осадок в присутствии алкоголя. Эти декстрины дают цветовую реакции с йодом от красной до фиолетовой.
Как это работает?
Когда глюкозные цепи достаточно длинные, они становятся подобны пружинам. Эти пружины поддерживается слабыми связями между молекулами глюкозы. Эти связи разрушаются при высоких температурах, и цепи глюкозы разматываются, поэтому тест на йод работает только с образцами холодного сусла и затора.
Когда цепи длиннее, чем 9 молекул глюкозы, трийодидный ион (I3-) встраивается внутрь пружины (рис. 1). Полученная йодно-декстриновая молекула поглощает свет, что является причиной типичной цветовой реакции между йодом и крахмалом. Чем длиннее цепи глюкозы, тем больше молекул йода встраивается в пружины, и тем интенсивнее будет цветовая реакция.
Полученный цвет зависит от длины цепей глюкозы. Более короткие цепи (начиная с около 9 молекул глюкозы в неразветвленных цепях и до 60 молекул глюкозы в разветленных) дают красный цвет. Эти декстрины также называются эритродекстринами. Амилоза, которая состоит из очень длинных цепочек глюкозы между случайными точками ветвления и очень большими декстринами, дает темно-синий цвет, тогда как амилопектин, который имеет гораздо больше точек ветвления и более короткие глюкозные цепи между этими точками, дает более красноватый цвет при наличие йода.
Растворы йода
Йод сам по себе очень плохо растворим в воде. Одним из способов его растворения является добавление йодистого калия или натрия. Эти соли растворяются в ионах калия или натрия и ионах йода. Ион йода (I-) реагирует со свободным йодом (I2) с образованием трийодидного иона (I3-), который растворим в воде и может реагировать с глюкозными цепями.
Раствор йода и йодистого калия также называют роствором Луголя, который был одним из первых в качестве йодного дезинфицирующего средства.
Дальнейшие усовершенствования привели к использованию других более растворимых агентов, содержащих продукты йода, который мы используем сегодня с целью очистки и дезинфекции (см. Повидон-йод, Википедия). Все эти продукты содержат свободный йод в растворе и поэтому подходят для йодной пробы.
Концентрированные растворы йода во время варки лучше всего разбавлять этанолом. Это делается в основном для того, чтобы тестовый раствора был светло-желтого цвета, чтобы лучше наблюдать изменения в цветовой реакции. Этанол лучше подходит для разбавления йода, чем вода из-за лучшей растворимости йода в спирте.
Раствор для крахмального теста, приготовленный из йода Лугола, имеет тенденцию давать более четкую реакцию с крахмалом, чем препарат, приготовленный из йодоформа. Это может быть связано с тем, что йодоформ вступает в реакцию медленнее по сравнению с йодом Луголя, но оба решения по-прежнему одинаково хорошо подходят для тестирования крахмала в пивоварении.
Очевидно, что тестовый раствор для йода лучше всего хранить в маленькой бутылке с пипеткой, обозначенной как «тест на крахмал».
Выполнение йодной пробы
В пивоварении йодную пробу лучше всего делать на куске белого мела или гипсокартона. Я использую кусок белого тротуарного мела, который был взят из ведерка с детскими мелками. Существует два основных преимущества этой практики по сравнению с йодной пробой, например, на белой пластине. С одной стороны мел принимает только каплю сусла и таким образом исключает шелуху или разные песчинки. Другая причина заключается в том, что этот метод позволяет увидеть йодный раствор для теста, который смог прореагировать или не прореагировал с образцом сусла, что устраняет неопределенность в том, откуда красноватый цвет мог появится.
Если мела нет под рукой, то обычная или фильтровальная бумага также подойдет, если она не содержит крахмал. Некоторая бумага содержит крахмал, и добавление капли йодного раствора покажет это.
Альтернативные методы проверки крахмала
Большинство пивоваров научились проводить тест на крахмал в белом блюдце. Проблема с этим методом заключается в том, что взятый образец затора может содержать частицы шелухи и зерна, которые могут реагировать с йодом и приводить к ложному показанию. Чтобы выполнить тест, возьмите образец сусла без шелухи или частей эндосперма и поместите его на белое блюдце. Затем добавьте раствор для проверки крахмала и наблюдайте за цветовой реакцией.
Примеры йодной пробы
Белый + коричневый = синий! Это возможно? Опыт с крахмалом и водой
Всем большущий привет!
Александра и Артём приветствуют вас в своей домашней лаборатории!
Уверены, что такую лабораторию можно устроить в каждом доме. Ведь для этого не потребуются какие-то сложные химические приспособления и физические приборы. Потребуется то, что всегда под рукой. А вот без чего никак не обойтись, так это без вашей любознательности, исследовательской жажды и хорошего настроения.
Хотите узнать, чем Саша и Тёма займутся сегодня? На очереди у наших юных экспериментаторов занимательный опыт с крахмалом и водой.
Как соединив вещество белого цвета с веществом коричневого цвета получить синий цвет? «Это невозможно!» — скажете вы.
Хмм… Ребята сначала тоже так думали. Но…
В общем, смотрите сами) Только внимательно! А потом попробуем сделать описание того, что увидели.
Ход эксперимента
Объяснение
Почему же капля йода окрасила крахмальную воду в сине-фиолетовый цвет? Впрочем, как и от природы крахмальную картошку?
Здесь все дело в реакции йода с крахмалом.
Крахмал очень интересное вещество. Это только кажется, что он однородный. А на самом деле он состоит из двух разных веществ, так называемых полимеров:
Молекула амилозы очень длинная и похожа на спираль. А внутрь этой спирали встраиваются молекулы йода. Образуется новое соединение, называемое соединением «включения» под названием клатрат. В этом новом соединении молекулы одного вещества, которых называют «гости», встраиваются в молекулы другого вещества, которое называют «хозяином».
Гости – это молекулы йода.
А хозяин — это молекула амилозы.
Вот это соединение и придает йоду новую сине-фиолетовую окраску. Интересно, а что же делает в этот момент вторая составная часть белого крахмального порошка под названием амилопектин? Да тоже окрашивается, но только в красный цвет. Но мы этого не замечаем. Так как сине-фиолетовый цвет забивает красный.
Интересно, что если мы нагреем полученный синий раствор, то он вновь станет белым, а когда остынет, то вновь посинеет. Чудеса да и только!
С помощью полученных знаний вы легко сможете проверить наличие крахмала там, где его быть не должно, например, в сметане. Просто капните в сметану капельку йода. Видите синий цвет? Тогда производители сметаны вели себя не очень хорошо. Только не капайте прямо в баночку, лучше переложите немножко сметаны на блюдечко и проведите опыт с небольшим ее количеством.
Знаете для чего еще применяют крахмал? Его широко используют в пищевой промышленности, например, при изготовлении колбасы, печенья и даже мороженного. А еще с его помощью можно накрахмалить белье, после чего оно становится приятным на ощупь, не так сильно мнется и дольше служит.
А еще с помощью крахмала можно:
А вот для чего нужен йод, я думаю, все прекрасно знают)
Ну вот, сегодня мы узнали еще немного больше. Значит, день прошел не зря! Попробуйте сделать этот эксперимент самостоятельно. Еще больше интересных опытов с водой найдете здесь и вот здесь.
Ну а в будущих выпусках нашей домашней лаборатории обязательно расскажем вам о том, как с помощью простых ингредиентов приготовить настоящую неньютоновскую жидкость.
Так что заходите в гости почаще! Не пропустите!
Желаем вам разных нескучностей!
Ваши Артём, Александра и Евгения Климкович.
Table of Contents:
Видео дня
Слюна и крахмал Пищеварение
Шаг 1
Налейте чайную ложку воды в одну из пробирок. Отметьте эту «трубку А» куском маскировочной ленты.
Шаг 2
Впейте в чайную ложку, пока она не заполнится. Вылейте слюну во вторую пробирку. Отметьте эту «трубку B» куском маскировочной ленты.
Шаг 3
Измерьте 1/4 чайной ложки кукурузного крахмала и поместите в каждую пробирку. Встряхните каждую пробирку, чтобы растворить крахмал.
Шаг 4
Наденьте защитные очки. Заполните глазную капельницу йодом.
Шаг 5
Поместите четыре капли йода в каждую пробирку. Наблюдайте, как жидкость в обеих трубах превращается в синий цвет.
Шаг 6
Поместите пробирки в держатель и оставьте их ненарушенными в течение 30 минут.
Шаг 7
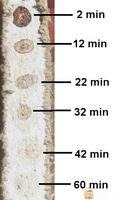
Проверьте цвет через 30 минут. Пробирка, наполненная водой и кукурузным крахмалом, по-прежнему будет фиолетовой. Но пробирка с слюной осветлит или даже станет ясной. Это потому, что ферменты в слюне разрушают крахмал. Это показывает первые шаги в пищеварении.
Изучение содержания витамина С в соке
Шаг 1
Налейте чашку воды в миску. Добавьте 2 столовые ложки кукурузного крахмала и смешайте с вилкой до полного растворения крахмала.
Шаг 2
Наденьте защитные очки. Заполните пипетку йодом. Добавьте йод в смесь кукурузного крахмала по одной капле за раз, пока вся смесь не станет темно-синего цвета. Опорожните остальную часть пипетки. Промойте капельницу водой.
Шаг 3
Налейте 2 столовые ложки смеси йода и кукурузного крахмала в четыре пробирки и поместите их в стойку. С липкой лентой и ручкой наклейте каждую пробирку на оранжевый, лимонный, яблочный или вишневый сок.
Шаг 4
Заполните пипетку апельсиновым соком. Поместите две капли в первую пробирку. Закрутите трубку для смешивания раствора. Продолжайте добавлять сок и закручивать до тех пор, пока не будет ясно. Запишите количество капель, необходимых для устранения проблемы.
Шаг 5
Повторите с тремя другими соками, записав количество капель для каждого сока. Поскольку аскорбиновая кислота или витамин С прекращают реакцию между кукурузным крахмалом и йодом, сок с самым высоким содержанием витамина С потребует наименьших капель, чтобы очистить раствор. Соки, содержащие меньше витамина С, потребуют больше капель сока, чтобы очистить раствор.
Если в крахмал добавить йод что будет
Исследовательские работы и проекты
Опыты и наблюдения с крахмалом
Опыты с крахмалом
Опыт 1. Крахмал и йод.
Цель: проверить присутствие крахмала при помощи йода.
Налил воду в два стакана. В один из них насыпал крахмал. В каждую воду добавили 2-3капли йода. В том стакане, где была простая вода, она пожелтела. А в том стакане, где был раствор с крахмалом, он посинел.
Вывод: можно проверить присутствие крахмала одной каплей раствора йода.
Опыт 2. Крахмал в продуктах
Мне понадобилось: йод, пипетка, пищевые продукты.
Цель: выявить наличие крахмала в продуктах.
С помощью пипетки капнул йод на маленький кусочек хлеба, сыра, печенья, картофеля, лимона
Вывод: йод изменил свой цвет на хлебе, печенье, картофеле, значит, в этих продуктах присутствует крахмал. А вот на сыре и лимоне цвет йода не изменился, значит, крахмала нет.
Опыт 3. Твёрдая жидкость
Мне понадобилось: 1,5 части кукурузного крахмала;1 часть воды; пищевые красители.
Цель: узнать, что образуют вода и крахмал. Смешал крахмал и воду. Медленно опустил в полученную жидкость пальцы. Жидкость стекает. Со всей силы ударил по ней кулаком. Поверхность жидкости превратилась в упругую массу.
Цель: узнать, что происходит с крахмалом в холодной воде.
Мне понадобилось: крахмал, стакан холодной воды.
В холодную воду крахмал опустили. Мутный раствор недолго стоял, на дно опустился осадок – крахмал.
Вывод: крахмал не растворяется в холодной воде и не набухает.
Опыт 5. Крахмальный клейстер
Цель: узнать, как кипяток влияет на крахмал.
Мне понадобилось: крахмал, стакан кипятка.
Решил я опыт свой повторить, крахмал кипятком в стакан заварить. В липкую массу он превратился, как клей. И кисель получился!
Вывод: крахмал, залитый кипятком, набухает и становится клейким. Это свойство крахмала используют как загуститель, в качестве бумажного клея.
Опыт 6. Молочные продукты и крахмал
Цель: узнать, есть ли в составе молочных продуктов крахмал.
Мне понадобилось: молочный продукт и крахмал.
Капнул несколько капель йода на творог. Реакции йода с крахмалом нет.
Вывод: в натуральных молочных продуктах крахмала быть не должно. Но некоторые производители, для того чтобы сделать продукт более густым, добавляют крахмал или муку.
Опыт 7. Магическая надпись
Цель: посмотреть взаимодействие крахмала и йода.
Мне понадобилось: Ватман, вода, йод, крахмал, распылитель.
Ватман обработал смесью воды с крахмалом, кроме отдельных частей, где написано название «УДИВИТЕЛЬНЫЙ КРАХМАЛ». Взял распылитель и побрызгал на него раствором – это смесь воды с йодом. В результате, название моей работы «УДИВИТЕЛЬНЫЙ КРАХМАЛ» выглядит как белые буквы на фиолетовом фоне.
Вывод: при взаимодействии крахмала и йода происходит химическая реакция, которая образует сложные молекулы фиолетового цвета. Соответственно, участки листа, необработанные смесью воды с крахмалом, остаются белыми. (Приложение № 8)
Таким образом, опыты помогли мне узнать много нового и интересного. Свойства крахмала можно использовать в самых разных сферах жизни. В ходе экспериментов обнаружил продукты питания из повседневного рациона, в которых содержится крахмал, нашёл продукты, в которых его нет.
Это исследование еще раз убедило меня в том, что для получения ответов на вопросы, не обязательно ждать, когда мы начнём изучать химию. Можно просто устроить лабораторию на кухне!
Заключение
Практическая значимость моего проекта заключается в том, что о результатах исследования можно рассказать на уроках окружающего мира, конференции или классном часе. Познакомить одноклассников с технологией опытов по обнаружению крахмала в продуктах питания. Предложить памятки по использованию крахмала в домашних условиях.
Список литературы
Приложение
Вопросы анкетирования
Положительные свойства крахмала
Приложение № 2. Рецепт приготовления крахмала в домашних условиях
Пошаговый рецепт
Для начала я начистил 5 средних картофелин, натёр их в крупную терку. Поставил чашку с водой в тёплое место.
Залил тёплой водой натёртый картофель. Затем тщательно отжал и дал постоять 30 минут, затем еще раз отжал. Через дуршлаг отделил воду от картофеля.
После того, как испарилась вся вода, на дне остался чистый картофельный крахмал!
Изготовление лизунаиз крахмала в домашних условиях
Нам понадобится: крахмал; вода; клей ПВА; красители; плотный пакетик небольшого размера.
Изготовление игрушкииз крахмала в домашних условиях
Нам понадобится: воздушный шарик (без картинки), крахмал, чайная ложка, воронка, перманентный несмываемый маркер, разные ленточки, разноцветная шерсть (для украшения).