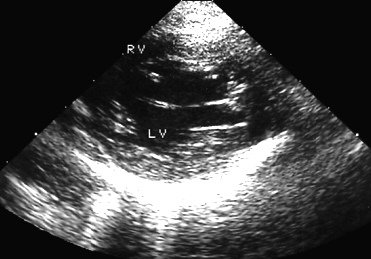
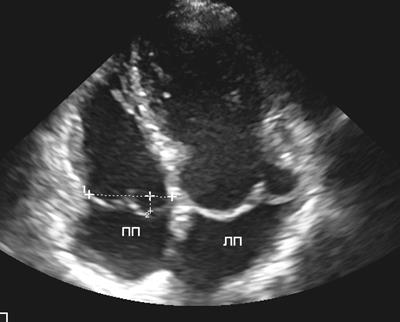
евстахиев клапан в правом предсердии чем грозит
Тромбоэмболия сети Хиари и легочной артерии
ФГБУ «Центральная клиническая больница с поликлиникой» Управления делами Президента РФ, 121356 Москва, ул. Маршала Тимошенко, 15
В статье представлено клиническое наблюдение пациента c тромбоэмболией сети Хиари и легочной артерии вследствие тромбоза вен нижних конечностей. Сеть Хиари встречается в небольшом проценте случаев в правом предсердии и обычно не имеет существенного клинического значения. Однако иногда она может быть ассоциирована с такими патологическими изменениями, как открытое овальное окно, внутрипредсердный тромбоз или предсердные аритмии. В данном случае сеть Хиари выступила в качестве преграды, задержавшей продвижение тромба.
Сеть Хиари выявляется в популяции в 2% случаев и представляет собой фиброзно-нитевидную структуру в виде сетки, которая прикрепляется к клапану нижней полой вены (евстахиев клапан) с одной стороны и к различным частям правого предсердия (ПП) — с другой [1]. Наряду с евстахиевым клапаном сеть Хиари может прикрепляться к клапану основного венозного коллектора, впадающего в ПП коронарного синуса (тебезиев клапан), к терминальному гребню, расположенному в зоне устья верхней полой вены, межпредсердной перегородке и стенке предсердия [1].
Обычно сеть Хиари не имеет существенного клинического значения. Однако в литературе периодически появляются описания случаев, в которых сеть Хиари играет определенную функциональную роль. С подобным случаем довелось столкнуться и нам.
Описание клинического наблюдения
Больной М., 68 лет, поступил в отделение нарушений ритма сердца ФГБУ «ЦКБ с поликлиникой» УДП РФ в январе 2014 г. с жалобами на сердцебиение и перебои в работе сердца, общую слабость, головокружение.
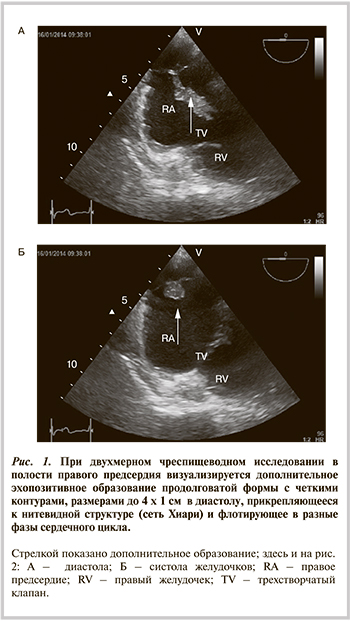
Из анамнеза известно, что больной страдает рядом сопутствующих заболеваний, таких как хронический бронхит, эмфизема легких, диффузный пневмосклероз, многоузловой эутиреоидный зоб, аденома предстательной железы, хронический простатит.
При поступлении в стационар состояние средней тяжести, периферических отеков нет, температура тела 36,6 °С. Периферические лимфатические узлы не увеличены. При аускультации легких дыхание жесткое, проводится во все отделы, хрипов нет. При аускультации сердца тоны сердца приглушены, аритмичные. Частота сердечных сокращений около 140 уд/мин, дефицита пульса нет. АД 130/85 мм рт.ст. Живот мягкий, при пальпации безболезненный. Печень выступает на 1 см из-под края реберной дуги. Селезенка не пальпируется. Стул в норме. Дизурических явлений нет.
Пациент в сознании, контактен, ориентирован. Острой очаговой неврологической и менингеальной симптоматики нет.
При поступлении в клиническом анализе крови эритроцитоз (эр. 6,03×1012/л при норме до 5,6×1012/л; Hb 168 г/л при норме до 160 г/л), нейтрофилез за счет сегментоядерных форм (н. 6,16×109/л при норме до 5,9×109/л, с. 78% при норме до 72%), лимфоцитопения (лимф. 1,155×109/л при норме от 1,2×109/л; 15% при норме от 19%), тромбоцитопения (тр. 121×109/л при норме от 180×109/л), остальные показатели в пределах нормы. При динамическом наблюдении за 3 нед лечения показатели красной и белой крови нормализовались.
В анализе мочи регистрировалась протеинурия (бело.
Евстахиев клапан в правом предсердии чем грозит
Малые аномалии развития сердца (МАРС) анатомические изменения архитектоники сердца и магистральных сосудов, причиной возникновения которых является наследственно детерминированная соединительнотканная дисплазия сердца 4. МАРС в ряде случаев являются основой кардиоваскулярной патологии у детей, вместе с тем, некоторые исследователи считают их вариантами нормы или пограничными состояниями. Однако МАРС могут с годами сами становиться причиной развития самых разнообразных осложнений или усугублять другие патологические состояния или заболевания [6]. Превышение установленного порогового уровня сердечной стигматизации у здоровых детей (более 3 малых аномалий развития сердца) свидетельствует о возможном неблагополучии как в отношении факторов, влияющих на формирование здоровья, так и показателей, характеризующих его [2]. Частота выявления их при эхокардиографическом исследовании (ЭхоКГ) среди детей и подростков колеблется от 39 до 68,9 % [2, 6].
Цель исследования. Выявить распространенность и структуру МАРС у детей и подростков по данным ЭхоКГ.
Материал и методы исследования. Были проанализированы результаты 3552 ЭхоКГ детей и подростков в возрасте от 1 года до 16 лет, проведенных в отделении ультразвуковой диагностики клиники Рост ГМУ в период с 2009 по 2013 гг.
Результаты исследования и их обсуждение. В соответствие с классификацией [2] были выявлены МАРС в следующих группах: аномалий предсердий и межпредсердной перегородки, аорты, левого желудочка и митрального клапана.
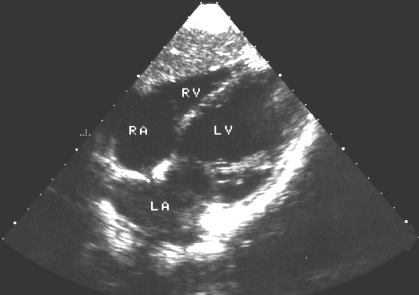
1.Аномалии предсердий и межпредсердной перегородки: увеличенная заслонка нижней полой вены более 1 см, открытое овальное окно (рис.1), небольшая аневризма межпредсердной перегородки (рис.2).
Рис.1. Ультразвуковая томограмма сердца. Апикальная четырехкамерная позиция. Открытое овальное окно. RA – правое предсердия, RV – правый желудочек, LA – левое предсердие, LV – левый желудочек.
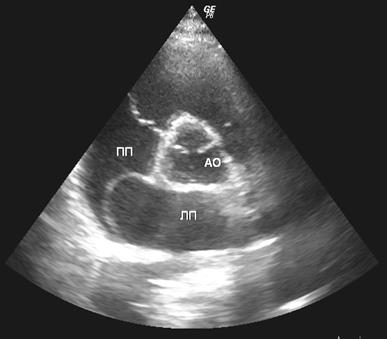
Рис.2. Ультразвуковая томограмма сердца. Парастернальная позиция по короткой оси левого желудочка на уровне аортального клапана. Аневризма межпредсердной перегородки. АО – восходящая аорта, ЛП – левое предсердие, ПП – правое предсердие.
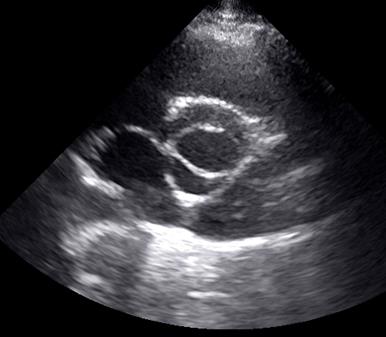
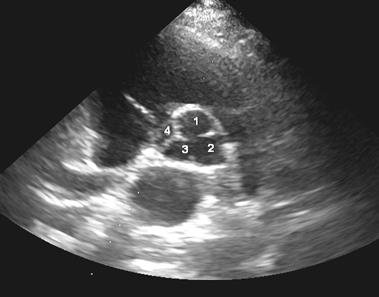
2.Аномалии аорты: дилатация синусов Вальсальвы, клапан аорты с двумя (рис.3) или четырьмя заслонками (рис.4), асимметрия заслонок клапана аорты, пролабирование заслонок клапана аорты.
Рис.3. Ультразвуковая томограмма сердца. Парастернальная позиция по короткой оси левого желудочка на уровне аортального клапана. Двустворчатый аортальный клапан.
Рис.4. Ультразвуковая томограмма сердца. Парастернальная позиция по короткой оси левого желудочка на уровне аортального клапана. Четырехстворчатый (1-4) аортальный клапан.
3.Аномалии левого желудочка: деформация выносящего тракта желудочка с систолическим валиком в верхней трети межжелудочковой перегородки, разнонаправленные трабекулы в полости левого желудочка (рис.5), небольшая аневризма межжелудочковой перегородки.
Рис.5. Ультразвуковая томограмма сердца. Парастернальная позиция по короткой оси левого желудочка на уровне митрального клапана. Малая аномалия развития – дополнительная хорда в полости левого желудочка. RV – правый желудочек, LV – левый желудочек.
4.Аномалии митрального клапана: пролабирование митрального клапана (рис.6), эктопия крепление сухожильных хорд створок клапана, аномальное расположение оснований сосочковых мышц.
Рис. 6. Пролапс митрального и трехстворчатого клапанов. Апикальная четырехкамерная позиция.
МАЛЫЕ АНОМАЛИИ РАЗВИТИЯ СЕРДЦА
К малым аномалиям развития сердца (МАРС) следует относить анатомические изменения архитектоники сердца и магистральных сосудов не приводящие к грубым нарушениям функции сердечно-сосудистой системы. Этиологической причиной малых аномалий развития сердца, является наследственно детерминированная соединительнотканная дисплазия, имеющая различные клинические проявления, зависящие от степени пенетрантности гена. Ряд малых аномалий могут иметь дизэмбриогенетический характер. Не исключается воздействие различных экологических факторов: физическое, химическое воздействие, нарушение микроэлементного гомеостаза, влияние геопатогенных зон.
К малым аномалиям сердечно-сосудистой системы, с высокой генетической предрасположенностью, относятся :
Для последних характерен аутосомно-доминантный тип наследования.
МАРС могут исчезать в процессе онтогенетического развития. К ним относятся:
Последний после периода новорожденности обычно значительно уменьшается по длине и претерпевает обратное развитие. Так же нестабильный характер имеет синдром пролабирования митрального и трикуспидального клапанов.
Для избежания субъективизма и последующей гипердиагностики МАРС, необходима их объективизация, посредством количественной оценки. В кардиологической практике количественная оценка широко применяется при исследовании глубины пролабирования митрального клапана. Также количественный подход применяется при определении длины удлиненного Евстахиева клапана, дилатации магистральных сосудов, атриовентрикулярных отверстий, числа дополнительных трабекул.
Когда идет речь об отнесении какого-либо структурного дефекта в сердце к МАРС, необходимо помнить, что принцип оценки по функциональной значимости является условным. Двухстворчатый аортальный клапан обычно не приводит к нарушению аортального кровотока, однако именно при этой аномалии развития частота внезапной смерти выше, чем в популяции. Хорошо известно, что какая бы не была опухоль сердца: злокачественная, доброкачественная-она злокачественна по своей локализации. По этой причине рассмотрение МАРС только с точки зрения изменения структуры органа опасно и чрезвычайно вредно. С другой стороны преувеличение функциональной значимости стигмы в сердце также не оправдано. В каждом конкретном случае структурная аномалия в сердце должна быть оценена в прогностическом плане.
Открытое овальное окно
Можно отнести к малым аномалиям развития сердца, поскольку при этом состоянии шунтирование крови практически не наблюдается. В клинической оценке открытого овального окна имеет значение возрастной фактор. У новорожденных детей открытое овальное окно может сопровождать респираторный дистресс синдром, в то время как у подростков данная аномалия протекает латентно, субклинически. При первичной легочной гипертензии наличие открытого овального окна является прогностически благоприятным признаком, и продолжительность жизни таких больных больше, чем при отсутствии этой микроаномалии. В данном случае, возникающий шунт разгружает правые отделы сердца и облегчает естественное течение заболевания.
ЭхоКГ критерии
Двухмерная ЭхоКГ
Допплер-ЭхоКГ
Подклапанный аппарат атриовентрикулярных клапанов
Аномалия строения
папиллярных мышц:
одна папиллярная
мышца,
располагающаяся в
области верхушки,
запирательная
функция клапана не
нарушена.
Наиболее часто в детском возрасте встречается нарушенное распределение хорд к передней или задней створке митрального клапана.
Нарушенное распределение хорд к передней (задней) створке митрального клапана
ЭхоКГ критерии
Одномерная ЭхоКГ:
Двухмерная ЭхоКГ
Допплер-ЭхоКГ
Отсутствие значимого градиента давления между левым предсердием и левым желудочком, а также левым желудочком и аортой.
Эктопическое крепление сухожильных нитей
(например, к межжелудочковой перегородке или задней стенке левого желудочка) встречается значительно реже. Аналогичные изменения могут обнаруживаться со стороны трикуспидального клапана.
Пролапс митрального клапана
Среди ультразвуковых методов диагностики первичного пролапса митрального клапана предпочтение отдается двухмерной эхокардиографии, так как при одномерной отмечается большое количество ложноположительных и ложноотрицательных результатов. При двухмерной эхокардиографии необходимо измерять площадь атриовентрикулярного клапана и окружность атриовентрикулярного кольца, которые у детей с пролапсом митрального клапана достоверно больше, чем у здоровых. Иногда удается выявить нарушение архитектоники створок, удлинение, нетипичное крепление и неправильное распределение хорд. Конечный диастолический диаметр левого желудочка у детей с первичным пролапсом митрального клапана уменьшен: у одной трети соответствует 5-й и у половины 25-й процентили. Сочетание уменьшенной полости левого желудочка с увеличением площади митрального клапана способствует возникновению клапанно-желудочковой диспропорции, которая является одним из патогенетических аспектов пролабирования створок.
Пролапс трикуспидального клапана
Редко встречается в изолированном виде и обычно сочетается с пролабированием митральных створок. Частота этого феномена намного выше чем предполагалось. Это связано с тем, что в эру одномерной эхокардиографии выявляемость пролапса трикуспидального клапана была очень низкой и недостоверной.
Аневризма межпредсердной перегородки
ЭхоКГ критерии
Двухмерная ЭхоКГ
Аневризматическое
выпячивание
межпредсердной
перегородки в
сторону правого
предсердия в области
овального окна.
Аневризматическое
выпячивание
межпредсердной
перегородки в сторону
правого предсердия в
области овального
окна.
Евстахиев клапан
Евстахиевая заслонка (заслонка нижней полой вены-valvula venae cavae inferioris) располагается на уровне передней арки нижней полой вены и, обычно после периода новорожденности не превышает в длину одного сантиметра или полностью рудиментируется. Клапан представляет собой складку эндокарда шириной в среднем до 1 см. У зародыша заслонка направляет струю крови из вены к овальному отверстию. После рождения при отсутствии сообщения между предсердиями эта функция заслонки теряет свое значение. По данным секционного материала Евстахиев клапан обнаруживается у 86% детей.
При популяционных исследованиях с использованием эхокардиографии, необычно длинный Евстахиев клапан (более 1 см) определяется у 0,20% населения, и рассматривается как стигма (рис.161). По нашим данным эта малая аномалия предрасполагает к суправентрикулярным аритмиям, верятно рефлекторно вследствие раздражения пейсмекерных образований предсердия.
Увеличенная
Евстахиева заслонка
нижней полой вены.
Двухмерная ЭхоКГ:
Визуализация клапаноподобной структуры в правом предсердии в области впадения нижней полой вены.
Дополнительные трабекулы в полости левого желудочка
ЭхоКГ критерии
Двухмерная ЭхоКГ
Функционально узкая аорта
ЭхоКГ критерии:
В большинстве случаев у детей с функционально узкой аортой выявлено повышение мышечной массы левого желудочка, о чем свидетельствовали значения диастолической толщины задней стенки левого желудочка и межжелудочковой перегородки, соответствующие 90-97 процентили. Утолщение межжелудочковой перегородки отмечалось у 35,1% мальчиков и 34,1% девочек, а задней стенки левого желудочка у 80,7% мальчиков и 88,6% девочек. Отмечено сочетание функционально узкой аорты с другими аномалиями сердца-дисфункцией митрального клапана (25,7%), пролапсом митрального клапана (8,9%), дополнительными трабекулами в полости левого желудочка (10,8%).
Дети с погранично низкими значениями диаметра аорты имеют предрасположенность к возникновению суправентрикулярных и желудочковых аритмий, а также недостаточную работоспособность и толерантность к физическим нагрузкам.
Дилатация корня аорты и синусов Вальсальвы
Является индикатором дисплазии соединительной ткани и наблюдается при синдромах Марфана, Элерса-Данлоса и других наследственных соединительнотканных заболеваниях. Однако,эти МАРС могут наблюдаться в изолированном виде без внешних проявлений заболевания (идиопатическая дилатация корня аорты). При выявлении дилатированного корня аорты (90 и более процентиль кривой распределения) необходимо исключить постстенотическую дилатацию, аортоартериит, артериальную гипертензию и другие заболевания. Дети с широкой аортой без признаков соединительнотканного заболевания часто имеют, как внешние малые аномалии развития (аналогичные первичному пролапсу митрального клапана), так и другие МАРС (дополнительная трабекула левого желудочка, дилатация ствола легочной артерии, эктазия митрального кольца). При аускультации выслушивается акцент II тона, может определяться шум волчка на сосудах шеи. Вероятно, идиопатическая дилатация корня аорты является проявлением нарушения диспропорционального онтогенетического развития у детей с наследственно обусловленной предрасположенностью к слабости соединительной ткани.
Идиопатическое расширение легочной артерии
Характеризуется расширением ствола при отсутствии порока сердца и патологии легких. Дилатация ствола легочной артерии происходит на фоне наследственно обусловленной патологии соединительной ткани, что подтверждается одновременным обнаружением других маркеров соединительнотканной дисплазии сердца и частым выявлением расширения при наследственно детерминированных синдромах, например при синдроме Марфана. При аускультации может определяться систолический шум средней интенсивности на основании сердца, уменьшающийся при вертикальном положении. При идиопатическом расширении легочной артерии необходимо динамичное наблюдение и обследование.
Чем опасна удлиненная евстахиевая заслонка?
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Опыт работы в лечебно-диагностическом центре «Арт-Мед» позволяет разделить пациентов, которые приходят на эхокардиографию, на определенные группы, в зависимости от причин их обращения.
Первую категорию составят беременные женщины, поскольку эхокардиографическое исследование считается обязательным и входит в план обследования.
Вторую, многочисленную категорию, составят люди молодого возраста с кардиалгиями.
Третью группу составят больные с хронической патологией сердца, нуждающиеся в динамическом наблюдении (врожденные и приобретенные пороки и т.д.) или в уточнении диагноза.
Четвертую группу составят больные с впервые возникшими жалобами на боли в области сердца, одышку, проявления сердечной недостаточности. Данная группа пациентов наиболее серьезная, т.к.
среди них можно встретить «острую» патологию (аневризма грудной восходящей аорты, тромбоэмболия в систему легочной артерии, развитее аневризмы левого желудочка и т.д.). Пятую группу составят пациенты с шумом в области сердца.
Попытаемся объяснить возможности эхокардиографии в диагностике патологии сердца и дифференциальной диагностике. Для этого попытаемся проанализировать вышеперечисленные группы пациентов.
Эхокардиография при беременности
Во время беременности у здоровой женщины можно наблюдать незначительные изменения размеров полостей сердца и изменения со стороны гемодинамики по сравнению с исходными. Систолическое давление в легочной артерии может увеличивается до 40 мм рт. ст.
На 2 — 3 мм может увеличиться диаметр корня аорты,левого предсердия и левого желудочка. Частота сердечных сокращений возрастает на 25 — 30 %, уже в первом триместре беременности увеличивается минутный объем кровотока и ударный объем. Артериальное давление не изменяется.
Увеличивается степень клапанной регургитации (на трикуспидальном клапане и клапане легочно артерии до 3 степени, на митральном клапане до 2 степени). В редких случаях можно наблюдать реакцию листков перикарда — наличие незначительного количества жидкости в перикарде.
Жидкость исчезает спустя 1 — 3 месяца после родов в отсутствии лечения.
Одной из особенностей у беременных женщин является динамический стеноз нижней полой вены.
Данное явление может сопровождаться аускультативной картиной — шумом при аускультации и синкопальными состояниями, возникающими при перемене положения тела в пространстве.
В ряде случаев на фоне беременности открывается овальное окно и отмечается небольшое шунтирование крови слева направо. Все вышеперечисленные изменения как правило ичезают после родов. Динамику лучше проводить через 1 — 3 месяца после родов.
Причины кардиалгии — болей, симулирующих боли в сердце
Наиболее частой причиной кардиалгии у людей молодого возраста является переутомление, стресс и гипокалиемия (недостаток калия).
Иногда у данной категории больных можно наблюдать незначительное пролабирование онования передней створки митрального клапана в полость левого предсердия, что является вариантом норы для молодых людей и детей (рис. 1).
Данный пролапс нельзя путать с патологическим, когда имеются органические изменения створок (например, при миксоматозной дегенерации — рис. 2).
Рис. 1. Незначительный пролапс передней створки митрального клапана (вариант нормы).
Рис. 2. Миксоматозная дегенерация створок митрального клапана.
Провести дифференциальный диагноз можно на приеме у кардиолога или терапевта. Как правило, после беседы с пациентом и аускультации доктор назначает ЭКГ и ЭхоКГ исследование. При подозрении на нарушение электролитного баланса рекомендуется биохимическое исследование крови.
У больных с хронической патологией сердца, например, ревматическим пороком сердца, врожденным пороком сердца, протезированным клапаном сердца и т.д. эхокардиография проводится 1 раз в год или 1 раз в 2 года.
Эхокардиография позволяет оценить состояние и структуру клапанов сердца, степень порока, состояние протеза, систолическую функцию желудочков сердца, состояние стенок аорты, степень легочной гипертензии, состояние плевральных полостей и перикарда и т.д. (рис. 3 и 4).
В ряде случаев больные обращаются с целью уточнения степени или характера порока.
Рис. 3. Ревматический порок сердца — стеноз митрального клапана.
Рис. 4. Врожденный порок сердца — дефект межпредсердной перегородки. Дилатация правых камер сердца, шунтирование крови через дефект в режиме цветового допплера.
Пациенты с впервые возникшими жалобами на боли в области сердца и с клиническими проявлениями сердечной недостаточности являются наиболее серьезной группой обследованных и зачастую требуют более детального обследования (например — коронароангиографию) или консультацию кардиохирурга или сосудистого хирурга (рис. 5).
Рис. 5. Аневризма восходящего отдела аорты.
Причины развития сердечной недостаточности разнообразные. Методика эхокардиографии позволяет приблизить верификацию диагноза, а в ряде случаев и установить точный диагноз.
Шумы в области сердца
Одна из наиболее частых причин направления на эхокардиографическое исследование — наличие шума в области сердца.
В «доэхокардиографическую» эру было в ряде случаев сложно отличить нормальный функциональный шум от патологического.
Попытаемся перечислить причины наиболее часто встречающихся нормальных функциональных шумов в области сердца. Особенно хорошо они прослушиваются у детей, подростков и худых людей.
Дополнительная хорда в полостях желудочков (фальш — хорда или ложная хорда) — нитчатая структура, распологающаяся в полости левого или правого желудочка.
Располагается между межжелудочковой перегородкой (МЖП) и стенкой сердца, головкой папиллярной мышцы и стенкой и т.д. Основание дополнительной хорды не утолщается в систолу.
Число хорд может быть различным. Встречается в 98% случаев (рис. 6).
Рис. 6. Малая аномалия развития — дополнительная хорда в полости левого желудочка (вариант нормы).
Дополнительная мышечная трабекула в полости желудочков (фальш — трабекула) — мышечная структура, распологающаяся в полости левого или правого желудочка. Часто расположена параллельно межжелудочковой перегородке или поперечно между стенками желудочка. Основание дополнительной мышечной трабекулы утолщается в систолу. Встречается в 85% случаев (рис. 7).
Рис. 7. Малая аномалия развития — дополнительная мышечная трабекула в полости левого желудочка и две дополнительные хорды (вариант нормы).
Евстахиев клапан нижней полой вены — рудиментарный клапан. Не играет никакой роли в гемодинамике сердца. Встречается в 20% случаев.
Сеть Хиари — рудимент, продолжение Евстахиева клапана нижней полой вены в коронарный синус. Встречается в 2% случаев.
Аневризма межпредсердной перегородки
Аневризма межпредсердной перегородки (МПП) — врожденная особенность развития межпредсердной перегородки. Мембрана овальной ямки удлинена и выбухает в сторону (рис. 8). Существует ряд типов аневризмы межпредсердной перегородки:
Рис. 8. Аневризма межпредсердной перегородки.
Рис. 9. Аневризма межпредсердной перегородки — тип R.
В случае, если аневризма имеет очень большие размеры и значительно вдается в полость предсердия, она может расцениваться как врожденный порок межпредсердной перегородки (крайне редко встречается). При наличии дефекта межпредсердной перегородки в области аневризмы межпредсердной перегородки ситуация расценивается как врожденный порок сердца.
Аневризма мембранозной части межжелудочковой перегородки — встречается редко (0,5 — 1 % случаев).
Добавочные головки папиллярных мышц — число их может быть различно и по данным анатомов может достигать 16, размеры головок также различные. Чем больше папиллярных мышц в полости желудочка, тем больше хорд от них отходит.
Незаращение овального окна — вариант развития мембраны овальной ямки, встречается у 25 % людей. Клапан мембраны овальной ямки прикрывает овальное окно. Шунтирование крови отсутствует но может возникнуть в ряде ситуаций (например, при резком повышении давления в полости левого или правого предсердий).
Открытое овальное окно — встречается реже (1 — 2 % людей). В настоящее время в педиатрической практике происходит гипердиагностика открытого овального окна.
Шунтирование крови при этом происходит слева направо, носит непостоянный характер, объем шунта небольшой. Отсутствует легочная гипертензия и дилатация правых камер.
Противопоказания для дайвинга
Единственным противопоказанием для людей с открытым овальным окном является занятие дайвингом (подводным плаванием). В любом случае — собираететесь ли Вы в Египет или Таиланд и хотите окунуться в чарующий мир морского дна, или проводите время в городе, не поленитесь сходить к кардиологу и пройдите эхокардиографическе исследование. Это позволит избежать трагических последствий.
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Здоровье человека
К группе МАРС относят:
МАРС — это не только название красной планеты, таким образом обозначается заболевание сердца, которым страдают дети. Эта проблема мало где описана в доступной форме, хотя вопросов вызывает немало. Будем разбираться и искать ответы на распространённые вопросы, которые возникают у родителей.
Описание и характеристика
Когда ставится диагноз МАРС у ребёнка, первый вопрос, который тревожит родителей — что это. Аббревиатура расшифровывается как малые аномалии развития сердца. Под этим непонятным названием скрываются аномалии развития соединительной ткани сердечной мышцы.
Соединительная ткань составляет каркас сердца, его клапаны и стенки в сосудах. За счёт присутствия этой ткани сердечная мышца является эластичной и прочной. Под малыми аномальными явлениями подразумеваются анатомические изменения, которые имеют врождённый характер.
При этом диагнозе соединительная ткань может быть слабой, формироваться в отличных от нормы местах, её количество может быть недостаточным или, наоборот, избыточным. Выявляется подобная проблема до достижения ребёнком трёхлетнего возраста. Недуг не прогрессирует и имеет склонность исчезать по мере роста ребёнка.
Что провоцирует
Специалисты выявили ряд причин, по которым может возникать заболевание МАРС у детей.
Причин много, они разнообразные и непохожие друг на друга. Но объединяет их одно обстоятельство — все они могут вызывать развитие МАРС.
Распространённые виды
МАРС может проявляться в различном виде. Есть много разновидностей этого заболевания. Мы рассмотрим наиболее распространённые варианты:
Характерные симптомы
Малые аномалии развития сердца у детей редко когда проявляются, в большинстве случаев ребёнок не имеет жалоб. В редких случаях родители могут замечать следующую симптоматику:
В подавляющем большинстве случаев МАРС сочетается с другими заболеваниями, связанными с развитием соединительной ткани.
Проблемы могут быть связаны с органами зрения, скелетным корпусом, кожей, почками и желчным пузырём. Ввиду такого обстоятельства симптоматика имеет системный характер, другими словами, затрагивает весь организм.
Такие проявления могут быть незначительными и существенными, каждый случай индивидуален.
Тест: А что вы знаете о человеческой крови?
Сочетаний МАРС с другими заболеваниями масса, перечислить их все мы не сможем. Лишь постараемся выделить основные и наиболее распространённые.
Диагностика и исследования
В международной классификации болезней для малых аномалий развития сердца выделен отдельный код. Для МАРС у детей отведён код по МКБ 10 Q20.9. Чтобы подтвердить диагноз МАРС у ребёнка, в кардиологии используется много методов:
Последний метод является простым и результативным, поэтому всё больше специалистов выбирают именно его.
Лечение МАРС
Есть немало способов лечения малых аномалий развития сердца. Все эти методы имеют условное разделение на три группы:
Возможные осложнения
Хотя в большинстве случаев МАРС проходит с возрастом, но всё же в отдельных ситуациях он может быть причиной образования ряда осложнений:
Такие осложнения по большей части характерны для ПМК и ДХПЛЖ.
Прогноз при заболевании
Если МАРС протекает без каких-либо жалоб на состояние и не вызывает развития нарушений в работе сердца, то заболевание можно считать индивидуальной особенностью организма. В этом случае человек может никогда не узнать о своём заболевании, или выявить его случайно. На качество и продолжительность жизни МАРС не окажет ни малейшего влияния.
При наличии хоть одного симптома из описанных выше заболевание нуждается в диагностике, лечении и контроле. Игнорировать проблему исходя из того, что она не является опасной, нельзя. Никто не может сказать, каким образом МАРС будет развиваться, и как организм отреагирует на эти изменения.
Возможна ли профилактика?
Можно снизить вероятность развития МАРС и даже вообще исключить его появление. Для этого нужно придерживаться несложных мер профилактики:
Будет ли у ребёнка обнаружен МАРС и как он повлияет на его организм — всё это зависит от родителей, их сознательности и внимательности. Своевременное выявление проблемы, постоянное наблюдение, лечение и профилактика — основа здоровья вашего малыша.
>Евстахиева заслонка: что это такое и для чего она нужна
Что это такое и где находится?
В настоящее время до конца не решен вопрос, какие малые аномалии развития кардиоваскулярной системы считаются патологией, а какие – возрастными анатомо-физиологическими особенностями детского организма. Исключение составляет только наличие анатомических отклонений сердца у взрослых.
Кровоток в утробе матери имеет существенные отличия. На протяжении первых четырех недель развития происходит основная закладка структур сердца.
Формируется мышечная сердечная ткань (миокард) и соединительная – каркас магистральных коронарных сосудов, артерий и вен. До момента рождения легкие не участвуют в процессе насыщения маленького организма кислородом и удаления углекислоты.
Эту роль выполняет плацентарное кровообращение посредством доставки оксигенированной крови через пупочные сосуды.
Евстахиев клапан (ЕК) представляет собой заслонку в просвете нижней полой вены, которая необходима для кровообращения у плода (направления крови из правого предсердия в левое через открытое овальное отверстие). Расположение ЕК показано на фото ниже:
За счет этих коммуникаций осуществляется доставка и отток крови в объеме, необходимом для маленького организма. После родов и удаления плаценты изменяются сосудистые пути.
С первым криком ребенка при рождении легкие расправляются и под увеличенным внутрисердечным давлением плодные отверстия в сердце начинают закрываться.
В случае сохранения складки из ткани эндокарда (внутренней оболочки) у взрослого говорят об удлиненной евстахиевой заслонке.
Удлиненная евстахиева заслонка
Евстахиева заслонка в сердце определяется на уровне арки нижней полой вены, по ее передней поверхности. В среднем после рождения и достижением ребенком возраста 5-7 лет ее размер не превышает 10 миллиметров, или же соединительнотканная структура полностью отсутствует. Анатомически представляет собой:
Чем опасно наличие заслонки у взрослых?
Все малые аномалии развития кардиоваскулярной системы не вызывают значительных нарушений гемодинамики (кровообращения). Увеличение частоты выявления такой патологии связано с распространением УЗИ диагностики для детей и взрослых, что позволяет на ранних этапах выявить отклонение.
Согласно последним исследованиям в кардиологии и общей терапии, удлинение евстахиевой заслонки на более чем 1 сантиметр определяют у 0,25%-0,50% населения. В большинстве случаев происходит это на фоне состояния полного здоровья.
Наличие подобного клапана повышает риск развития некоторых осложнений, поскольку в правом предсердии располагается главный источник электрических импульсов сердечной сократимости.
Рефлекторное раздражение пейсмекерных (вводящих ритм) клеток может вызывать аритмию таких типов:
Клиническая симптоматика возникает только при сочетании нескольких аномалий развития, или на фоне сопутствующей патологии, ухудшающей состояние. Характерны симптомы: одышка с затрудненным дыханием при нагрузке, слабость и бледность лица, синюшность вокруг носогубного треугольника, отеки.
Выводы
Удлиненная евстахиева заслонка у взрослых расценивается как малый признак аномалии развития сердца. При его выявлении на УЗИ в любом возрасте врач оценивает общее состояние пациента. Без симптомов нарушения гемодинамики лечение не требуется. Достаточно соблюдать график ежегодных профилактических осмотров, обследования и ультразвуковой диагностики у кардиолога.
Евстахиев клапан в правом предсердии узи
На протяжении беременности в сердце у плода происходит ряд физиологических изменений, необходимых для кровообращения в утробе матери без участия легких.
Анатомическим приспособлением к таким условиям считается овальное «окно» между предсердиями и евстахиев клапан в нижней полой вене. Со временем такие образования закрываются.
Если у ребенка остается часть заслонки, говорят о наличии малой аномалии развития, которая во взрослом возрасте может вызывать нарушения кровообращения. Для выявления патологии следует обратиться к детскому кардиологу.
Технические требования и условные обозначения
Представленные записи аускультации сердца рекомендуется слушать ТОЛЬКО через хорошие наушники, тут подробнее об этом. Тут написано, как интерпретировать представленные спектральные фонокардиограммы.
В колонке справа представлен архив сайта и оглавление. Представленные материалы могут быть полезными изучающим искусство аускультации сердца.
По вопросам, которые не относятся к сути представленных материалов, можно писать по адресу ivshpakiv УЛИТКА gmail.com
Сокращения:Т1 — первый тон сердцаТ2 — второй тон сердцаТ3 — третий тон сердца
Т4 — четвертый тон сердца. Пятый и далее автору не известен.
Что происходит при наличии сосудистой сети Киари
В процессе диагностики в правом предсердии обнаружили сеть Киари или Хиари, хотя я не ощущал никак особых симптомов. Что она представляет собой, опасна ли для здоровья, будут ли проблемы в будущем и что нужно делать?

Здравствуйте. Сеть Киари в правом предсердии представляет собой непатологическую подвижную тонкую сетчатую структуру в правом предсердии, которую видно на мониторе УЗИ из любой позиции там, где в предсердие впадает нижняя полая вена.
То есть сетка состоит из остатков эмбрионального клапана коронарного синуса, что прикрепляются к евстахиеву клапану нижней полой вены с одной стороны, а с другой – к частям правого предсердия (ПП).
Она обнаруживается действительно случайно при диагностике у 1-2% населения.
Если быть точнее, то эта врожденная аномальная структура сердца в виде сетевидной пластинки с дырками – перегородка предсердия – начинается у заслонки венечного синуса (Тебезиева клапана) и заслонки нижней полой вены (Евстахиева клапана). Она в некоторой степени может перегораживать предсердие.
Пластинка может иметь разные положения, но в основном прикрепляется чуть кпереди от Ловерова (межвенозного) бугорка. Сеть Хиари появляется в связи с недостаточной редукцией правого (реже – левого) синусового клапана или из-за ложной перегородки. Удлиненную заслонку Евстахиева клапана и Сеть Хиари считают вариантом нормы.
Диагностика
Чтобы визуализировать сеть Chiari применяют ЭхоКГ-диагностику. При этом используются позиции, в которых одновременно исследуют ПП: апикальную 4КП, модифицированную парастернальную биккавальную позицию и короткую ось на уровне Аок со стороны левого парастернального доступа, но это могут выполнять только профессиональные диагностики.
Также используют позиции субкостальные: 4КП, короткую ось на уровне Аок и длинную ось полой вены снизу. Чтобы оценить место прикрепления сети Хиари, необходимо провести полипозиционное исследование и включить промежуточные позиции прикрепления на евстахиевом и клапане коронарного синуса.
В других возможных местах в одной плоскости сеть может не визуализироваться. Тогда применяют 3D-ЭхоКГ-исследование. Лучше всего оценку устья коронарного синуса удается датчиком из пищевода, а точнее – из его средних отделов.
Клиника
Сеть Хиари высоко сопряжена с ООО (открытым овальным окном). У 82% пациентов, которым назначают эндоваскулярное закрытие ООО, имеется сеть Хиари или евстахиев клапан.
Если имеется ООО, то чаще выявляют право-левое шунтирование крови, чем при отсутствии сети.
Сеть, как и клапан, препятствуют закрытию открытого овального окна, тогда может развиться аневризма межпредсердной перегородки (МПП) и парадоксальная эмболия.
В этом случае поток крови будет направляться из нижней полой вены к МПП. При аневризме МПП происходит выпячивание стенки между предсердиями S-образно (изгибаться в обе стороны), вправо или влево. Симптомы при этом не проявляются, а патология через некоторое время исчезает.
В некоторых случаях при наличии сети Chiari у пациентов возникают приступы мигрени. Если у больных развивается инфекционный эндокардит, то болезнь может поразить ткани сети. Они могут иметь вид опухолевого образования, тогда не исключен ложный диагноз.
Если рассматривать сети Хиари, как тромбоэмболические осложнения, то их роль двояка:
Были случаи отрыва фрагментов ткани сети и миграции их в легкие.
Аритмогенность сетей Хиари может происходить из-за тесной взаимосвязи САС (симпатико-адреналовой системы) с венозным синусом на некоторых участках, а также в связи с наличием миокардиальных волокон в ретикулярной структуре тканей сети.
Исследованиями не подтвержден факт препятствия сетей Chiari кровотоку. Но были случаи, что из-за этих предсердных образований было сложно провести катетеры в коронарный синус или правые отделы сердца.
Клиническое значение
Изолированно сеть встречается реже, чем в сочетании с коммуникациями между предсердиями. Если ее выявляют, то это дает основание искать ООО и АМПП (аневризмы межпредсердной перегородки) полипозиционным исследованием, используя стандартные и промежуточные позиции.
Клинически из-за патологии возможны тромбоэмболические осложнения (тромб in situ), инфекционный эндокардит, трудности с дифференциальной диагностикой из-за различных внутрипредсердных образований (опухолей, тромбов, кист), возможны сложности при проведении эндоваскулярных доступов к сердцу.
На эхокардиографии показана сеть Хиари(CN):

На видео в этой статье можно увидеть работу сердца с наличием сети Хиари.
Вывод
Сама сеть клинически не имеет существенного значения, но ее часто ассоциируют с патологиями: открытым овальным окном (ООО), внутрипредсердным тромбозом или предсердными аритмиями. Осложняется сетка Хиари тромбозом с последующей тромбоэмболией, но лечения не назначают, поскольку она преграждает продвижение тромба, является рудиментом заслонки коронарного синуса.
Практического значения сетевидная пластинка с дырками не имеет. Но проводят для ее обнаружения необычный диагноз, что не исключает врачебной ошибки. Поэтому важно проводить тщательную эхокардиографию, что при сердечно-сосудистых вмешательствах облегчит преодолеть трудности при проведении катетеризации в коронарный синус или правые отделы сердца.
Клиническое значение малых аномалий развития сердца у детей
В последние годы большое внимание уделяется дисплазии соединительной ткани (ДСТ) у детей. Под ДСТ понимают врожденную аномалию соединительно-тканной структуры различных органов и систем, в основе которой лежит снижение содержания отдельных видов коллагена и/или нарушение их соотношения, приводящее к снижению прочности соединительной ткани [12, 13, 24, 26].
В развитии ДСТ принимают участие эндогенные (хромосомные и генетические дефекты) и экзогенные (неблагоприятная экологическая обстановка, неадекватное питание, стрессы) факторы [12, 30, 43].
Особенность морфогенеза соединительной ткани заключается в том, что она участвует в формировании каркаса сердца практически на всех этапах онтогенеза, следовательно, влияние любого повреждающего фактора может привести к развитию ДСТ сердца [15].
в классификации заболеваний сердечно-сосудистой системы Нью-Йоркской ассоциации кардиологов, а также в Омске, на симпозиуме, посвященном проблеме дисплазии соединительной ткани, был впервые выделен синдром ДСТ сердца, сопровождающий как дифференцированные, так и недифференцированные ДСТ. При синдроме ДСТ сердца в патологический процесс вовлекается его соединительно-тканный каркас — сердечные клапаны (атриовентрикулярные, полулунные, евстахиев клапан), подклапанный аппарат, перегородки сердца и магистральные сосуды.
В клинической практике, когда речь идет о морфологической основе изменений сердечно-сосудистой системы без гемодинамических нарушений, Ю. М. Белозеровым (1993) и С. Ф.
Гнусаевым (1995) вместо термина «ДСТ сердца» был предложен другой — «малые аномалии развития сердца» (МАРС) [3, 8].
Согласно определению этих авторов, МАРС считаются анатомические изменения архитектоники сердца и магистральных сосудов, не приводящие к грубым нарушениям функций сердечно-сосудистой системы [9].
Классификация МАРС по С. Ф. Гнусаеву, 2001 (с изменениями)
До сих пор нет единого мнения о клиническом значении МАРС, многие из которых имеют нестабильный характер, связанный с ростом ребенка. Так, возможно обратное развитие увеличенного евстахиева клапана, пролабирующих гребенчатых мышц в правом предсердии, пролапса митрального клапана (ПМК), закрытие открытого овального окна, нормализация длины хорд митрального клапана и диаметра магистральных сосудов. В ряде случаев МАРС изменяются не только в качественном, но и в количественном отношении [3]. Превышение установленного порогового уровня сердечной стигматизации у здоровых детей (более 3 МАРС), по мнению С. Ф. Гнусаева (1995), свидетельствует о возможном неблагополучии как в отношении факторов, влияющих на формирование здоровья, так и показателей, характеризующих его [8].
Учитывая, что МАРС являются вариантом висцеральных ДСТ, дети, как правило, имеют выраженный полиморфизм клинико-морфологических нарушений, зависящий от степени ДСТ и вовлечения в патологический процесс других органов и систем.
Выявлена ассоциативная связь между числом внешних фенотипических маркеров ДСТ и МАРС [12, 16, 21, 22]. При этом имеют значение не только число внешних фенотипических маркеров, но и «диагностический вес» каждого из них.
Отмечено, что дисплазии кожи и скелета наиболее часто сочетаются с МАРС [12].
Клиническая значимость патологии соединительной ткани у лиц с ДСТ подтверждается данными о высокой частоте нейровегетативных расстройств, изменений центральной нервной системы (энурез, дефекты речи, вегетососудистая дистония (ВСД)), нарушений психики [5, 12, 24].
Как правило, у таких пациентов всегда выявляется ВСД, что, вероятно, обусловлено наследуемыми (наследственными) особенностями структуры и функции лимбико-ретикулярного комплекса, определяющими аномальный характер нейровегетативных реакций [12]. Е. В. Буланкиной (2002) установлена отчетливая взаимосвязь между вегетативной дисфункцией и ДСТ [4].
При этом выраженность диспластических изменений сочеталась с тяжестью процессов дезадаптации регуляторных механизмов и снижением стрессовой устойчивости организма. Наиболее распространенными проявлениями вегетативной дисфункции являются цефалгии, вегетативные кризы, вегетовисцеральные пароксизмы, пре- и синкопальные состояния [12, 16]. Согласно данным С. Ф.
Гнусаева (1995), у лиц с ПМК выявлена недостаточность сегментарных вегетативных структур [8]. Исследования Т. М.
Домницкой (2000) позволили установить прямую зависимость между ПМК, аномально расположенными трабекулами (АРТ) и распространенностью невротических (невротические реакции, невроз навязчивых состояний, панические расстройства) и энцефалопатических (церебрастенический синдром, заикание, тики, нарушения сна, энурез, гипердинамический синдром, страхи) расстройств [10].
Нередко МАРС сопровождают такие патологические состояния, как нарушения сердечного ритма и проводимости, в том числе синдром ранней реполяризации, синдром слабости синусового узла, синдром Вольф–Паркинсон–Уайта, повышение электрической активности левого желудочка, блокада правой ножки пучка Гиса, экстрасистолия и пароксизмальная тахикардия [4, 6, 8, 34]. По данным Л. А. Балыковой и соавт. (2002), у 90% больных с нарушениями сердечного ритма с помощью эхографии были выявлены МАРС (преимущественно ПМК) [2]. Однако не все МАРС сопровождаются нарушениями сердечного ритма и (или) могут являться их причиной. К аритмогенным МАРС относятся фиброзно-мышечные аномально расположенные хорды (АРХ) и АРТ, ПМК и пролапс трикуспидального клапана (ПТК), аневризма межпредсердной перегородки, увеличенный и/или пролабирующий евстахиев клапан.
Наличие проводящих кардиомиоцитов в фиброзно-мышечных АРХ и АРТ формирует дополнительные проводящие пути, чем объясняется происхождение импульса, опережающего внутрижелудочковое проведение и вызывающего раннее возбуждение прилежащих к нему сегментов с последующей их более ранней реполяризацией [12, 15, 19, 20, 28]. Имеется гистологическое подтверждение наличия проводящих клеток в АРТ с диагонально-базальной, срединно-поперечной и продольной локализацией и в АРХ, соединяющих базальные септальные отделы и боковую стенку левого желудочка [3, 10, 33]. M. Suwa и соавт. (1986) отметили возрастание частоты желудочковых экстрасистол с увеличением толщины хорды. По мнению E. Chesler и соавт. (1983), появление желудочковых экстрасистол связано с миксоматозно измененными хордами, вызывающими механическое раздражение стенки левого желудочка [27]. Факт аритмогенности АРХ и АРТ также подтверждается исчезновением у пациентов экстрасистолии в случае их самостоятельного разрыва или оперативного рассечения либо при физической нагрузке, когда уменьшается степень их натяжения [8, 10, 12]. Довольно распространенным нарушением сердечного ритма при АРХ и АРТ является и синдром раннего возбуждения желудочков [6, 12].
Аритмии при ПМК и ПТК, по данным разных авторов, встречаются от 15 до 90% случаев [11].
Среди причин аритмий рассматриваются вегетативные дисфункции, механическая стимуляция эндокарда, дефицит внутритканевого магния, психологический стресс и миксоматозная дегенерация створок клапанов [3, 10–12, 18, 27, 29, 37, 39].
Установлена прямая корреляционная зависимость между частотой, а также степенью тяжести нарушений ритма и глубиной ПМК [1].
Ряд авторов полагают, что причиной развития аритмий при ПМК и ПТК может являться турбулентный поток, возникающий в результате регургитации через клапанное кольцо во время систолы желудочков, особенно при ПТК, когда происходит механическое раздражение зоны синусового узла [3, 8, 23]. Возможным механизмом развития желудочковых экстрасистол при ПМК большинство исследователей считают избыточное натяжение папиллярных мышц вследствие их аномальной тракции при пролабировании створок [12, 14, 25, 38].
Развитие аритмий может провоцировать пролабирующий евстахиев клапан и аневризма межпредсердной перегородки: условия для возникновения аритмий возникают в результате их холмистых движений и рефлекторного раздражения ими пейсмекерных образований в правом предсердии [42].
Согласно исследованиям О. А. Дианова (1999), нарушения сердечного ритма встречались у детей с погранично узкой аортой, у которых в 32,4% случаев регистрировалась суправентрикулярная и в 10,8% — желудочковая экстрасистолии, свидетельствующие о декомпенсации адаптации, особенно в условиях физической нагрузки [4].
По данным Ю. М. Белозерова, дети с МАРС отличаются сниженными возможностями кардиогемодинамики и демонстрируют плохую переносимость физических нагрузок [3]. По данным Н. А. Мазура, установлена связь между ПМК и синдромом внезапной смерти у взрослых. Накоплено достаточно сведений о том, что дети с МАРС относятся к группе риска по развитию инфекционного эндокардита.
Таким образом, существующие результаты исследований о том, что МАРС в ряде случаев являются основой кардиоваскулярной патологии у детей. В то же время неоправданным было бы преувеличение их роли в функциональных нарушениях сердечно-сосудистой системы. Очевидно, в каждом конкретном случае значимость структурных аномалий сердца должна рассматриваться индивидуально.
Принципы терапии детей с МАРС еще до конца не сформулированы. Однако на сегодняшний день можно предложить следующую тактику ведения детей с МАРС:
Вопрос о допуске к занятиям спортом решается индивидуально.
При наличии ПМК необходимо учитывать семейный анамнез (случаи внезапной смерти у родственников), наличие жалоб на сердцебиения, кардиалгии; синкопальные состояния; изменения на ЭКГ (нарушения сердечного ритма, синдром укороченного и удлиненного QT) являются основанием для принятия решения о противопоказании спортивных тренировок. Это касается и наличия АРХ, АРТ с синдромом раннего возбуждения желудочков, которые, являясь аритмогенными МАРС, могут спровоцировать нарушения сердечного ритма у спортсменов в условиях физического и психоэмоционального напряжения.
Медикаментозное лечение включает применение:
В настоящее время терапия препаратами магния при МАРС приближается к патогенетической. Это обусловлено тем, что магний входит в состав основного вещества соединительной ткани и необходим для правильного формирования волокон коллагена.
В условиях магниевой недостаточности нарушается способность фибробластов продуцировать коллаген [29, 31].
Кроме того, магний оказывает мембраностабилизирующее действие, удерживает калий внутри клетки, препятствует симпатикотоническим влияниям, что делает возможным его применение для лечения нарушений сердечного ритма [40, 41].
В работах О. Б. Степуры (1999), О. Д. Остроумовой и соавт. (2004) имеются сведения о достоверном уменьшении степени ПМК, симптомов ВСД, количества желудочковых экстрасистол на фоне терапии препаратами магния [17, 18].
Целесообразным может быть признано назначение следующих препаратов:
Магнерота, содержащего соль магния и оротовую кислоту. Последняя не только усиливает реабсорбцию Mg в кишечнике, но и обладает самостоятельным метаболическим действием. Детям назначают по 500 мг магнерота (32,8 мг магния 3 раза в день в течение 1 нед, затем 250 мг 3 раза в день в течение последующих 5 нед. Принимается препарат за 1 ч до еды).
Магне В6. Выпускается в таблетках (48 мг магния или в растворе для приема внутрь (100 мг магния). Детям с массой тела более 10 кг (старше 1 года) — 5–10 мг/кг/сутки в 2–3 приема. Детям старше 12 лет — 3–4 табл. в сут, в 2–3 приема. Продолжительность курса 6–8 нед.
Калия оротата. Детям препарат назначают из расчета 10–20 мг/кг/сут в 2–3 приема за 1 ч до еды или через 4 ч после еды. Продолжительность курса — 1 мес.
Следует проводить повторные курсы терапии этими препаратами (3–4 раза в год).
Для улучшения клеточной энергетикии миокарда применяют препараты, обладающие комплексным влиянием на метаболические процессы в организме, а также являющиеся активными антиоксидантами и мембраностабилизаторами:
Кроме указанных препаратов для улучшения метаболических процессов в соединительной ткани, миокарде и в организме в целом показано применение:
Показаны повторные курсы лечения (до 3 раз в год).
При наличии ВСД проводится комплексная длительная терапия по восстановлению баланса между симпатическим и парасимпатическим отделами вегетативной нервной системы (дифференцированная фитотерапия, вегетотропные препараты, ноотропы, вазоактивные препараты — кавинтон, вазобрал, инстенон, циннаризин и др.).
Таким образом, все вышесказанное позволяет сделать вывод, что МАРС, являясь висцеральным проявлением дисплазии соединительной ткани, составляют морфологическую основу функциональных изменений сердечной деятельности и нейровегетативных расстройств. Выбор индивидуальной программы курсового лечения способствует улучшению обменных процессов в соединительной ткани и профилактирует возможные осложнения ДСТ у детей и подростков.
По вопросам литературы обращайтесь в редакцию.
Н. А. Коровина, доктор медицинских наук, профессор А. А. Тарасова, кандидат медицинских наук, доцент Т. М. Творогова, кандидат медицинских наук, доцент Л. П. Гаврюшова, кандидат медицинских наук, доцент М. С. Дзис РМАПО, Москва