кадмий с чем реагирует
Характеристики и свойства металла кадмий
Кадмий — металл из периодической таблицы Менделеева, который находится под номером 48. Обладает уникальными свойствами, считается относительно редким. Чаще применяется при покрытии других металлов для защиты от образования ржавчины, но может использоваться и в других сферах деятельности.

История открытия
Новый химический элемент, который был назван кадмием, открыл Фридрих Штромейер в 1817 году. Известный профессор химии, фармацевт занимался инспектирование аптек. В процессе прокаливании разных образцов карбоната натрия он отметил, что из некоторых представителей получается коричневый или оранжево-желтый оксид. При детальном изучении профессор обнаружил что он не содержит свинца и железа. Появление такого окраса он объяснил присутствием неизвестного элемента.
Практически в то же время, независимо от работ Штромейера, изучая соединения на основе цинка кадмий выделили К. Херман и И. Ролофф.
Запасы и месторождения
Кадмий — редкий рассеянный элемент. Из него образуется ограниченное число соединений. Основным минералом, в котором содержится значительное количество этого элемента, является гринокит. Из него не образуются естественные скопления. Чаще данный минерал встречается в виде землянистой корки, которой покрываются цинковые минералы.
В больших количествах его добывают в зонах сульфидных месторождений. Самые большие из них расположены в Средней Азии, Казахстане, на Южном Урале.
Редкие минералы, которые могут содержать кадмий, — кадмоселит, отавит, монтепонит.
Добыча и промышленное получение
Процесс промышленного получения кадмия из расходного сырья включает нескольких этапов:
После проведения всех этапов на выходе получается металл с чистотой 99,95%.
Свойства и характеристики
Чтобы понять, насколько важен металл для промышленности, где он может применяться, нужно изучить его свойства — физические, химические, механические.
Физические
Физические свойства кадмия:
Кадмий — мягкий, тяжелый, тягучий металл белого цвета с характерным металлическим блеском.
Металл кадмий (Фото: Instagram / zeodetoxru)
Химические
Кадмий не вступает в реакцию с бором, кремнием, углеродом. Взаимодействует с кислотами.
Механические
Где используется кадмий?
Поскольку металл может накапливаться в раковых клетках, его применяют при лечении онкологических заболеваний.
Влияние на организм
Кадмий — опасный для человека металл. Его изотопы выделяют вредные вещества, которые могут привести к ухудшению общего состояния, отравлению. Острая интоксикация организма наступает после попадания в организм 30 мг вещества. Симптомы отравления кадмием:
Если в организме присутствует постоянный повышенный уровень этого вещества, состояние будет ухудшаться постепенно.
Самый опасный вариант развития событий — хроническая интоксикация организма. Поскольку общее состояние ухудшается медленно, специфическая клиническая картина отсутствует. Человек не обращает внимание на ухудшение состояния, списывая недомогание на нехватку витаминов, переутомление, плохую экологию.
При лечении интоксикации кадмием пациент должен находиться в стационаре. Запрещено заниматься самолечением, поскольку это может привести к летальному исходу. Уровень содержания этого металла в организме определяется с помощью анализа мочи.
Чтобы вывести отравляющее вещество из желудочно-кишечного тракта, проводится промывание желудка с применением зонда. После очистки пациент должен выпить сорбент. При проведении процедур для улучшения общего состояния врачи контролируют работу почек и печени.
Ученые считают кадмий одновременно полезным и вредным металлом. Он применяется в разных направлениях промышленности, но очень опасен организма. Длительный контакт с кадмием может привести к острому или хроническому отравлению.
Кадмий
(молярная масса)
(первый электрон)
Кадмий — элемент двенадцатой группы (в устаревшей классификации — побочной подгруппы второй группы), пятого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 48. Обозначается символом Cd (лат. Cadmium ). Простое вещество кадмий при нормальных условиях — мягкий ковкий тягучий переходный металл серебристо-белого цвета. Устойчив в сухом воздухе, во влажном на его поверхности образуется плёнка оксида, препятствующая дальнейшему окислению металла. Кадмий и его соединения ядовиты.
Содержание
История открытия
Открыт немецким профессором Ф. Штромейером в 1817 году. Провизоры Магдебурга при изучении оксида цинка ZnO заподозрили в нём примесь мышьяка. Штромейер выделил из ZnO коричнево-бурый оксид, восстановил его водородом и получил серебристо-белый металл, который получил название кадмий.
Происхождение названия
Штромейер назвал кадмий по греческому названию руды, из которой в Германии добывали цинк, — καδμεία. В свою очередь, руда получила своё название в честь Кадма, героя древнегреческой мифологии.
Нахождение в природе
Среднее содержание кадмия в земной коре — 130 мг/т, в морской воде — 0,11 мкг/л. Кадмий относится к редким, рассеянным элементам: он содержится в виде изоморфной примеси во многих минералах и всегда в минералах цинка. Известно всего лишь 6 кадмиевых минералов. Весьма редкими минералами кадмия являются гринокит CdS (77,8 % Cd), хоулиит (то же), отавит CdCO3, монтепонит CdO (87,5 % Cd), кадмоселит CdSe (47 % Cd), ксантохроит CdS(H2O)х (77,2 % Cd). Основная масса кадмия рассеяна в большом числе минералов (более 50), преимущественно в сульфидах цинка, свинца, меди, железа, марганца и ртути. Максимальная концентрация отмечена в минералах цинка и, прежде всего, в сфалерите (до 5 %). В большинстве же случаев содержание кадмия в сфалерите не превышает 0,4—0,6 %. В других сульфидах, например, в станине содержание кадмия — 0,003—0,2 %, в галените — 0,005—0,02 %, в халькопирите — 0,006—0,12 %; из этих сульфидов кадмий обычно не извлекается.
Кадмий не образует самостоятельных месторождений, а входит в состав руд месторождений других металлов. Относительно высоко содержание кадмия в рудах среднетемпературных свинцово-цинковых и частично медно-колчеданных месторождений.
Почва содержит 0,06 мг/кг, глина — 0,3 мг/кг.
Нахождение в продуктах
ПДК кадмия в воде согласно СанПиН 2.1.4.1074-01 «Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества. Гигиенические требования к обеспечению безопасности систем горячего водоснабжения» — 1 мкг/л
Ископаемый уголь, древесный уголь, ПЭТ тара, древесные гранулы пеллеты (до 0,5 мг/кг), рыба (0,2 мг/кг), какао-порошок (0,5 мг/кг), почки животных (1 мг/кг), рис (0,06 мг/кг), сигарета (0,002 мг/кг), пшеничный хлеб (0,03 мг/кг), маргарин (0,042 мг/кг), говядина/свинина (0,016 мг/кг), креветки (1,2 мг/кг)
Получение
Единственный минерал, который представляет интерес в получении кадмия — гринокит, так называемая «кадмиевая обманка». Его добывают вместе со сфалеритом при разработке цинковых руд. В ходе переработки кадмий концентрируется в побочных продуктах процесса, откуда его потом извлекают. В настоящее время производится около 20000 тонн кадмия в год.
Физические свойства
Кадмий — серебристо-белый мягкий металл с гексагональной решёткой. Температура плавления — 321 °C, температура кипения — 770 °C. Если кадмиевую палочку изгибать, то можно услышать слабый треск — это трутся друг о друга микрокристаллы металла (так же трещит и пруток олова); любые примеси в металле уничтожают этот эффект. Кадмий твёрже олова, но мягче цинка — его можно резать ножом. При нагревании выше 80 °C кадмий теряет упругость до такой степени, что его можно истолочь в порошок.
Химические свойства
Сплавы
Кадмий используется как компонент твёрдых припоев (сплавов на основе серебра, меди, цинка) для снижения их температуры плавления. Около 10 % производимого кадмия — компонент ювелирных и легкоплавких сплавов. Сплав кадмия с золотом имеет зеленоватый цвет.
Защитные покрытия
40 % производимого кадмия используется для нанесения антикоррозионных покрытий на металлы. Кадмирование стальных деталей даёт большую устойчивость против коррозии, особенно в морской воде.
Кадмирование — это электролитическая процедура нанесения кадмиевых покрытий на поверхность металлоизделий. Кадмием покрывают высокоуглеродистые, инструментальные и нержавеющие стали, а кадмирование хлористо-аммонийное наносят на высокопрочные стали.
Химические источники тока
Около 20 % кадмия идёт на изготовление кадмиевых электродов, применяемых в аккумуляторах (никель-кадмиевых и серебряно-кадмиевых), нормальных элементах Вестона, в резервных батареях (свинцово-кадмиевый элемент, ртутно-кадмиевый элемент) и др.
Пигменты
Около 20 % кадмия используется для производства неорганических красящих веществ (сульфиды и селениды, смешанные соли, например, сульфид кадмия — кадмий лимонный).
Другие сферы применения
Ограничение применения
В 2016 году принят Технический регламент Евразийского экономического союза «Об ограничении применения опасных веществ в изделиях электротехники и радиоэлектроники» (ТР ЕАЭС 037/2016), по которому содержание кадмия в изделиях электротехники и радиоэлектроники не должно превышать 0,01 % по весу однородного материала (Приложение N 2). В Европе действует аналогичная норма (Директива 2002/95/EC).
Физиологическое действие
Кадмий и все его соединения ядовиты. Особенно опасным случаем является вдыхание паров его оксида (CdO). Вдыхание в течение 1 минуты воздуха с содержанием 2,5 г/м 3 оксида кадмия, или 30 секунд при концентрации 5 г/м 3 является смертельным. Кадмий является канцерогеном.
Пары кадмия, все его соединения токсичны, что связано, в частности, с его способностью связывать серосодержащие ферменты и аминокислоты.
Симптомы острого отравления кадмием — рвота и судороги.
В питьевой воде ПДК для кадмия 0,001 мг/дм³ (СанПиН 2.1.4.1074-01).
Механизм токсического действия
Механизм токсического действия кадмия заключается, по-видимому, в связывании карбоксильных, аминных и особенно сульфгидрильных групп белковых молекул, в результате чего угнетается активность ферментных систем. Растворимые соединения кадмия после всасывания в кровь поражают центральную нервную систему, печень и почки, нарушают фосфорно-кальциевый обмен. Хроническое отравление приводит к анемии и разрушению костей.
Кадмий в норме в небольших количествах присутствуют в организме здорового человека. Кадмий легко накапливается в быстроразмножающихся клетках (например, в опухолевых или половых). Он связывается с цитоплазматическим и ядерным материалом клеток и повреждает их. Он изменяет активность многих гормонов и ферментов. Это обусловлено его способностью связывать сульфгидрильные (-SH) группы.
Изотопы
Из восьми природных изотопов кадмия шесть стабильны, для двух изотопов обнаружена слабая радиоактивность. Это 113 Cd (изотопная распространённость 12,22 %, бета-распад с периодом полураспада 7,7⋅10 15 лет) и 116 Cd (изотопная распространённость 7,49 %, двойной бета-распад с периодом полураспада 3,0⋅10 19 лет).
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
| 1 | H | He | ||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| 8 | Uue | Ubn | Ubu | Ubb | Ubt | Ubq | Ubp | Ubh | Ubs |
Eu, Sm, Li, Cs, Rb, K, Ra, Ba, Sr, Ca, Na, Ac, La, Ce, Pr, Nd, Pm, Gd, Tb, Mg, Y, Dy, Am, Ho, Er, Tm, Lu, Sc, Pu,
Th, Np, U, Hf, Be, Al, Ti, Zr, Yb, Mn, V, Nb, Pa, Cr, Zn, Ga, Fe, Cd, In, Tl, Co, Ni, Te, Mo, Sn, Pb, H2,
W, Sb, Bi, Ge, Re, Cu, Tc, Te, Rh, Po, Hg, Ag, Pd, Os, Ir, Pt, Au
КАДМИЙ
КАДМИЙ (Cadmium) Cd, – химический элемент II группы Периодической системы. Атомный номер 48, относительная атомная масса 112,41. Природный кадмий состоит из восьми стабильных изотопов: 106 Cd (1,22%), 108 Cd (0,88%), 110 Cd (12,39%), 111 Cd (12,75%), 112 Cd (24,07%), 113 Cd (12,26%), 114 Cd (28,85%) и 116 Cd (7,58%). Степень окисления +2, редко +1.
Кадмий был открыт в 1817 немецким химиком Фридрихом Штромейером (Stromeyer Friedrich) (1776–1835).
При проверке оксида цинка, вырабатываемого одной из шенебекских фабрик, появилось подозрение, что он содержит примесь мышьяка. При растворении препарата в кислоте и пропускании через раствор сероводорода выпадал желтый осадок, похожий на сульфиды мышьяка, однако более тщательная проверка показала, что этого элемента нет. Для окончательного заключения образец подозрительного оксида цинка и другие цинковые препараты (в том числе карбонат цинка) с этой же фабрики послали Фридриху Штромейеру, занимавшему с 1802 кафедру химии в Геттингенском университете и должность генерального инспектора ганноверских аптек.
Распространенность кадмия в природе и его промышленное извлечение.
Содержание кадмия в земной коре составляет 1,6·10 –5 %. Он близок по распространенности к сурьме (2·10 –5 %) и в два раза более распространен, чем ртуть (8·10 –6 %). Для кадмия характерна миграция в горячих подземных водах вместе с цинком и другими химическими элементами, склонными к образованию природных сульфидов. Он концентрируется в гидротермальных отложениях. Вулканические породы содержат до 0,2 мг кадмия на кг, среди осадочных пород наиболее богаты кадмием глины – до 0,3 мг/кг, в меньшей степени – известняки и песчаники (около 0,03 мг/кг). Среднее содержание кадмия в почве – 0,06 мг/кг.
У кадмия есть собственные минералы – гринокит CdS, отавит CdCO3, монтепонит CdO. Однако своих месторождений они не образуют. Единственным промышленно значимым источником кадмия являются руды цинка, где он содержится в концентрации 0,01–5%. Кадмий накапливается также в галените (до 0,02%), халькопирите (до 0,12%), пирите (до 0,02%), станните (до 0,2%). Общие мировые ресурсы кадмия оцениваются в 20 млн. т, промышленные – в 600 тыс. т.
Характеристика простого вещества и промышленное получение металлического кадмия.
В сухом воздухе кадмий устойчив. Во влажном воздухе он быстро тускнеет, а при нагревании легко взаимодействует с кислородом, серой, фосфором и галогенами. С водородом, азотом, углеродом, кремнием и бором кадмий не реагирует.
Пары кадмия взаимодействуют с парами воды с выделением водорода. Кислоты растворяют кадмий с образованием солей этого металла. Кадмий восстанавливает нитрат аммония в концентрированных растворах до нитрита аммония. Он окисляется в водном растворе катионами некоторых металлов, например меди(II) и железа(III). С растворами щелочей, в отличие от цинка, кадмий не взаимодействует.
Основные источники кадмия – промежуточные продукты цинкового производства. Осадки металлов, полученные после очистки растворов сульфата цинка действием цинковой пыли, содержат 2–12% кадмия. Во фракциях, образующихся при дистилляционном получении цинка, содержится 0,7–1,1% кадмия, а во фракциях, полученных при ректификационной очистке цинка – до 40% кадмия. Кадмий извлекают и из пыли свинцовых и медеплавильных заводов (она может содержать до 5% и 0,5% кадмия, соответственно). Пыль обычно обрабатывают концентрированной серной кислотой, а затем сульфат кадмия выщелачивают водой.
Из растворов сульфата кадмия действием цинковой пыли осаждают кадмиевую губку, затем ее растворяют в серной кислоте и очищают раствор от примесей действием оксида цинка или карбоната натрия, а также методами ионного обмена. Металлический кадмий выделяют электролизом на алюминиевых катодах либо восстановлением цинком.
Для удаления цинка и свинца металлический кадмий переплавляют под слоем щелочи. Расплав обрабатывают алюминием, чтобы удалить никель, и хлоридом аммония, чтобы избавиться от таллия. Применяя дополнительные методы очистки, можно получить кадмий с содержанием примесей 10 –5 % по массе.
В год производится около 20 тыс. т кадмия. Объем его производства в большой степени связан с масштабами производства цинка.
Важнейшей областью применения кадмия является производство химических источников тока. Кадмиевые электроды используются в батареях и аккумуляторах. Отрицательные пластины никель-кадмиевых аккумуляторов изготовлены из железных сеток с губчатым кадмием в качестве активного агента. Положительные пластины покрыты гидроксидом никеля. Электролитом служит раствор гидроксида калия. На основе кадмия и никеля изготавливают и компактные аккумуляторы для управляемых ракет, только в этом случае в качестве основы устанавливают не железные, а никелевые сетки.
Процессы, протекающие в никель-кадмиевом щелочном аккумуляторе, можно описать суммарным уравнением:
Cd + 2NiO(OH) + 2H2O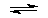
Никель-кадмиевые щелочные аккумуляторы более надежны, чем свинцовые (кислотные). Эти источники тока отличаются высокими электрическими характеристиками, стабильностью работы, длительным сроком эксплуатации. Их можно зарядить всего за один час. Однако никель-кадмиевые аккумуляторы нельзя подзаряжать без полной предварительной разрядки (в этом отношении они уступают металлогидридным аккумуляторам).
Кадмий широко используется для нанесения антикоррозионных покрытий на металлы, особенно в случаях их контакта с морской водой. Кадмируются наиболее важные детали кораблей, самолетов, а также различные изделия, предназначенные для работы в условиях тропического климата. Раньше железо и другие металлы кадмировали погружением изделий в расплавленный кадмий, сейчас кадмиевое покрытие наносят электролитически.
У кадмиевых покрытий есть некоторые преимущества по сравнению с цинковыми: они более устойчивы к коррозии, их легче сделать ровными и гладкими. Высокая пластичность таких покрытий обеспечивает герметичность резьбовых соединений. К тому же кадмий, в отличие от цинка, устойчив в щелочной среде.
Однако у кадмирования есть свои проблемы. При электролитическом нанесении кадмия на стальную деталь в металл может проникнуть содержащийся в электролите водород. Он вызывает у высокопрочных сталей так называемую водородную хрупкость, приводящую к неожиданному разрушению металла под нагрузкой. Для предотвращения этого явления в кадмиевые покрытия вводят добавку титана.
Кроме того, кадмий токсичен. Поэтому, хотя кадмированную жесть применяют довольно широко, для изготовления кухонной утвари и тары для пищевых продуктов использовать ее запрещено.
Примерно десятая часть мирового производства кадмия расходуется на производство сплавов. Кадмиевые сплавы используют главным образом как антифрикционные материалы и припои. Сплав, содержащий 99% кадмия и 1% никеля, применяют для изготовления подшипников, работающих в автомобильных, авиационных и судовых двигателях в условиях высоких температур. Поскольку кадмий недостаточно стоек к действию кислот, в том числе и содержащихся в смазочных материалах органических кислот, иногда подшипниковые сплавы на основе кадмия покрывают индием.
Легирование меди небольшими добавками кадмия позволяет делать более износостойкими провода на линиях электрического транспорта. Медь с добавкой кадмия почти не отличается по электропроводности от чистой меди, но заметно превосходит ее прочностью и твердостью.
Кадмий входит в легкоплавкого сплава Вуда (Wood’s metal), содержащего 50% висмута, 25% свинца, 12,5% олова, 12,5 % кадмия. Сплав Вуда можно расплавить в кипящей воде. Любопытно, что первые буквы компонентов сплава Вуда образуют аббревиатуру ВОСК. Он был изобретен в 1860 не очень известным английским инженером Б.Вудом (B.Wood). Часто это изобретение ошибочно приписывают его однофамильцу – знаменитому американскому физику Роберту Уильямсу Вуду, который родился лишь спустя восемь лет. Легкоплавкие сплавы кадмия используют как материал для получения тонких и сложных отливок, в автоматических противопожарных системах, для спайки стекла с металлом. Припои, содержащие кадмий, довольно устойчивы к температурным колебаниям.
Резкий скачок спроса на кадмий начался в 1940-е и был связан с применением кадмия в атомной промышленности – выяснилось, что он поглощает нейтроны и из него стали делать регулирующие и аварийные стержни атомных реакторов. Способность кадмия поглощать нейтроны строго определенных энергий используется при исследовании энергетических спектров нейтронных пучков.
Соединения кадмия.
Кадмий образует бинарные соединения, соли и многочисленные комплексные, в том числе металлоорганические, соединения. В растворах молекулы многих солей, в частности галогенидов, ассоциированы. Растворы имеют слабокислотную среду вследствие гидролиза. При действии растворов щелочей, начиная с рН 7–8, осаждаются основные соли.
Оксид кадмия CdO получают при взаимодействии простых веществ или прокаливанием гидроксида либо карбоната кадмия. В зависимости от «термической истории» он может быть зеленовато-желтым, коричневым, красным или почти черным. Это частично обусловлено размером частиц, но в большей степени является результатом дефектов кристаллической решетки. Выше 900° С оксид кадмия летуч, а при 1570° С полностью возгоняется. Он обладает полупроводниковыми свойствами.
Оксид кадмия легко растворяется кислотах и плохо – в щелочах, легко восстанавливается водородом (при 900° С), монооксидом углерода (выше 350° С), углеродом (выше 500° С).
Оксид кадмия используют в качестве материала электродов. Он входит в состав смазочных масел и шихты для получения специальных стекол. Оксид кадмия катализирует ряд реакций гидрогенизации и дегидрогенизации.
Гидроксид кадмия Cd(OH)2 выпадает в виде белого осадка из водных растворов солей кадмия(II) при добавлении щелочи. При действии очень концентрированных растворов щелочей он превращается в гидроксокадматы, такие как Na2[Cd(OH)4]. Гидроксид кадмия реагирует с аммиаком с образованием растворимых комплексов:
Кроме того, гидроксид кадмия переходит в раствор под действием цианидов щелочных элементов. Выше 170° С он разлагается до оксида кадмия. Взаимодействие гидроксида кадмия с пероксидом водорода в водном растворе приводит к образованию пероксидов разнообразного состава.
Применяют гидроксид кадмия для получения других соединений кадмия, а также как аналитический реагент. Он входит в состав кадмиевых электродов в источниках тока. Кроме того, гидроксид кадмия используется в декоративных стеклах и эмалях.
Фторид кадмия CdF2 мало растворим в воде (4,06% по массе при 20° С), не растворим в этаноле. Его можно получить действием фтора на металл или фтороводорода на карбонат кадмия.
Фторид кадмия используется в качестве оптического материала. Он входит в состав некоторых стекол и люминофоров, а также твердых электролитов в химических источниках тока.
Хлорид кадмия CdCl2 хорошо растворим в воде (53,2% по массе при 20° С). Его ковалентный характер обусловливает сравнительно низкую температуру плавления (568,5° С), а также растворимость в этаноле (1,5% при 25° С).
Хлорид кадмия получают при взаимодействии кадмия с концентрированной соляной кислотой или хлорированием металла при 500° С.
Хлорид кадмия является компонентом электролитов в кадмиевых гальванических элементах и сорбентов в газовой хроматографии. Он входит в состав некоторых растворов в фотографии, катализаторов в органическом синтезе, флюсов для выращивания полупроводниковых кристаллов. Его используют как протраву при крашении и печатании тканей. Из хлорида кадмия получают кадмиеорганические соединения.
Бромид кадмия CdBr2 образует чешуйчатые кристаллы с перламутровым блеском. Он очень гигроскопичен, хорошо растворим в воде (52,9% по массе при 25° С), метаноле (13,9% по массе при 20° С), этаноле (23,3% по массе при 20° С).
Получают бромид кадмия бромированием металла или действием бромоводорода на карбонат кадмия.
Бромид кадмия служит катализатором в органическом синтезе, является стабилизатором фотоэмульсий и компонентом вирирующих составов в фотографии.
Иодид кадмия CdI2 образует блестящие кристаллы в виде листочков, у них слоистая (двумерная) кристаллическая структура. Известно до 200 политипов иодида кадмия, различающихся последовательностью расположения слоев с гексагональной и кубической плотнейшей упаковкой.
В отличие от других галогенов, иодид кадмия не гигроскопичен. Он хорошо растворяется в воде (46,4% по массе при 25° С). Получают иодид кадмия иодированием металла при нагревании или в присутствии воды, а также действием иодоводорода на карбонат или оксид кадмия.
Иодид кадмия служит катализатором в органическом синтезе. Он является компонентом пиротехнических составов и смазочных материалов.
Сульфид кадмия CdS был, вероятно, первым соединением этого элемента, которым заинтересовалась промышленность. Он образует кристаллы от лимонно-желтого до оранжево-красного цвета. Сульфид кадмия обладает полупроводниковыми свойствами.
В воде это соединение практически не растворяется. К действию растворов щелочей и большинства кислот он также устойчив.
Получают сульфид кадмия взаимодействием паров кадмия и серы, осаждением из растворов под действием сероводорода или сульфида натрия, реакциями между кадмий- и сераорганическими соединениями.
Сульфид кадмия – важный минеральный краситель, раньше его называли кадмиевой желтью.
В малярном деле кадмиевая желть впоследствии стала применяться шире. В частности, ею красили пассажирские вагоны, потому что, помимо прочих достоинств, эта краска хорошо противостояла паровозному дыму. Как красящее вещество сульфид кадмия использовали также в текстильном и мыловаренном производствах. Соответствующие коллоидные дисперсии применяли для получения цветных прозрачных стекол.
В последние годы чистый сульфид кадмия вытесняется более дешевыми пигментами – кадмопоном и цинкокадмиевым литопоном. Кадмопон – смесь сульфида кадмия и сульфата бария. Его получают, смешивая две растворимые соли – сульфат кадмия и сульфид бария. В результате образуется осадок, содержащий две нерастворимые соли:
CdSO4 + BaS = CdS Ї + BaSO4 Ї
Цинкокадмиевый литопон содержит еще и сульфид цинка. При изготовлении этого красителя в осадок выпадают одновременно три соли. Литопон – кремового цвета или цвета слоновой кости.
С добавками селенида кадмия, сульфида цинка, сульфида ртути и других соединений сульфид кадмия дает термически устойчивые пигменты с яркой окраской от бледно-желтой до темно-красной.
Сульфид кадмия придает пламени синюю окраску. Это его свойство используют в пиротехнике.
Кроме того, сульфид кадмия применяется как активная среда в полупроводниковых лазерах. Он случит в качестве материала для изготовления фотоэлементов, солнечных батарей, фотодиодов, светодиодов, люминофоров.
Селенид кадмия CdSe образует темно-красные кристаллы. Он не растворяется в воде, разлагается соляной, азотной и серной кислотами. Получают селенид кадмия сплавлением простых веществ или из газообразных кадмия и селена, а также осаждением из раствора сульфата кадмия под действием селеноводорода, реакцией сульфида кадмия с селенистой кислотой, взаимодействием между кадмий- и селенорганическими соединениями.
Селенид кадмия является люминофором. Он служит в качестве активной среды в полупроводниковых лазерах, является материалом для изготовления фоторезисторов, фотодиодов, солнечных батарей.
Селенид кадмия является пигментом для эмалей, глазурей и художественных красок. Селенидом кадмия окрашивают рубиновое стекло. Именно он, а не оксид хрома, как в самом рубине, сделал рубиново-красными звезды московского Кремля.
Теллурид кадмия CdTe может иметь окраску от темно-серой до темно-коричневой. Он не растворяется в воде, но разлагается концентрированными кислотами. Его получают взаимодействием жидких или газообразных кадмия и теллура.
При нарушении стехиометрии или введении примесей (например, атомов меди и хлора), теллурид кадмия приобретает светочувствительные свойства. Это используется в электрофотографии.
Кадмиеорганические соединения CdR2 и CdRX (R = CH3, C2H5, C6H5 и другие углеводородные радикалы, Х – галогены, OR, SR и др.) обычно получают из соответствующих реактивов Гриньяра. Они термически менее устойчивы, чем их цинковые аналоги, однако в целом менее реакционноспособны (обычно не воспламеняются на воздухе). Их наиболее важной областью применения является получение кетонов из хлорангидридов кислот.
Биологическая роль кадмия.
Кадмий обнаруживается в организмах практически всех животных (у наземных около 0,5 мг на 1 кг массы, а у морских – от 0,15 до 3 мг/кг). Вместе с тем его относят к наиболее токсичным тяжелым металлам.
Кадмий сосредотачивается в организме преимущественно в почках и печени, при этом содержание кадмия в организме к старости повышается. Он накапливается в виде комплексов с белками, которые участвуют в ферментативных процессах. Попадая в организм извне, кадмий оказывает ингибирующее действие на целый ряд ферментов, разрушая их. Его действие основано на связывании группы –SH цистеиновых остатков в белках и ингибировании SH-ферментов. Он может также ингибировать действие цинксодержащих ферментов, замещая цинк. Из-за близости ионных радиусов кальция и кадмия, он может замещать кальций в костной ткани.
Классическим примером хронического отравления кадмием является заболевание, впервые описанное в Японии в 1950-е и получившее название «итай-итай». Болезнь сопровождалась сильными болями в поясничной области, болью в мышцах. Появлялись и характерные признаки необратимого поражения почек. Были зафиксированы сотни смертельных исходов «итай-итай». Заболевание приняло массовый характер в силу высокой загрязненности окружающей среды в Японии в то время и специфики питания японцев – преимущественно рисом и морепродуктами (они способны накапливать кадмий в высоких концентрациях). Исследования показали, что заболевшие «итай-итай» потребляли до 600 мкг кадмия в сутки. В дальнейшем в результате мероприятий по охране окружающей среды, частота и острота синдромов, подобных «итай-итай» заметно снизилась.
В США была обнаружена зависимость между содержанием кадмия в атмосфере и частотой смертельных случаев от сердечно-сосудистых заболеваний.
Считают, что без вреда для здоровья в организм человека в сутки может поступать около 1 мкг кадмия на 1 кг собственного веса. В питьевой воде кадмия не должно содержаться более 0,01 мг/л. Противоядием при отравлении кадмием является селен, однако употребление продуктов, богатых этим элементом, приводит к понижению содержания серы в организме, и в этом случае кадмий снова становится опасным.



