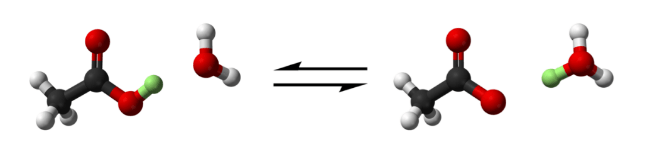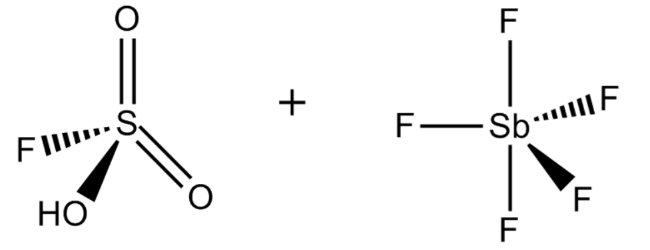как узнать сильная кислота или слабая кислота
Сильная и слабая кислота 2021
Что такое сильная кислота?
Говорят, что кислота является сильной, если она диссоциирует или ионизируется полностью в растворе. Это означает, что он может давать наибольшее количество ионов Н + или протонов при смешивании в растворе. Эти ионы представляют собой заряженные частицы. Поскольку сильная кислота подавляет большее количество ионов при ее разрушении или ионизации, это означает, что сильная кислота является проводником электричества.
Такие химические реакции можно почтить, но в немногих случаях кислота выделяет H + ион довольно легко, и реакция выглядит как односторонняя. И кислота полностью диссоциирована.
Например, когда хлористый водород растворяется в H2O, чтобы сделать HCl, так мало реакции обратного, что мы можем написать:
Когда-нибудь будет проведена стопроцентная виртуальная реакция, в которой хлористый водород будет демонстрировать реакцию с H3O + (Ион гидроксида) и Cl – ионов. Здесь сильной кислотой является хлористый водород.
Что такое слабая кислота?
Говорят, что кислота является слабой, если она частично или частично ионизирует, выделяя в раствор лишь некоторые из ее атомов водорода. Следовательно, он менее эффективен по сравнению с сильной кислотой при выделении протонов. Слабые кислоты имеют более высокую рКа, чем сильные кислоты.
Этановая кислота является хорошим примером слабой кислоты. Он показывает реакцию с H2O для получения H3O + (Ионы гидроксида) и СН3СООН (ионы этаноата), но обратная реакция показывает больший успех, чем передний. Молекулы реагируют довольно легко, чтобы улучшить кислоту, и H2О.
Разница между сильной кислотой и слабой кислотой
Определение
Сильная кислота
Сильная кислота представляет собой кислоту, полностью ионизирующуюся в водном растворе. Сильная кислота всегда теряет протон (A H +), когда растворяется в H2О. Другими словами, сильная кислота всегда находится на цыпочках и достаточно эффективна в подаче протонов.
Слабая кислота
Слабой кислотой является та, которая частично ионизируется в растворе. Он выделяет лишь небольшое количество атомов водорода в раствор. Следовательно, он менее способен, чем сильная кислота.
Электрическая проводимость
Сильная кислота
Сильные кислоты всегда проявляют сильную проводимость. Сильные кислоты обычно пропускают больше тока по сравнению со слабыми кислотами при одинаковом напряжении и концентрации.
Слабая кислота
Слабые кислоты имеют низкую проводимость. Они плохие проводники и показывают низкое значение для текущего прохождения
Скорость реакции
Сильная кислота
Скорость реакции быстрее в сильных кислотах
Слабая кислота
Скорость реакции медленнее в слабых кислотах
Примеры
Сильная кислота
Соляная кислота (HCl), азотная кислота (HNO3), Перхлорной кислоты (HClO4), Серной кислоты (H2ТАК4), Гидроокиси кислота (HI), гидробромовая кислота (HBr), хлорная кислота (HClO3).
Слабая кислота
Серная кислота (H2ТАК3), Уксусная кислота (CH3COOH), фосфорной кислоты (H3ПО4), Бензойной кислоты (C6ЧАС5COOH), фтористоводородную кислоту (HF), муравьиную кислоту (HCOOH), азотную кислоту (HNO2).
Сильная кислота
В сильной кислоте рН ниже, чем обычно 3. Сильные кислоты обладают очень высокой концентрацией ионов H + (кислота с рН 3 имеет 0,001 моль на литр ионов водорода).
Слабая кислота
Слабая кислота имеет рН от 3 до 7.
Значение pKa
Сильная кислота
В сильной кислоте величина pKa довольно низкая.
Слабая кислота
В слабой кислоте значение рКа довольно велико.
диссоциация
Сильная кислота
HCl (g) + H2O (l) ≈ H3О + (aq) + Cl − (Водно)
Слабая кислота
Резюме Сильной кислоты Vs. Слабая кислота
Различия между сильными и слабыми кислотами приведены ниже: Сравнительная таблица
Кислоты и основания
После прочтения статьи Вы сможете разделять вещества на соли, кислоты и основания. В статье описано, что такое pH раствора, какими общими свойствами обладают кислоты и основания.
В неорганической химии, как правило, под кислотой имеют ввиду кислоту Бренстеда-Лоури, то есть вещества, способные отдать протон. Если имеют ввиду определение кислоты по Льюису, то в тексте такую кислоту называют кислотой Льюиса. Данные правила справедливы для кислот и оснований.
Диссоциация
Свойства кислот и оснований
Основания, как правило, мыльные на ощупь, кислоты, в большинстве своём, имеют кислый вкус.
При реакции основания со многими катионами формируется осадок. При реакции кислоты с анионами, как правило, выделяется газ.
Сильные и слабые кислоты и основания
Сильные кислоты
Примеры сильных кислот: HCl, HBr, HF, HNO3, H2SO4, HClO4
Список сильных кислот
Слабые кислоты
Растворяются в воде только частично, например, HF:
Сильные основания полностью диссоциируют в воде:
К сильным основаниям относятся гидроксиды металлов первой (алкалины, щелочные металы) и второй (алкалинотеррены, щёлочноземельные металлы) группы.
Список сильных оснований
Слабые основания
Список слабых оснований
Реакции кислот и оснований
Сильная кислота и сильное основание
Такая реакция называется нейтрализацией: при количестве реагентов достаточном для полной диссоциации кислоты и основания, результирующий раствор будет нейтральным.
Слабое основание и слабая кислота
Сильное основание и слабая кислота
Основание полностью диссоциирует, кислота диссоциирует частично, результирующий раствор имеет слабые свойства основания:
Сильная кислота и слабое основание
Кислота полностью диссоциирует, основание диссоциирует не полностью:
Диссоциация воды
Способы определения pH
Инструментальный метод
Индикаторы
Вещество, которое изменяет цвет в некотором интервале значений pH в зависимости от кислотности раствора, используя несколько индикаторов можно добиться достаточно точного результата.
Все катионы кроме металлов первой и второй группы имеют кислотные свойства.
Буфферный раствор
Растворы, которые сохраняют уровень pH при добавлении небольшого количества сильной кислоты или сильного основания, в основном состоят из:
Для подготовки буфферного раствора определённой кислотности необходимо смешать слабую кислоту или основание с соответствующей солью, при этом необходимо учесть:
Разница между сильными и слабыми кислотами
Содержание:
Ключевые области покрыты
1. Что такое сильная кислота
— определение, свойства, примеры
2. Что такое слабая кислота
— определение, свойства, примеры
3. В чем разница между сильной кислотой и слабой кислотой
— Сравнение основных различий
Ключевые слова: кислота, константа диссоциации кислоты, депротонирование, рН, полярность, протон, сильная кислота, слабая кислота
Что такое сильная кислота
Чем сильнее кислота, тем легче она теряет протоны. Эти протоны легко высвобождаются благодаря высокой полярности связи между атомом Н и остальной частью молекулы. это полярность определяется электроотрицательностью двух атомов, участвующих в этой связи. депротонирования (удаление протона) сильной кислоты зависит от полярности и размера аниона, к которому присоединен протон.
В качестве примера, если рассматривается кислота под названием H-A, диссоциация кислоты HA может быть представлена как
Но если молекула кислоты имеет больше чем один протон, который может быть выпущен, это может быть показано как ниже. Приведенный ниже пример показывает диссоциацию дипротоновой кислоты. Это означает, что он может выпустить два протона.
С другой стороны, сильные кислоты сильно влияют на pH раствора, поскольку сильные кислоты выделяют в раствор ионы H +. PH зависит от концентрации H +. Соотношение между концентрацией H + и pH может быть указано ниже.
Примеры сильных кислот
Что такое слабая кислота
Например, диссоциация этановой кислоты может быть показана, как показано ниже.
Рисунок 1: Диссоциация этановой кислоты
При написании диссоциации слабых кислот следует использовать двойные стрелки вместо одной стрелки. Это показывает, что реакция является равновесной реакцией.
Примеры слабых кислот
Разница между сильными и слабыми кислотами
Определение
Сильная кислота: PH раствора сильной кислоты очень низкий (около pH = 1).
Слабая кислота: РН раствора слабой кислоты составляет около 3-5.
Константа диссоциации кислоты
Сильная кислота: Константа диссоциации кислоты K более высокое значение для сильных кислот.
Слабая кислота: Константа диссоциации кислоты K является более низким значением для сильных кислот.
Количество выпущенных ионов H +
Сильная кислота: Сильные кислоты выделяют всю Н + ионы это может выпустить в раствор.
Слабая кислота: Слабые кислоты не выделяют все Н + ионов.
Заключение
Сила кислоты определяется полярностью и атомными размерами молекулы кислоты. В зависимости от того, как молекулы кислоты диссоциируют в воде, существует два типа кислот: сильные и слабые кислоты. Основное различие между сильными и слабыми кислотами состоит в том, что сильные кислоты полностью диссоциируют в водных растворах, тогда как слабые кислоты частично диссоциируют в водных растворах.
Рекомендации:
1. «Сильные и слабые кислоты». Сильные и слабые кислоты. Н.п., н.д. Web.
Характерные химические свойства кислот
Содержание:
Кислоты – это химические соединения, содержащие в себе положительный атом водорода (катион H+) и кислотный остаток (анион A-). Является сложным веществом.
Общая характеристика
В первую очередь кислоты различают по растворимости. Есть нерастворимые, растворимые и полурастворимые кислоты. Эти различия прописаны в таблице растворимости, так что наизусть запоминать не требуется.
Классификация:
Бескислородные кислоты – это растворы галогеноводородов, атомы которых в растворе связаны полярной ковалентной связью. Название кислоты складывается из названия кислотного остатка в первую очередь, а дальше называется катион (водород). Так с хлором и водородом образуется хлороводородная кислота, а с серой – сероводородная.
Кислородосодержащие кислоты, или оксокислоты называют за счёт наличия в них кислорода. Общего принципа построения названия этих кислот нет, так что их названия необходимо запоминать на память.
Физические свойства
Кислоты, в зависимости от условий, могут быть в трёх агрегатных состояниях: в жидком, твёрдом и газообразном состоянии. Кислоты могут обладать цветом и запахом.
Химические свойства
Изменение цвета индикаторов
Кислота в водной среде способна изменить цвет разных индикаторов. Кислоты окрашивают в красных цвет лакмус, метилоранж и универсальный индикатор. Фенолфталеин не окрашивается.
Взаимодействие кислот с металлами
Кислота способна реагировать только с металлами, находящимися левее водорода в ряду активности металлов.
Из приведенного выше химического уравнения нужно отметить, что при взаимодействии кислоты и металла происходит реакция замещения, образуется соль и выделяется H2.
Взаимодействие кислот с основными и амфотерными оксидами
При взаимодействии кислоты с основным или амфотерным оксидами происходит реакция обмена в результате которой образуются соль и H2O.
В качестве примера приведены следующие реакции:
Из приведённого выше химического уравнения нужно отметить, что в реакциях основного оксида калия и амфотерного оксида алюминия (III) с кислотами, образуется соль и H2O.
Взаимодействие кислот с основными и амфотерными гидроксидами
Из приведённой выше химического уравнения нужно отметить, что при реакции основного гидроксида калия и амфотерного гидроксида алюминия (III) с кислотами образуются соль и H2O.
Взаимодействие кислот с солями
Реакция кислоты с солью является реакцией обмена, так же ее называют реакцией нейтрализации. Она возможно только в случае выпадения соли в осадок, выделения газа, слабые электролиты или вода. Рассмотрим все случаи более подробно.
Из приведённого выше химического уравнения можно увидеть, что при взаимодействии кислоты и соли образуются новые кислота и нерастворимая соль, которые выпадают в осадок. Осадок может иметь различную окраску, плотность и консистенцию.
Из приведённых выше химических уравнений нужно отметить, что при реакции соли с кислотой образуется новая соль и выделяется газ. Разберём одну из реакций: при взаимодействии твёрдого хлорида натрия с концентрированной хлороводородной кислотой образовалась натриевая соль серной кислоты и выделился летучий газ хлороводород.
Такие реакции возможны только при условии, когда одним из реагентов сильный электролит. Для того, чтобы убедиться, что реакция будет протекать используют вытеснительный ряд:
В этом ряду кислоты расположены так, что в растворах кислот и их солей могут в результате реакции вытесняют из раствора те, что стоят левее в ряду. Азотная и фосфорная кислоты находятся на одном месте в ряду, т.к. имеют одинаковые вытеснительные способности.
Из приведённого выше химического уравнения нужно отметить, что хлороводородная кислота, которая находится в данном ряду левее, способна вытеснять кислотный остаток карбоновой кислоты, стоящей в ряду правее. Нужно учитывать, что карбоновая кислота слабая и при стандартных условиях она распадется на углекислый газ и воду. Углекислый газ выделяется из раствора, а вода остаётся.
Разложение кислородсодержащих кислот
В результате реакции разложения кислородсодержащих кислот всегда образуется вода и оксид.
Из приведённых выше реакций можно увидеть, что карбоновая легко разлагается при обычных условиях, так как является одной из самых слабой кислотой. Для разложения сернистой и кремниевой кислоты их растворы необходимо нагреть. Во всех трёх реакция в результате образуется вода и оксиды кислотных остатков.
8 сильнейших кислот, известных нам
Что делает кислоту сильной или слабой? Чтобы ответить на этот вопрос, нам сначала нужно взглянуть на определение кислоты. Это химическое соединение, которое принимает электроны и / или отдает (диссоциирует) ионы водорода, также известные как протоны.
Следовательно, уровни кислотности кислоты зависят от ее способности диссоциировать ионы водорода, т.е. чем больше число ионов водорода, продуцируемых кислотой в растворе, тем более кислым он является. Теперь, прежде чем мы перейдем к списку сильнейших кислот на Земле, есть определенные термины и определения, с которыми вам необходимо ознакомиться.
Это подводит нас к другому связанному и важному показателю кислотности pKa. Это в основном отрицательный целочисленный логарифм Ka.
Чем сильнее кислота, тем ниже значения pKa.
Уксусная кислота отдает протон (в зеленом цвете) воде, чтобы произвести ион гидрония и ион ацетата. (Кислород в красном, водород в белом и углерод в черном)
Функция кислотности Гаммета: (H o) Всем нам известна шкала pH, которая обычно используется для измерения уровней кислотности или основности химических веществ, но когда речь идет о суперкислотах, она просто становится бесполезной, поскольку их уровни кислотности в миллион раз больше, чем серная и соляная кислоты.
Таким образом, чтобы измерить суперкислоты на основе их уровней кислотности, исследователи придумали функцию кислотности Гаммета. Первоначально он был предложен американским физическим химиком Луи Плаком Гаммет.
8. Серная кислота
Серная кислота (98%) на листе бумаги
Серная кислота или купорос не нуждаются в формальном введении. Он не имеет запаха, цвета и вызывает интенсивную экзотермическую реакцию при смешивании с водой. Серная кислота является важным химическим веществом, которое необходимо для многих отраслей промышленности, таких как сельское хозяйство, очистка сточных вод и нефтепереработка. Она также используется в кислотах аккумулятора и чистящих средствах.
Она также играет важную роль в изучении кислот в целом. Серная кислота служит базовым эталоном для сравнения уровней кислотности суперкислот или кислот. Хотя существует несколько способов получения серной кислоты, обычно используют контактный процесс и влажный процесс серной кислоты.
H 2 SO 4 может нанести значительный ущерб коже человека при прямом контакте. Это также очень разъедает многие металлы. Химическое вещество гораздо более агрессивно и опасно, когда присутствует в высокой концентрации, благодаря своим превосходным окислительным и дегидратирующим свойствам.
7. Соляная кислота
Подобно серной кислоте, соляная кислота также является важным химическим веществом, которое широко используется в лабораториях и различных отраслях промышленности. Соляная кислота была обнаружена где-то около 800 г. н.э. иранским ученым-эрудитом по имени Джабир ибн Хайян.
Те, кто задаются вопросом, почему соляная кислота сильнее серной кислоты, несмотря на то, что последняя является контрольной точкой для суперкислот, причина этого заключается в том, что серная кислота является дипротоновой кислотой, которая обычно не полностью диссоциирует.
Другими словами, HCl сильнее серной кислоты, поскольку ее ионы водорода (HCl) легко отделяются от хлорида по сравнению с сульфат-ионом из серной кислоты. Так или иначе, соляная кислота в основном используется в тяжелой промышленности для удаления ржавчины с железа и стали перед дальнейшей обработкой. Кроме того, это жизненно важный компонент в производстве органических (винилхлорид используется для ПВХ) и многих неорганических соединений.
6. Трифторметансульфоновая кислота
Трифликовая кислота используется во многих протонированиях и титрованиях (количественный анализ химического состава). Важная причина, по которой трифликовая кислота является предпочтительной в определенных случаях, заключается в том, что она не сульфонирует другие вещества, что характерно для хлорсульфоновой кислоты и серной кислоты.
Излишне говорить, что это чрезвычайно опасно. Любой контакт кожи с кислотой может вызвать серьезные ожоги и может привести к незначительному повреждению тканей. Это может также вызвать отек легких и судороги и другие критические условия при вдыхании.
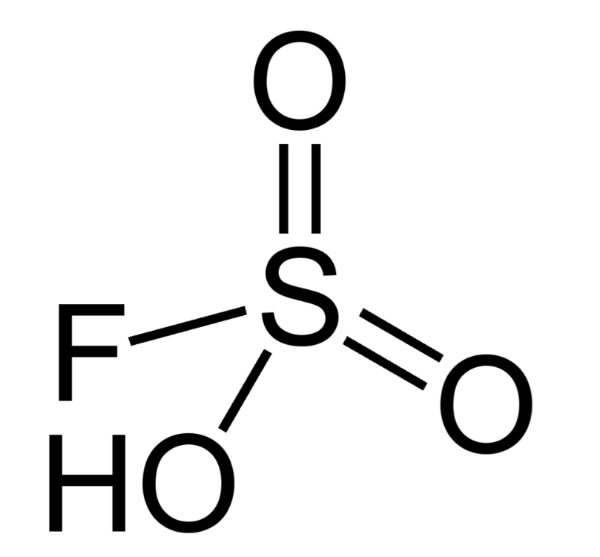
5. Фторсульфоновая кислота
Фторосерная кислота или серно-фтористоводородная кислота (официальное название) является второй сильнейшей однокомпонентной кислотой, доступной сегодня. Это желтый на вид и, конечно, очень едкий / токсичный. HSO 3 F обычно получают путем взаимодействия фтористого водорода с триоксидом серы, и в сочетании с пентафторидом сурьмы он образует «волшебную кислоту», гораздо более сильную кислоту и протонирующий агент.
Кислота может быть использована для алкилирования углеводородов (с алкенами) и изомеризации алканов, а также для травления стекла (художественное стекло). Это обычный фторирующий агент в лабораториях.
4. Хлорная кислота
Хлорная кислота является одной из самых сильных кислот Бренстеда-Лоури, которые обладают сильными окислительными свойствами и обладают высокой коррозионной активностью. Традиционно ее получают обработкой перхлората натрия соляной кислотой (HCl), которая также создает хлорид натрия.
NaClO4 + HCl → NaCl + HClO4
В отличие от других кислот, хлорная кислота не подвержена гидролизу. Это также одна из самых регулируемых кислот в мире. Еще в 1947 году в Лос-Анджелесе, штат Калифорния, около 150 человек получили ранения и 17 человек погибли в результате химического взрыва, в котором содержалось почти 75% хлорной кислоты (по объему) и 25% ангидрида уксусной кислоты. Также было повреждено более 250 близлежащих зданий и транспортных средств.
Несмотря на взрывную природу, хлорная кислота широко используется и даже предпочтительна в некоторых типах синтеза. Это также важный компонент перхлората аммония, который используется в современном ракетном топливе.
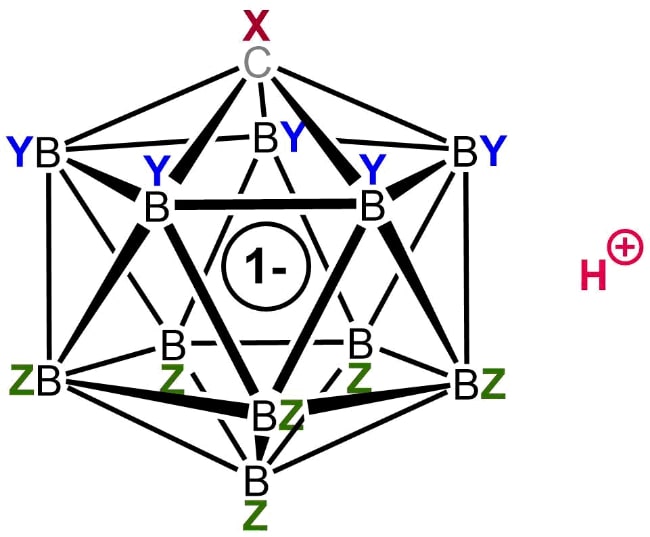
3. Фторированная карборановая кислота
Общая структура карбоновой кислоты
Одним из таких членов этой группы является фторированная карборановая кислота. Хотя о существовании такого химического вещества первоначально сообщалось в 2007 году, исследователи смогли в полной мере изучить его природу только в 2013 году. До его открытия корона сильнейшей кислоты Бренстеда перешла к сильно хлорированной версии этого семейства суперкислот.
Фторированный карборан является единственной известной кислотой, которая может протонировать (переносить ион водорода) диоксид углерода с образованием катионов, соединенных водородом. В отличие от этого, CO 2 не подвергается какой-либо заметной протонации при обработке другими суперкислотами, такими как магическая кислота и HF-SbF5.
2. Волшебная кислота
FSO 3 H · SbF 5, наиболее известный как магическая кислота, получают смешением фторсерной кислоты и пентафторида сурьмы в молярном соотношении 1: 1. Эта сверхкислотная система была впервые разработана в 1966 году исследователями из лаборатории Джорджа Олаха, Университета Case Western Reserve в Огайо.
Его довольно причудливое название было установлено после официального события в 1966 году, когда сотрудник лаборатории Олаха продемонстрировал протонирование углеводородов, в котором парафиновая свеча «волшебным образом» растворилась и превратилась в раствор трет-бутильного катиона после того, как она была помещена в то, что сейчас известно как волшебная кислота.
Хотя Волшебная кислота обычно используется для стабилизации ионов углерода в растворах, она имеет несколько других важных промышленных применений. Например, он может ускорить изомеризацию насыщенных углеводородов и даже протоната метана, ксенона и галогенов, которые все являются слабыми основаниями.
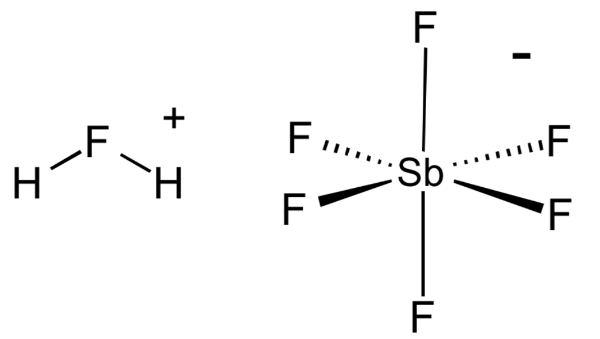
1. Фтороантимоновая кислота
Фторантимоновая кислота является, пожалуй, самой сильной из всех известных суперкислот, основанных на значениях функции кислотности Гаммета. Его получают путем смешивания фтористого водорода с пентафторидом сурьмы, как правило, в соотношении 2: 1. Эта реакция носит экзотермический характер.
Этот суперкислота имеет несколько важных применений в химическом машиностроении и нефтехимической промышленности. Например, его можно использовать для отделения метана и Н 2 от неопентана и изобутана (оба алкана) соответственно.
Неудивительно, что H 2 FSbF 6 чрезвычайно агрессивен и может подвергаться сильному гидролизу при контакте с водой. Как и большинство суперкислот, фторантимоновая кислота может питаться прямо через стекло, поэтому она должна храниться в контейнерах из политетрафторэтилена.
Теперь, большинство из вас, возможно, наткнулись на карбоновые кислоты (либо хлорированная карбоновая кислота, либо фторированная карборановая кислота), когда искали «самые сильные кислоты в мире». Ну, технически они верны, так как карбоновые кислоты являются самыми сильными известными однокомпонентными кислотами на Земле, гораздо более кислыми, чем подобные хлорной и трифликовой кислотам (фтороантимоновая кислота на самом деле является смешанной кислотой).