Атропин для кошек для чего
Атропина сульфата раствор для инъекций 1% (для ветеринарного применения) (Atropine sulfate solution for injections 1% (for veterenaty purposes)
Состав по компонентам
Белый кристаллический или зернистый порошок, растворим в воде и спирте.
Алкалоид, содержащийся в растениях семейства пасленовых, блокатор м-холинорецепторов. Препятствует стимулирующему действию ацетилхолина, уменьшает секрецию слюнных, желудочных, бронхиальных, слезных, потовых желез, поджелудочной железы. Снижает тонус мышц ЖКТ, желчных протоков и желчного пузыря; вызывает тахикардию, улучшает AV проводимость. После в/в введения максимальный эффект проявляется через 2-4 мин, после орального приема (в виде капель) через 30 мин. Возбуждает кору головного мозга (в высоких дозах). Расширяет зрачки, затрудняет отток внутриглазной жидкости, повышает внутриглазное давление, вызывает паралич аккомодации. Зрачок, расширенный атропином, не суживается при инстилляции холиномиметических препаратов. Максимальное расширение зрачка наступает через 30-40 мин, исчезает через 7-10 дней.
Язвенная болезнь желудка и двенадцатиперстной кишки, пилороспазм, желчнокаменная болезнь, холецистит, острый панкреатит, гиперсаливация (паркинсонизм, отравление солями тяжелых металлов), спазмы кишечника и мочевых путей, печеночная и почечная колики, бронхиальная астма, для предупреждения бронхо- и ларингоспазма, AV блокада, отравления м-холиномиметиками (мухомор), антихолинэстеразными средствами, премедикация перед хирургическими операциями. Местно (в офтальмологии): для исследования глазного дна, для расширения зрачка и достижения паралича аккомодации с целью определения истинной рефракции глаза; для лечения иритов, иридоциклитов, хориоидитов, кератитов, эмболий и спазмов центральной артерии сетчатки и некоторых травм глаза.
Сухость во рту, мидриаз, атония кишечника, головокружение, тахикардия, затруднение мочеиспускания, гиперемия кожи век, фотофобия, отек конъюнктивы век и глазного яблока. Ксеростомия, мидриаз, паралич аккомодации, тахикардия, атония кишечника, атония мочевого пузыря, головная боль, головокружение, утрата осязания.
Гиперчувствительность, закрытоугольная глаукома, нарушения мочеиспускания при аденоме предстательной железы.
При инстилляции раствора в глаз необходимо прижать нижнюю слезную точку во избежании попадания раствора в носоглотку. При субконъюнктивальном или парабульбарном введении для уменьшения тахикардии целесообразно назначить валидол.
Платифиллин (Platyphylline)
Владелец регистрационного удостоверения:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Платифиллин
Фармакологическое действие
Блокатор м-холинорецепторов. По сравнению с атропином оказывает менее выраженное влияние на периферические м-холинорецепторы (по действию на гладкомышечные клетки органов ЖКТ и циркулярной мышцы радужки в 5-10 раз слабее атропина). Блокируя м-холинорецепторы, нарушает передачу нервных импульсов с постганглионарных холинергических нервов на иннервируемые ими эффекторные органы и ткани (сердце, гладкомышечные органы, железы внешней секреции); подавляет также н-холинорецепторы (значительно слабее). Холиноблокирующее действие в большей степени проявляется на фоне повышенного тонуса парасимпатической части вегетативной нервной системы или действия м-холиностимуляторов.
Фармакокинетика
Показания активных веществ препарата Платифиллин
Язвенная болезнь желудка и двенадцатиперстной кишки, пилороспазм, холецистит, холелитиаз, кишечная колика, почечная колика, желчная колика; бронхиальная астма (для предупреждения бронхо- и ларингоспазма), бронхорея; альгодисменорея; спазм церебральных артерий; ангиотрофоневроз; артериальная гипертензия, стенокардия (в составе комбинированной терапии).
Расширение зрачка с диагностической целью (в т.ч. исследование глазного дна, определение истинной рефракции глаза); острые воспалительные заболевания глаз (в т.ч. ирит, иридоциклит, кератит), травмы глаза.
Открыть список кодов МКБ-10
| Код МКБ-10 | Показание |
| G45 | Преходящие транзиторные церебральные ишемические приступы [атаки] и родственные синдромы |
| H16 | Кератит |
| H20.0 | Острый и подострый иридоциклит (передний увеит) |
| H20.1 | Хронический иридоциклит |
| I10 | Эссенциальная [первичная] гипертензия |
| I20 | Стенокардия [грудная жаба] |
| I73.0 | Синдром Рейно |
| J45 | Астма |
| K25 | Язва желудка |
| K26 | Язва двенадцатиперстной кишки |
| K27 | Пептическая язва |
| K31.3 | Пилороспазм, не классифицируемый в других рубриках |
| K80 | Желчнокаменная болезнь [холелитиаз] (в т.ч. печеночная колика) |
| K81.0 | Острый холецистит |
| K81.1 | Хронический холецистит |
| N23 | Почечная колика неуточненная |
| N94.4 | Первичная дисменорея |
| N94.5 | Вторичная дисменорея |
| R10.4 | Другие и неуточненные боли в области живота (колика) |
| S05 | Травма глаза и глазницы |
| Z01.0 | Обследование глаз и зрения |
Режим дозирования
Применяют внутрь, парентерально (п/к, в/в), ректально, местно в офтальмологии.
Доза зависит от показаний, пути введения, возраста пациента.
Побочное действие
Со стороны пищеварительной системы: сухость во рту, жажда, атония кишечника.
Со стороны сердечно-сосудистой системы: снижение АД, тахикардия.
Со стороны ЦНС и периферической нервной системы: возбуждение ЦНС, головокружение, расширение зрачков, паралич аккомодации, головная боль, фотофобия, судороги, острый психоз.
Со стороны мочевыделительной системы: затруднение мочеиспускания, задержка мочи.
Прочие: ателектаз легкого.
Побочные реакции наиболее вероятны при применении платифиллина в высоких дозах.
Противопоказания к применению
Применение при беременности и кормлении грудью
Применение при нарушениях функции печени
Применение при нарушениях функции почек
Применение у детей
Особые указания
Влияние на способность к управлению транспортными средствами и механизмами
Необходимо воздерживаться от потенциально опасных видов деятельности, требующих повышенного внимания и быстроты психомоторных реакций.
Лекарственное взаимодействие
Платифиллин является антагонистом прозерина.
При одновременном применении увеличивается продолжительность снотворного действия фенобарбитала, этаминала натрия, магния сульфата.
Морфин усиливает угнетающее действие платифиллина на сердечно-сосудистую систему.
Местная анестезия в ветеринарной практике (спектр применения, показания и противопоказания, техника, дозировки)
Актуальность темы
Осветить простоту и необходимость применения местной анестезии, исходя из литературных данных, а также собственных результатов.
Методы
Местная анестезия подразделяется на:
– терминальную (анестезию поверхности органа);
– инфильтрационную (пропитывание анестетиком тканей);
– регионарную: паравертебральную, межреберную, стволовую, сакральную, анестезию челюстной области;
– спинномозговую (субарахноидальную);
– перидуральную (эпидуральную);
– внутрикостную;
– внутривенную регионарную;
– анестезию поперечного сечения.
Материалы
Для проведения местной анестезии в первую очередь требуются анестетик, инъекционные иглы (для мелких животных), спинальные иглы (для крупных животных), эпидуральные катетеры.
Используемые в настоящее время анестетики являются химическими производными кокаина, растительного алкалоида. Уже к 1960 г. был изобретен аналог лидокаина. При выборе анестетика необходимо ориентироваться на его свойства. Не меньшее значение имеет и цена (лидокаин в десятки раз дешевле бупивакаина и ропивакаина). Зная особенности действующего вещества, можно сделать правильный выбор или подобрать верную комбинацию и сочетать препараты.
Свойства местных анестетиков
Местом действия анестетика является липидная оболочка нервных клеток, поэтому важной характеристикой является растворимость в жирах, которая определяет активность вещества. Другой интересный показатель – рКа, чем ближе эта цифра к физиологическому рН, тем быстрее начинает действовать местный анестетик. В щелочной среде адреналин нестабилен, поэтому содержащие его анестетики (ультракаин, убистезин) имеют рН около 4-5, следовательно, они начинают работать медленнее, чем анестетики, в которые адреналин добавляют непосредственно перед работой. Аналогичная проблема возникает при обезболивании воспаленных участков (где величина рН низкая), там для развития эффекта требуется больше времени. Подщелачивание раствора (0,2 мл 5%-ного натрия бикарбоната на 2 мл 1%-ного лидокаина) ускоряет начало действия, удлиняет его продолжительность и уменьшает боль при подкожном введении.
Добавление адреналина усиливает вазоконстрикцию, абсорбция анестетика уменьшается, а длительность его действия увеличивается, но это актуально только для анестетиков короткого действия (лидокаин), в отношении бупивакаина и ропивакаина это малоэффективно. Закономерно, что для кошек дозы анестетика обычно ниже, т. к. токсический эффект достигается раньше, а период действия меньше.
Токсичность и влияние на организм
Сердечно-сосудистая система: передозировка лидокаином вызывает аритмии и депрессию кровообращения; попадание ропивакаина в кровяное русло приводит к АВ-блокаде, желудочковым аритмиям и судорогам. Дыхательная система: лидокаин устраняет рефлекторный бронхоспазм, к апноэ может привести блокада межреберных нервов. ЦНС: токсичность слабо выражена из-за предварительной седации. Иногда могут быть мышечные подергивания (особенно во время введения).
Техника выполнения
Показания (операции на тазовых конечностях, хвосте, тазовой и брюшной полостях). Препарат: лидокаин 2%-ный в дозе 2-4 мг/кг в зависимости от области проведения вмешательства. Если операции на хвосте или тазовых конечностях, достаточно 2-3 мг/кг, если проводится овариогистерэктомия или диагностическая лапаротомия, дозы увеличивают до 4 мг/кг. Бупивакаин/ропивакаин из расчета 2-3 мг/кг. Общий объем препарата не должен превышать 1,5 мл для кошки и 10 мл для собаки. Для введения анестетика возможно применение обычных игл (для мелких животных) или спинальных. Размер иглы выбирают в зависимости от размера и упитанности животного. Лучший тест на проникновение в эпидуральное пространство – это характерное потрескивание при прохождении желтой связки и потеря сопротивления при введении раствора. Отсутствие болевой чувствительности тазовых конечностей и зияние ануса через 5-10 мин после введения препарата свидетельствуют об успешном проведении анестезии. При выполнении кесарева сечения эффективно добавлять к анестетику налбуфин из расчета 0,25 мг/кг. Применение эпидурального катетера необходимо при операции длительностью более 3-4 часов или при высокой степени болевого синдрома в послеоперационный период. Также благодаря катетеру возможно проведение высокой эпидуральной анестезии при операции на органах грудной клетки.
Пример анестезиологического протокола:
1) Кошка (унилатеральная мастэктомия + овариогистерэктомия) вес 4 кг, 7 лет. Анестезиологический риск 2-й степени.
Ожидаемая степень боли: от умеренной до тяжелой.
Премедикация: антибиотик, НПВП.
Седация: пропофол 6 мг/кг.
Эпидуральная анестезия: налбуфин 1 мг + лидокаин 3,5 мг/кг (0,7 мл 2%-ный лидокаин).
Дополнительно: золетил из расчета 1-2 мг/кг.
Послеоперационный период: опиоиды каждые 8 часов из расчета 0,4 мг/кг.
2) Собака (ампутация тазовой конечности) вес 25 кг, 3 года.
Анестезиологический риск 2-3-й степени.
Ожидаемая степень боли: от умеренной до
тяжелой.
Премедикация: антибиотики, ранняя анальгезия опиатами.
Седация: опиаты + медетомидин 10-30 мкг/кг + пропофол 6 мг/кг.
Эпидуральная анестезия: катетер L7-S1 до L5, бупивакаин 1,5 мг/кг (7,5 мл 0,5%-ного
раствора)
Дополнительно: если катетер установлен верно – ничего, если анестезия неадекватная – газ
или золетил.
Послеоперационный период: опиоиды каждые 8 часов из расчета 0,4 мг/кг.
Блокада плечевого сплетения
Показания: операции на грудной конечности ниже уровня локтя
Препарат выбора: лидокаин или бупивакаин
Перед проведением блокады животное должно быть хорошо седировано. Для введения анестетика используют спинальные иглы размером от 21G до 18G, иглу вводят медиальнее плечевого сустава на 2-3 см, но латеральнее ребра параллельно позвоночнику. Некоторые авторы рекомендуют после введения иглы на ½ изменить угол более дорсально. Необходимо убедиться, что не повреждены сосуды, после чего вводится анестетик, дозу которого лучше распределять на нескольких уровнях. В связи с тем что плечевое сплетение и связанные с ним нервы занимают обширное пространство, дозу анестетика разводят NaCl на 50% для увеличения объема раствора. Потеря чувствительности происходит в течение 10-20 мин идлится около 2-4 часов. Полное восстановление наступает через 6 часов. Блокада плечевого сплетения – достаточно эффективный и безопасный метод, но могут возникнуть проблемы с длительным периодом ожидания эффекта особенно у собак с ожирением.
Анестезиологический протокол: собака (ампутация запястья) вес 15 кг, возраст 10 мес.
Ожидаемая степень боли: от умеренной до тяжелой.
Анестезиологический риск 2-й степени.
Премедикация: антибиотики, НПВП.
Седация: опиаты + медетомидин 10-30 мкг/кг + пропофол 6 мг/кг.
Блокада плечевого сплетения: бупивакаин 0,5%-ный 2 мг/кг (30 мг = 6 мл, развести до 12 мл NaCl).
Дополнительно: если катетер установлен верно – ничего, если анестезия неадекватная – газ или золетил.
Послеоперационная анальгезия: опиоиды при необходимости.
Блокада межреберных нервов
Показания: снятие боли во время и после торакотомии, наличие плеврального дренажа, переломы ребер. Блокада позволяет минимизировать количество системных анальгетиков, которые способны угнетать дыхание. Инъекция позволяет обезболить участок в два межреберных промежутка. Суммарная доза от всех инъекций анестетика не должна превышать общей дозы на вес животного.
Препарат выбора: лидокаин, бупивакаин, ропивакаин.
Целесообразно применять данную блокаду после торакотомии или до операции в случае длительного ожидания. Обычно выраженной седации не требуется и достаточно обезболивания. Анестетик вводят в два промежутка каудальнее и в два промежутка дорсальнее области разреза. Препарат быстро всасывается в кровь, поэтому не стоит превышать дозу 1,5 мг/кг в сумме на всю блокаду. При введении может возникнуть чувство жжения, для уменьшения неприятных ощущений анестетик можно разводить NaCl. Еще один способ снизить боль и улучшить экскурсию грудной клетки – интраплевральная анестезия. Анестетик вводится по дренажным трубкам в дозе 1,5 мг/кг в течение 1-2 мин, после чего лучше положить животное на бок, где располагается разрез. Вероятно, эффект достигается из-за ретроградной блокады межреберных нервов. Перед введением раствора необходимо провести аспирацию жидкости и воздуха.
Анестезиологический протокол: собака доберман, торакотомия по поводу резекции доли легкого (абсцесс), возраст 3 г, вес 37 кг.
Ожидаемая степень боли: от умеренной до тяжелой.
Премедикация: атропин, опиаты.
Седация: миорелаксанты (если доступны).
Анестезия: кетамин (или золетил), пропофол, высокая эпидуральная анестезия.
Послеоперационный период: блокада межреберных нервов – ропивакаин 1,5 мг/кг (5,5 мл 1%-ного раствора) по 1,1 мл в каждый из 5 межреберных промежутков.
Интраплевральная блокада: (после того как животное проснется) 5,5 мл ропивакаина до 10 мл NaCl каждые 8 часов в течение 24-36 часов + опиаты.
Ретробульбарная блокада
Применение: операция на глазном яблоке, удаление глазного яблока.
Препарат выбора: лидокаин (+ адреналин, новокаин 0,5%-ный).
Выводы
Таким образом, при качественном выполнении местного обезболивания возможно снизить дозы общего анестетика, а порой и ограничиться только гипнотическими средствами, улучшить состояние животного после операции, а значит, сократить реабилитацию. Применение местных анестетиков несущественно удорожает стоимость операции, зато поднимает имидж клиники и позволяет выполнять больший спектр операций. Выражаю благодарность всей операционной бригаде и отделению реабилитации, без этих людей совершенствовать свою работу невозможно, мы одна команда!
(Вилковыский И. Ф., Чернявская А. В., Плярпа И. А., Масалов В. В., Гекова Н., Смирнова Ю.)
Системный подход к лечению ХПН и ОПН у кошек и собак
Известно расхожее выражение, что все мы состоим из воды. В сфере диализа жидкостная среда организма так и называется – вода. И у людей, и у животных в ней происходят все биохимические процессы, обеспечивающие полноценную жизнь. Здесь же накапливаются токсины, в том числе уремические, сигнализирующие о патологическом состоянии почек, почечной недостаточности.
Активная вода организма составляет 70 % массы тела. Если же рассматривать ее состав в процентных соотношениях, то в самых больших объемах представлены вода плотных тканей и внутриклеточная вода – 40 и 33 процента соответственно. Далее следует интерстициальная жидкость и лимфа – 12 %. Всего 4,5 процента приходится на долю плазмы крови, по столько же – на воду хрящей и необменную воду костей. Наконец, оставшиеся 1,5 % – трансцеллюлярная вода.
Представим живой организм в виде некой емкости. У нас получится сосуд, разделенный множеством мембран, через которые постепенно просачивается вода. Если она загрязнена, то с течением времени станет грязной жидкость во всем сосуде. Из этого наглядного примера обмена веществ понятно, что при почечной недостаточности мочевые токсины накапливаются не только и не столько в крови, но и во всей активной воде организма – и вся она требует очищения. Об этом следует помнить при расчете дозы гемодиализа. Также не стоит забывать о прямой зависимости времени выравнивания уремических токсинов крови и остальной жидкости от степени дегидратации организма: при обычных условиях процесс занимает порядка четырех часов, в обезвоженной же клетке обмен происходит значительно медленнее.
Снова рассмотрим на примере. Возьмем животное массой 20 кг с мочевиной крови 50 ммоль/литр. Из вышесказанного ясно, что такой же уровень уремической интоксикации будет иметь вся вода организма, а это порядка 14 л жидкости – и необходимо очистить весь этот объем. Очевидно, что плазмаферез, удаляющий 30 процентов плазмы, то есть всего 1,5 % от общей воды, окажется неэффективным, и должно быть принято решение о проведении гемодиализа.
Лечение любого заболевания внутренних органов должно начинаться с создания оптимальных условий, при которых они смогут полноценно выполнять свою работу. Такого же подхода требует и почечная недостаточность у кошек или собак, и, соответственно, нефропротекция. Если почки поражены незначительно, интоксикация начнет снижаться сразу после устранения патологии. Необходимо учитывать и основные факторы, без изменения которых положительные результаты окажутся под вопросом. Остановимся на них более подробно.
Послесловие
За годы работы мы выяснили, что большинство врачей в других клиниках неверно оценивают гемодиализ, считая его крайней мерой. Владельцы, «взращенные» на этом заблуждении, приходят к нам с формулировкой «все остальное не помогло» – и почти все обращения за лечением почечной недостаточности у собак и кошек случаются с опозданием, будь то острая или хроническая формы заболевания.
Уважаемые коллеги и владельцы животных! Бесполезно очищать почки, когда они уже мертвы. Гемодиализ – не волшебное средство, спасающее пациента в последнюю секунду. Назначенный своевременно, он дает врачу необходимые часы и дни для осуществления полноценной нефропротекции.
Допустим, у пациента полностью нарушена фильтрационная способность почек, например, с тотальным ОКН при пироплазмозе. Необходимо восстановить канальцевый эпителий – процесс, зачастую длящийся 15-20 дней. Несмотря на все наши капельницы, собака или кошка может элементарно не дожить до выздоровления, умерев от банальной уремии через неделю. Между тем, к нам часто попадают животные с мочевиной 90-100 и креатинином больше 2 500. Как правило, при таком уровне интоксикации в организме нарастают необратимые процессы системной дегенерации обмена веществ – и изменить что-то бывает уже невозможно.
Существует простой способ оценки эффективности терапии при почечной недостаточности у кошек и собак. В начале лечения у животного берется анализ крови на мочевину с креатинином. Повторите исследование не через 5-7 дней, как это обычно бывает, а через сутки, тогда вы точно будете знать, правильно ли выполнены назначения, все ли патологические факторы учтены. Если показатели растут, почка либо мертва, либо вы что-то упустили. Важно проводить исследования в одной лаборатории, чтобы исключить разницу погрешности измерений, которая скроет истинную суточную динамику.
Не залечивайте животное! Когда терапия назначена правильно, улучшение состояния пациента произойдет уже через 12 часов. Если этого не случилось, значит, упущен какой-то фактор, например, неверно определены степени обезвоживания или истощения, Ph плазмы крови, не учтены анемия, наличие сопутствующей инфекции, хронические заболевания и прочее. В этом случае тактику лечения нужно срочно менять.
Хроническая почечная недостаточность у собак и кошек – не диагноз. Это обязан знать каждый врач – и с этим знанием он должен подходить к каждому нефробольному. ХПН – это синдром, обусловленный гибелью нефронов в почке, который наблюдается от нескольких месяцев до нескольких лет. Причинами этого симптомокомплекса могут быть повышенное артериальное давление, хронический пиелонефрит, гидронефроз, нефросклероз, целый ряд аутоиммунных болезней, сахарный диабет и т.д. Иными словами, любые патологические факторы, приводящие к гибели нефронов, – истинная причина, следствием которой уже является ХПН. И ваша главная задача – находить и устранять их.
Современные возможности терапии хронического панкреатита
Хронический панкреатит — длительно протекающее воспалительное заболевание поджелудочной железы, проявляющееся необратимыми морфологическими изменениями, которые вызывают боль и/или стойкое снижение функции поджелудочной железы. При хроническом панкреатит
Хронический панкреатит — длительно протекающее воспалительное заболевание поджелудочной железы, проявляющееся необратимыми морфологическими изменениями, которые вызывают боль и/или стойкое снижение функции поджелудочной железы. При хроническом панкреатите морфологические изменения поджелудочной железы сохраняются после прекращения воздействия этиологического агента. В настоящее время распространенность хронического панкреатита, по данным аутопсий, составляет от 0,01 до 5,4%, в среднем — 0,3-0,4%, при этом за последние 40 лет заболеваемость выросла примерно в два раза, что связывают с тем, что население стало употреблять больше алкогольных напитков, а также с воздействием вредных факторов окружающей среды (см. диаграмму 1).
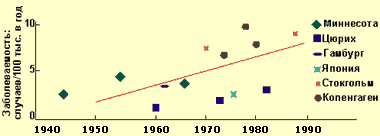 |
| Диаграмма 1. Заболеваемость ХП в 1945—1985 гг. (Worning H., 1990) |
В патогенезе хронического панкреатита важную роль играют несколько факторов. Одним из основных является обструкция главного панкреатического протока при конкрементах, воспалительном стенозе или опухолях. При алкогольном панкреатите повреждение поджелудочной железы связано с повышением содержания белка
в панкреатическом секрете, что приводит к возникновению белковых пробок и обструкции мелких протоков железы. Другим фактором, влияющим на патогенез алкогольного панкреатита, является изменение тонуса сфинктера Одди: его спазм вызывает внутрипротоковую гипертензию, а релаксация способствует рефлюксу дуоденального содержимого и внутрипротоковой активации панкреатических ферментов.
Разрушение экзокринной части поджелудочной железы вызывает прогрессирующее снижение секреции бикарбонатов и ферментов, однако клинические проявления нарушения переваривания пищи развиваются лишь при деструкции более 90% паренхимы органа. В первую очередь возникают проявления недостаточности липазы в виде нарушения всасывания жиров, жирорастворимых витаминов: A, D, E и K, что нечасто проявляется поражением костей, расстройствами свертывания крови. У 10–30% больных хроническим панкреатитом развивается сахарный диабет, обычно на поздних стадиях заболевания, нарушение толерантности в глюкозе наблюдается гораздо чаще. Для таких больных характерно развитие гипогликемических реакций на инсулин, недостаточное питание или злоупотребление алкоголем. Кетоацидоз развивается редко, что связано с одновременным снижением продукции инсулина и глюкагона.
Приступ хронического панкреатита проявляется иррадиирующими в спину болями в верхней половине живота, развивающимися после приема пищи, которые могут продолжаться в течение многих часов или нескольких дней. Нередко наблюдается тошнота, рвота, у 30–52% пациентов — снижение веса, у 16–33% — желтуха. Преходящая желтуха возникает вследствие отека железы при обострениях хронического панкреатита, постоянная — связана с обструкцией общего желчного протока вследствие фиброза головки поджелудочной железы. При разрывах протоков поджелудочной железы, на месте предыдущего некроза ткани происходит скопление секрета, что приводит к формированию псевдокист. Кисты могут быть бессимптомными или вызывать боли в верхней половине живота. При длительном течении заболевания, при уменьшении объема функционирующей паренхимы до 10% от нормы появляются признаки мальабсорбции (полифекалия, жирный стул, похудание).
В течении хронического панкреатита можно выделить несколько стадий (Lankisch P.G., Moessner Y.), умение различать которые важно для правильного подбора терапии. Так, на первой стадии заболевания клиническая симптоматика отсутствует: в этот период характерные для ХП изменения данных КТ или ЭРХПГ выявляются лишь при случайном обследовании.
На второй стадии возникают начальные проявления, характеризующиеся частыми эпизодами обострения ХП (которые могут быть ошибочно расценены как острый панкреатит). Заболевание видоизменяется от повторных приступов боли в животе до постоянных умеренных болей и похудания. С течением времени рецидивы становятся менее тяжелыми, но симптоматика сохраняется в периоды между приступами. На этой стадии может существенно ухудшаться качество жизни. Вторая стадия обычно продолжается на протяжении четырех—семи лет. Иногда заболевание быстро прогрессирует, развивается атрофия ПЖ, и нарушается функция органа.
У больных на третьей стадии постоянно присутствует симптоматика ХП, прежде всего — абдоминальная боль. Пациенты могут стать зависимыми от анальгетиков, значительно сокращают объем принимаемой пищи из-за опасения усиления боли. Появляются признаки экзокринной и эндокринной панкреатической недостаточности.
Особенность панкреатита на четвертой стадии — это атрофия ПЖ, развитие экзокринной и эндокринной недостаточности, что проявляется стеатореей, похуданием и сахарным диабетом. Снижается интенсивность боли, прекращаются острые приступы заболевания, могут развиваться тяжелые системные осложнения ХП и аденокарцинома поджелудочной железы.
Терапия панкреатита проводится по нескольким направлениям: отказ от употребления алкоголя; соблюдение диеты с низким содержанием жира (до 50–75 г/сут) и частым приемом небольших количеств пищи; купирование боли; ферментная заместительная терапия, борьба с витаминной недостаточностью; лечение эндокринных нарушений.
Лечение приступа хронического панкреатита, а также острого панкреатита проводиться по аналогичной схеме. Обязательные компоненты терапии: внутривенное введение растворов электролитов и коллоидов, голодная диета (полное голодание до двух дней) и анальгезия (например, меперидин). Рекомендуется введение свежезамороженной плазмы или альбумина. Диуретики не показаны большинству больных: олигурия разрешается при исчезновении гиповолемии и нормализации перфузии почек. Для облегчения рвоты, купирования пареза желудочно-кишечного тракта и уменьшения стимуляции поджелудочной железы может быть использована аспирация содержимого желудка через назогастральный зонд. Коагулопатия, возникающая при панкреатите, обычно требует назначения гепарина, свежей плазмы. В последние годы при остром панкреатите показана эффективность антагониста тромбоцит-активирующего фактора лексипафанта (60–100 мг/сут), однако его действие при хроническом панкреатите еще нуждается в уточнении.
Применение ингибиторов протеолитических ферментов (например, апротинина, габексата) является спорным. Исследования показывают, что при остром панкреатите не наблюдается дефицита ингибиторов протеаз, кроме того, проведенные клинические исследования не выявили преимуществ этих препаратов по сравнению с плацебо. Однако существуют данные, что габексат, низкомолекулярный ингибитор трипсина, эффективно используется для профилактики развития острого панкреатита, связанного с ЭРХПГ.
Ингибиторы секреции поджелудочной железы: глюкагон, соматостатин, кальцитонин, ингибиторы карбоангидразы, вазопрессин, изопреналин, также было предложено применять для лечения острого панкреатита, однако их эффективность к настоящему времени не получила достаточного подтверждения. Препараты пищеварительных ферментов можно использовать для лечения как в разгар заболевания с целью подавления панкреатической секреции, так и в период выздоровления, когда пациент снова получает возможность принимать пищу орально.
При билиарном обструктивном панкреатите должна быть проведена своевременная эндоскопическая декомпрессия желчных путей. Выполняется папиллосфинктеротомия, дилатация или стентирование панкреатического протока. Хирургическое лечение обструктивного панкреатита, безусловно, является основным методом, в то же время целесообразность проведения вмешательства в первые сутки после развития тяжелого приступа должна быть признана спорной. После стихания остроты воспаления целесообразно проведение холецистэктомии.
Схему длительной терапии при хроническом панкреатите можно разделить на две основные части, в соответствии с ведущими клиническими синдромами (см. диаграмму 2).
Боль могут облегчить большие дозы панкреатических ферментов. Попадание ферментов поджелудочной железы (прежде всего — трипсина) в двенадцатиперстную кишку по механизму отрицательной обратной связи вызывает снижение панкреатической секреции, снижение внутрипротокового давления и уменьшает боль. Традиционно для этой цели использовались порошок или таблетированные препараты панкреатина.
Если болевой синдром резистентен к терапии, при расширении главного протока более 8 мм, у 70–80% пациентов облегчение может принести латеральная панкреатоеюностомия. В случаях, когда панкреатический проток не расширен, показано проведение дистальной панкреатэктомии (при преимущественном поражении хвоста железы) или операция Уиппла (Whipple) (при поражении в основном головки железы). Альтернативой операции является чрезкожная денервация солнечного сплетения введением алкоголя, однако эффект этой процедуры сохраняется лишь в течение нескольких месяцев. Весьма перспективно эндоскопическое лечение под контролем эндоскопического УЗИ (дренирование псевдокист, невролиз солнечного сплетения).
Показаниями для заместительной терапии экзокринной панкреатической недостаточности являются исключительно клинические показатели: похудание, стеаторея, метеоризм. Классическая рекомендация, предусматривающая определение содержания жира в кале перед назначением лечения, в настоящее время потеряла свое значение из-за трудоемкости и низкой чувствительности данного метода. Для купирования внешнесекреторной панкреатической недостаточности используют различные препараты экстрактов поджелудочной железы (см. таблицу 1).
При выборе препарата для заместительной терапии следует учитывать следующие показатели:
Способность препарата активироваться только в щелочной среде — очень важное свойство, которое резко повышает эффективность ферментов; так, при использовании препарата, имеющего энтеросолюбильную оболочку, всасывание жиров повышается в среднем на 20% по сравнению с такой же дозой обычного средства. Однако при хроническом панкреатите происходит значительное снижение продукции бикарбонатов, что приводит к нарушению щелочной среды в двенадцатиперстной кишке. Это создает несколько проблем. Первая касается нарушения активации частиц ферментного препарата, покрытых энтеросолюбильной оболочкой. Вторая проблема заключается в том, что в кислой среде происходит преципитация желчных солей и нарушение эмульгации жира, что делает его малодоступным для расщепления липазой. Поэтому эффективность ферментной терапии (см. рисунок 1) может быть повышена благодаря одновременному назначению антацидов за 30 мин до и через 1 ч после еды или антисекреторных препаратов (Н2-блокаторы, омепразол), но необходимо помнить, что антациды, содержащие кальций или магний, ослабляют действие ферментных препаратов. Возможно использование препаратов, содержащих протеолитические ферменты растительного происхождения, которые сохраняют активность в гораздо более кислой среде, чем животные.
Значительное снижение качества жизни больного панкреатитом связано с такой проблемой, о которой обычно забывают, как стойкое вздутие живота. Нередко вздутие не купируется даже при приведении заместительной терапии высокими дозами ферментов. В этом случае к проводимой терапии необходимо добавить адсорбенты (симетикон, диметикон) или использовать комбинированные ферментные препараты, содержащие адсорбирующие вещества.
Разовая доза ферментов, которая рекомендуется для лечения внешнесекреторной панкреатической недостаточности, должна содержать не менее 20–40 тыс. ед. липазы. Обычно пациенту назначают две—четыре капсулы препарата (по 20—25 тыс. ед. липазы) при основных приемах пищи и по одной-две капсуле (по 8—10 тыс. ед. липазы) или таблетки панкреатина при употреблении небольшого количества пищи. При клинически выраженной панкреатической недостаточности обычно не удается полностью устранить стеаторею даже с помощью высоких доз препаратов, поэтому критериями адекватности подобранной дозы пищеварительных ферментов являются: прибавка веса, нормализация стула (менее трех раз в день), снижение вздутия живота.
Причины неэффективности заместительной терапии могут быть связаны как с неточной диагностикой заболевания, так и с неадекватным назначением терапии больному (см. рисунок 2).
Побочные эффекты ферментной терапии (см. рисунок 3) обычно не носят тяжелого характера, наиболее известный опасный побочный эффект — развитие фиброзирующей колопатии — возникает при длительном приеме очень высоких доз ферментов в виде микротаблеток: более 50 тыс. ед. липолитической активности на 1 кг веса тела в сутки.
Таким образом, терапия хронического панкреатита должна проводиться дифференцированно, в зависимости от ведущего клинического синдрома и стадии заболевания. Заболевание, которое удается обнаружить на первой стадии, как правило, не требует медикаментозной коррекции, в этом случае обычно достаточно изменения образа жизни и диетотерапии. Лечение ХП на второй стадии включает назначение таблетированного панкреатина, антисекреторных препаратов и спазмолитиков. Третья стадия обычно требует использования всего арсенала средств, которые имеются у врача для купирования панкреатической боли: микрогранулы панкреатина, антисекреторные препараты, октреотид, спазмолитики, мощные анальгетики, психотропные препараты. На последней, четвертой, стадии лечение основывается, прежде всего, на использовании микрогранул панкреатина в высокой дозе с целью проведения заместительной терапии.
По вопросам литературы обращайтесь в редакцию
А. В. Охлобыстин, кандидат медицинских наук
Э. Р. Буклис, кандидат медицинских наук
ММА им. И. М. Сеченова, Москва


