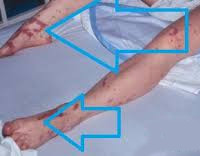
Бактериальный шок что это
Сепсис и септический шок: признаки и диагностика
Сепсис – это потенциально опасное для жизни состояние, вызванное реакцией организма на инфекцию. Организм обычно выделяет химические вещества в кровь для борьбы с инфекцией. Сепсис возникает, когда реакция организма на эти химические вещества нарушается, вызывая изменения, которые могут нарушить функцию многих органов.
Если сепсис переходит в септический шок, кровяное давление резко падает. Это может привести к смерти.
Сепсис вызывают инфекции и может случиться с кем угодно. Сепсис наиболее распространен и наиболее опасен для:
На ранних стадиях сепсис лечат с помощью антибиотиков и большого количества капельниц, повышающих шансы на выживание.
Признаки и симптомы сепсиса
Для постановки диагноза сепсис у вас должна быть вероятная или подтвержденная инфекция и все следующие признаки:
Признаки и симптомы септического шока
Когда обратиться к врачу
Чаще всего сепсис встречается у людей, которые госпитализированы или недавно были госпитализированы. Люди в отделении интенсивной терапии особенно уязвимы для развития инфекций, которые могут привести к сепсису. Если у вас появятся признаки и симптомы сепсиса после операции или после госпитализации, немедленно обратитесь за медицинской помощью.
Причины сепсиса
Хотя любой тип инфекции – бактериальная, вирусная или грибковая – может привести к сепсису, наиболее вероятные варианты:
Факторы риска
Сепсис и септический шок чаще встречаются:
Осложнения при сепсисе
По мере развития сепсиса нарушается кровоснабжение жизненно важных органов, таких как мозг, сердце и почки. Сепсис может вызвать образование тромбов в ваших органах, руках, ногах, пальцах рук и ног, что приводит к различной степени недостаточности органов и гибели тканей (гангрена).
Большинство людей выздоравливают от легкого сепсиса, но от септического шока смертность составляет около 40 процентов. Кроме того, эпизод тяжелого сепсиса может подвергнуть вас большему риску будущих инфекций.
Диагностика сепсиса
Врачи часто проводят несколько тестов, чтобы попытаться определить основную инфекцию.
Анализы крови
Образцы крови, взятые из двух разных участков, проверяются на:
Другие лабораторные исследования
В зависимости от ваших симптомов, ваш врач может также провести тестирование одной или нескольких из следующих биологических жидкостей:
Визуализация
Если место заражения неочевидно, ваш врач направит вас на один из следующих тестов:
Бактериальный шок. ДВС-синдром (конспект)
код для вставки на форум:
Необходимо повторить из курса биохимии систему гемостаза:
1. Стадии гемостаза.
2. Основные проявления сосудисто-тромбоцитарного гемостаза.
3. Стадии и основные проявления коагуляционного гемостаза.
4. Противосвертывающая система.
Для развития БШ необходимо по крайней мере два обязательных фактора:
Патогенез бактериального шока складывается из следующих процессов, быстро развивающихся в ответ на массивную инвазию бактериальных и тканевых токсинов, а также биологически активных аминов из первичного очага:
повреждение эндотелия преимущественно микроциркуляторного русла (МНР),
шоковые расстройства гемодинамики,
ДВС-синдром,
альтеративные изменения органов.
Шоковые расстройства гемодинамики проявляются в виде децентрализации кровотока с секвестрацией крови в МЦР, шунтировании кровотока. ДВС-синдром имеет острейшее течение с короткой фазой гиперкоагуляции, быстро сменяемой гипокоагуляцией, вследствие чего доминируют проявления геморрагического синдрома. Альтеративные (дистрофические и некротические) изменения носят полиорганный характер и обусловлены шоковыми расстройствами гемодинамики и ДВС-синдромом. В патогенезе БШ большое значение имеют также иммунные факторы, поступающие в кровоток медиаторы воспаления (гистамин, серотонин и др.), катехоламины, активация калликреин-кининовой системы и др.
Патологическая анатомия БШ
Патоморфологическая картина БШ складывается из следующих изменений:
3. ДВС-синдром при БШ характеризуется жидким состоянием крови, геморрагическим синдромом с множественными преимущественно диапедезными кровоизлияниями в различных органах и тканях, внутрисосудистой агрегацией форменных элементов крови (эритроцитов и тромбоцитов), образованием в МЦР отдельных нитей фибрина, предтромбов, преимущественно гиалиновых и глобулярных микротромбов.
Основные характеристики ДВС-синдрома: фазовые изменения гемостаза в виде гиперкоагуляции, сменяемой гипокоагуляцией; блокада МЦР агрегатами клеток крови и микротромбами; геморрагический синдром.
В детском возрасте ДВС-синдром может осложнять течение таких заболеваний, как асфиксия плода и новорожденного, болезнь гиалиновых мембран, гемолитическая болезнь новорожденных, инфекции, особенно вызванные грамотрицательной флорой и др.
Непосредственными причинами развития ДВС-синдрома при указанных заболеваниях и патологических состояниях могут выступать эндогенные и экзогенные факторы активации полисистемы гемостаза.
Эндогенные факторы: тканевой тромбопластйн, продукты распада тканей и клеток крови, лейкоцитарные протеазы, поврежденный эндотелий и др.
Экзогенные факторы: бактерии, вирусы, риккетсии, лекарственные препараты и др.
В основе развития ДВС-синдрома лежат следующие механизмы:
Указанные механизмы развития ДВС-синдрома находятся в тесной причинно-следственной связи, составляя суть определяемых лабораторно, клинически и морфологически стадий синдрома:
В настоящее время установлено также, что при осуществлении процессов внутрисосудистого свертывания крови в той или иной степени нарушается полимеризация фибрин-мономеров и образуется «заблокированный» фибриноген.
Механизмы образования последнего изучены недостаточно. Считается, что они связаны с активацией фибринолиза и других протеолитических систем. При этом происходит соединение полных и неполных фибрин-мономеров с фибриногеном, фибронектином, продуктами деградации фибриногена и фибрина(ПДФ), что приводит к образованию растворимых фибрин-мономерных комплексов (РФМК или продукты паракоагуляции). Возникновение «заблокированного» фибриногена лимитирует внутрисосудистое свертывание крови, так как, в частности, РФМК плохо коагулируют под влиянием тромбина и элиминируются из кровотока лейкоцитами и эндотелиальными клетками.
Процесс образования «заблокированного» фибриногена при ДВС-синдроме имеет достаточно большое значение, и возникновение гипокоагуляции крови вероятнее всего нельзя объяснять только коагулопатией потребления, как это делалось ранее.
В зависимости от продолжительности течения ДВС-синдром может быть острейшим (фаза гиперкоагуляции до нескольких минут, сменяется гипокоагуляцией), острым (развивается в течение 24 часов) и подострым развивается в течение нескольких дней с рецидивированием.
Морфологические изменения при ДВС-синдроме складываются из целого комплекса признаков, тесно переплетающихся с проявлениями основного заболевания и обусловленными пусковыми механизмами, длительностью процесса и лечебными мероприятиями. Среди всех морфологических признаков по степени диагностической ценности выделяют прямые и непрямые.
Наибольшую значимость имеют прямые признаки
— фибриновые образования, имеющие разнообразную структуру и являющиеся объективным морфологическим свидетельством активации свертывания крови:
— отдельные волокна и пучки фибрина, а также игловидные перекрещивающиеся волокна фибрина (предтромбы), построенные из нестабилизированного фибрина;
— выстилание слоем фибрина стенок сосудов, возникающее при повреждении последних преимущественно в зонах десквамации эндотелия;
— микротромбы, локализующиеся в основном в микроциркуляторном русле и имеющие разнообразный вид в зависимости от механизмов развития ДВС-синдрома:
— фибриновые микротромбы, построенные из стабилизированного фибрина и образующиеся при относительно медленном развитии процесса;
— гиалиновые микротромбы, возникающие при стремительном развитии процесса и состоящие из нестабилизированного фибрина и/или гемолизированных эритроцитов;
— глобулярные микротромбы, возникающие на почве нарушений кровообращения с агрегацией эритроцитов, последующим гемолизом и отложением окутывающего «тени» эритроцитов фибрина;
— тромбоцитарные, лейкоцитарные, эритроцитарные микротромбы, отражающие участие в фибринобразовании тех или иных форменных элементов крови, построены в основном из нестабилизированного фибрина;
— смешанные микротромбы из стабилизированного и нестабилизированного фибрина.
Морфологическая картина стадий ДВС-синдрома
Сравнение клинико-лабораторных данных и морфологических изменений позволило определить морфогенетическую картину развития ДВС-синдрома.
1-я и 2-я стадии ДВС-синдрома характеризуются появлением на фоне сосудистого поражения (набухание и десквамация эндотелия, плазматическое пропитывание, фибриноидное набухание и фибриноидный некроз) следующей картины изменений:
— агрегация тромбоцитов и эритроцитов вплоть до развития сладж-феномена (необратимая агрегация эритроцитов);
— развитие гемодинамических расстройств со спазмом артериальных сосудов и шунтированием кровотока;
— образование отдельных нитей и тяжей фибрина, предтромбов, единичных микротромбов.
На почве блокады сосудистого русла агрегатами форменных элементов крови, микротромбами и гемодинамических расстройств в 3-й, а затем в 4-й стадии ДВС-синдрома формируется разнообразная органная патология, чаще всего следующая:
— «шоковое легкое»: альвеолярный отек с кровоизлияниями, внутрисосудистая агрегация эритроцитов, микротромбоз, образование гиалиновых мембран;
— микротромбоз капилляров клубочков с некротическим нефрозом вплоть до образования симметричных кортикальных некрозов почек;
— кровоизлияния и некроз коры надпочечников (синдром Уотерхауза-Фридериксена);
— некроз аденогипофиза
— дистрофические изменения с рассеянными мелкоочаговыми некрозами и кровоизлияниями головного мозга, миокарда, печени, поджелудочной железы;
— кровоизлияния, эрозии и язвы желудочно-кишечного тракта.
Особенности ДВС-синдрома при гнойно-септических заболеваниях
При этих заболеваниях ДВС-синдром может быть по течению острейшим, острым, подострым.
Острейший ДВС-синдром наблюдается при септицемии и бактериальном шоке.
Процессы фибринобразования в МЦР зависят от выраженности поражения сосудистой стенки. При аллергических васкулитах (септицемия) определяются выстилание фибрином стенки сосудов, нити фибрина, предтромбы, единичные фибриновые микротромбы. Для бактериального шока характерны гиалиновые и глобулярные микротромбы. Во всех случаях выражен геморрагический синдром.
похожие статьи
Факторы неспецифической резистентности как возможные индикаторы развития и тяжести шока / Харин Г.М. // Матер. IV Всеросс. съезда судебных медиков: тезисы докладов. — Владимир, 1996. — №2. — С. 29.
Разрыв сердца при гнойном миокардите у малолетнего ребенка / Красильщик Д.З., Кобзарь Т.И. // Судебно-медицинская экспертиза. — М., 1968. — №2. — С. 49-50.
Инфекционно-токсический шок
Терминология
Следует сказать несколько слов о том, что такое шок вообще. Общепринятого определения не существует, зато в публикациях данной тематики часто цитируется крылатая фраза французского хирурга L.Deloyers:
«Шок легче распознать, чем описать, и легче описать, чем дать ему определение».
Тем не менее, смыслообразующими, критериальными признаками понятия «шок» практически все авторы признают следующее:
Причины
Симптоматика
Клиническая картина ИТШ определяется, в основном, двумя факторами: нарушения гемодинамики и общая интоксикация. Отмечается лихорадочное состояние на фоне высокой или очень высокой температуры, озноб, гипергидроз, интенсивная головная боль, боли в мышцах и/или суставах. Помрачается или утрачивается сознание, угнетаются функции центральной нервной системы. Артериальное давление резко падает. Типичны выраженные диспептические нарушения, олигурия или ишурия. При дальнейшей декомпенсации температура тела становится ниже нормальной, зачастую развивается эпилептиформные судороги, кожные покровы приобретают цианотичный оттенок.
В каждом конкретном случае, однако, имеются свои нюансы и специфические особенности: например, на первый план могут выйти симптомы печеночной, почечной, микроциркуляторной, сердечной, дыхательной недостаточности.
Диагностика
Несмотря на многообразие возможных симптомов, состояние больного, – обычно тяжелое или критическое, – по ряду вышеупомянутых ключевых критериев распознается как шоковое. Кроме анамнестических и клинических данных, при установлении диагноза решающей информативностью обладают результаты лабораторных анализов.
Следует отметить, что понятие «инфекционно-токсический шок» очень близко к понятию «септический шок», однако не является тождественным. Септический шок как крайняя выраженность клиники сепсиса всегда подразумевает присутствие патогена в крови, тогда как инфекционно-токсический шок может развиться и в тех ситуациях, когда болезнетворный микроорганизм не попал в системный кровоток (в отличие от циркулирующих токсинов) или уже эрадицирован антибиотиками.
Лечение
В целом, для подробного рассмотрения тактики купирования ИТШ нужна даже не отдельная статья, а отдельная книга.
Как показано выше, прогноз зависит от ряда факторов (конкретный возбудитель, возраст и тяжесть состояния пациента, своевременность оказания помощи и т.д.). Смертность колеблется в диапазоне примерно от 5 до 65 процентов.
Септический шок ( Инфекционно-токсический шок )
Септический шок – это тяжелое патологическое состояние, возникающее при массивном поступлении в кровь бактериальных эндотоксинов. Сопровождается тканевой гипоперфузией, критическим снижением артериального давления и симптомами полиорганной недостаточности. Диагноз ставится на основании общей клинической картины, сочетающей в себе признаки поражения легких, сердечно-сосудистой системы (ССС), печени и почек, централизации кровообращения. Лечение: массивная антибиотикотерапия, инфузия коллоидных и кристаллоидных растворов, поддержание деятельности ССС за счёт введения вазопрессоров, коррекция респираторных нарушений путем ИВЛ.
МКБ-10
Общие сведения
Септический шок (СШ) также называют инфекционно-токсическим (ИТШ). Как самостоятельная нозологическая единица патология впервые была описана в XIX веке, однако полноценное изучение с разработкой специфических противошоковых мер началось не более 25 лет назад. Может возникать при любом инфекционном процессе. Наиболее часто встречается у пациентов хирургических отделений, при менингококковой септицемии, брюшном тифе, сальмонеллезе и чуме. Распространен в странах, где диагностируется наибольшее количество бактериальных и паразитарных заболеваний (Африка, Афганистан, Индонезия). Ежегодно от ИТШ погибает более 500 тысяч человек по всему миру.
Причины
В абсолютном большинстве случаев патология развивается на фоне ослабления иммунных реакций. Это происходит у пациентов, страдающих хроническими тяжелыми заболеваниями, а также у людей пожилого возраста. В силу физиологических особенностей сепсис чаще диагностируется у мужчин. Список самых распространенных заболеваний, при которых могут возникать явления ИТШ, включает в себя:
Возбудитель сепсиса – грамположительные (стрептококки, стафилококки, энтерококки) и грамотрицательные (Enterobacter cloacae, Clostridium pneumoniae) бактерии. Во многих случаях культуры нечувствительны к антибиотикам, что затрудняет лечение пациентов. Септический шок вирусного происхождения в настоящее время вызывает споры специалистов. Одни представители научного мира утверждают, что вирусы неспособны стать причиной патологии, другие – что внеклеточная форма жизни может спровоцировать системную воспалительную реакцию, являющуюся патогенетической основой ИТШ.
Патогенез
В основе симптомов лежит неконтролируемое распространение медиаторов воспаления из патологического очага. При этом происходит активация макрофагов, лимфоцитов и нейтрофилов. Возникает синдром системного воспалительного ответа. На фоне этого снижается периферический сосудистый тонус, объем циркулирующей крови падает за счет повышения проницаемости сосудов и застоя жидкости в микроциркуляторном русле. Дальнейшие изменения обусловлены резким уменьшением перфузии. Недостаточное кровоснабжение становится причиной гипоксии, ишемии внутренних органов и нарушения их функции. Наиболее чувствителен головной мозг. Кроме того, ухудшается функциональная активность легких, почек и печени.
Помимо СВР в формировании септического шока важную роль играет эндогенная интоксикация. В связи со снижением работоспособности экскреторных систем в крови накапливаются продукты нормального обмена веществ: креатинин, мочевина, лактат, гуанин и пируват. Во внутренних средах повышается концентрация промежуточных результатов окисления липидов (скатол, альдегиды, кетоны) и бактериальных эндотоксинов. Всё это вызывает тяжелые изменения гомеостаза, расстройства кислотно-щелочного баланса, нарушения в работе рецепторных систем.
Классификация
Шоковое состояние классифицируется по патогенетическому и клиническому принципу. Патогенетически болезнь может быть «теплой» и «холодной». Тёплый шок характеризуется увеличением сердечного выброса на фоне снижения общего сосудистого тонуса, эндогенной гиперкатехоламинемией и расширением внутрикожных сосудов. Явления органной недостаточности выражены умеренно. Холодная разновидность проявляется снижением сердечного выброса, резким ослаблением тканевой перфузии, централизацией кровообращения и тяжелой ПОН. По клиническому течению септический шок подразделяется на следующие разновидности:
Публикации в СМИ
Шок септический
Cептический шок возможен при перитоните, инфекциях мочевыводящих и жёлчных путей, пневмонии, панкреонекрозе, септических родах и аборте. Чаще всего септический шок возникает в результате действия грамотрицательных бактерий ( Е. coli, Klebsiella, Proteus), но патогенными могут быть и другие агенты (грамположительные бактерии, вирусы, грибки, простейшие).
Патогенез • Изменения сосудистого русла имеют различную направленность (в зависимости от вида микроорганизмов, обусловивших септический шок) •• Грамположительная флора выделяет экзотоксины, вызывающие протеолиз и последующее образование плазмокининов. В рбзультате действия последних развиваются паралич сосудов и артериальная гипотензия по изоволемическому типу •• Грамотрицательная флора содержит эндотоксин, поступающий в кровь при разрушении бактерий. Стимулируя мозговой слой надпочечников, он приводит к выделению катехоламинов и последующему сужению сосудов • Нарушения сократительной функции миокарда при септическом шоке наступают на поздних сроках, в результате длительной коронарной недостаточности. Кроме прямого влияния токсинов на миокард, имеет значение сгущение крови, особенно значительное при перитоните и панкреонекрозе • Дыхательная недостаточность при септическом шоке обусловлена: •• синдромом шокового лёгкого, зависящего от нарушения микроциркуляции •• ухудшением сократимости дыхательных мышц •• несоответствием между функцией лёгких и возросшими требованиями к вентиляции (тахипноэ создаёт компенсаторный дыхательный алкалоз в ответ на избыточное образование органических кислот и угольной кислоты; гипервентиляция также связана с лихорадкой и прямым действием токсинов бактерий на дыхательный центр) • Печёночная недостаточность бывает обусловлена бактериемией, эндотоксемией, а также гипоперфузией и гипоксией органа. Истощаются фиксированные макрофаги (купферовские клетки), возникает портальная гипертензия • Нарушения реологии крови. С одной стороны, поражение печени приводит к уменьшению образования протромбина и повышению фибринолитической активности крови. С другой стороны, уровень фибриногена в крови остаётся высоким, а уровень эндогенного гепарина снижается. Поэтому гиперкоагуляция сохраняется и создаются условия для возникновения ДВС • Почечная недостаточность при септическом шоке возникает в результате гиперкоагуляции. Быстро развиваются необратимые изменения, вплоть до массивного тубулярного некроза • Повреждения поджелудочной железы имеют ишемическое происхождение. Вначале происходит активация секреторной функции с выбросом в кровоток протеолитических ферментов. На поздних сроках возможен асептический панкреонекроз. Дисфункция поджелудочной железы вызывает: •• гипергликемию •• избыточное образование кининов (протеазы поджелудочной железы трансформируют неактивные кининогены в активные кинины), кинины вызывают повышение проницаемости сосудистой стенки и снижают АД •• геморрагический гастроэнтероколит (в результате повышенной секреции протеаз в просвет кишечника и застоя крови в брыжейке) • Возникает вторичный иммунодефицит.
• Симптомы инфекции: гипертермия, ознобы, бактериемия, изменения белой и красной крови.
• Нервно-психические расстройства: возбуждение, судороги, сопор, кома.
• Сердечно-сосудистые расстройства: артериальная гипотензия, нарушения ритма, ишемия миокарда. Нарушения микроциркуляции: •• при гипердинамическом синдроме кожные покровы тёплые, сухие, гиперемированные •• при гиподинамическом синдроме — холодная, влажная, мраморная с цианозом кожа.
• Дыхательные расстройства: тахипноэ, гипоксемия, низкий артериовенозный градиент рО2.
• Нарушения функций паренхиматозных органов: •• олигурия (менее 600–700 мл/сут), гиперазотемия, гиперкреатининемия •• желтуха, повышение активности трансаминаз •• диастазурия, гиперамилаземия, гипергликемия.
• Тромбогеморрагический синдром, в т.ч. желудочно-кишечные кровотечения.
• Лабораторные данные: коагулопатия, нарушения КЩР (респираторный алкалоз, метаболический ацидоз), нарушение водно-электролитного баланса, диспротеинемия.
Лечение • Хирургическое лечение очагов инфекции • Коррекция расстройств гемодинамики • Обеспечение адекватной лёгочной вентиляции и газообмена: масочная ингаляция 100% кислорода, если при этом р a О2 не превышает 60–70 мм рт.ст. — ИВЛ • Восполнение потерь жидкости, парентеральное питание, коррекция КЩР и электролитных нарушений •• Суточный объём инфузии определяют дефицитом ОЦК •• Инфузии альбумина и протеина — при шоковом лёгком •• Белковые и аминокислотные инфузии (обеспечение не менее 4000 ккал) •• Жировые эмульсии не показаны из-за опасности блокады ретикулоэндотелиальной системы • Коррекция метаболических нарушений • При олигурии на фоне достаточного ОЦК — фуросемид (по 100–200 мг в/м или в/в дробно через каждые 4 ч) в сочетании с осмотическими диуретиками (маннитол 1 г/кг в/в капельно) • Лечение пареза кишечника •• Стимуляция моторики кишечника (гипертонические клизмы, диадинамические токи Бернара) • • Неостигмина метилсульфат (1 мл 0,05% р-ра п/к 2 р/сут), дистигмина бромид (1 мл 0,05% р-ра в/м 1 р/сут) • Антистафилококковый иммуноглобулин в/м через день до 4 доз, антистафилококковая плазма в/в, иммуноглобулин человеческий нормальный (IgG+IgA+IgM), иммуноглобулин человеческий нормальный, моноклональные АТ • Антибиотикотерапия •• Препараты выбора — пенициллины, аминогликозиды, цефалоспорины, карбапенемы, производные фторхинолона в больших дозах (например, гентамицин — до 240–400 мг/сут, цефалоспорины — до 12 г/сут) • • Для профилактики суперинфекции противогрибковые препараты (нистатин 500 000 ЕД 3–4 р/сут, леворин 500 000 ЕД 2–4 р/сут), амфотерицин В, флуконазол, бифидобактерии бифидум, бифиформ.
Синонимы • Токсико-инфекционный шок • Эндотоксиновый xe «Шок:эндотоксиновый» шок • Бактериемический шок • Инфекционно-токсический xe «Шок:инфекционно-токсический» шок
МКБ-10 • A48. 3 Синдром xe «Синдром:токсического шока» токсического шока
Код вставки на сайт
Шок септический
Cептический шок возможен при перитоните, инфекциях мочевыводящих и жёлчных путей, пневмонии, панкреонекрозе, септических родах и аборте. Чаще всего септический шок возникает в результате действия грамотрицательных бактерий ( Е. coli, Klebsiella, Proteus), но патогенными могут быть и другие агенты (грамположительные бактерии, вирусы, грибки, простейшие).
Патогенез • Изменения сосудистого русла имеют различную направленность (в зависимости от вида микроорганизмов, обусловивших септический шок) •• Грамположительная флора выделяет экзотоксины, вызывающие протеолиз и последующее образование плазмокининов. В рбзультате действия последних развиваются паралич сосудов и артериальная гипотензия по изоволемическому типу •• Грамотрицательная флора содержит эндотоксин, поступающий в кровь при разрушении бактерий. Стимулируя мозговой слой надпочечников, он приводит к выделению катехоламинов и последующему сужению сосудов • Нарушения сократительной функции миокарда при септическом шоке наступают на поздних сроках, в результате длительной коронарной недостаточности. Кроме прямого влияния токсинов на миокард, имеет значение сгущение крови, особенно значительное при перитоните и панкреонекрозе • Дыхательная недостаточность при септическом шоке обусловлена: •• синдромом шокового лёгкого, зависящего от нарушения микроциркуляции •• ухудшением сократимости дыхательных мышц •• несоответствием между функцией лёгких и возросшими требованиями к вентиляции (тахипноэ создаёт компенсаторный дыхательный алкалоз в ответ на избыточное образование органических кислот и угольной кислоты; гипервентиляция также связана с лихорадкой и прямым действием токсинов бактерий на дыхательный центр) • Печёночная недостаточность бывает обусловлена бактериемией, эндотоксемией, а также гипоперфузией и гипоксией органа. Истощаются фиксированные макрофаги (купферовские клетки), возникает портальная гипертензия • Нарушения реологии крови. С одной стороны, поражение печени приводит к уменьшению образования протромбина и повышению фибринолитической активности крови. С другой стороны, уровень фибриногена в крови остаётся высоким, а уровень эндогенного гепарина снижается. Поэтому гиперкоагуляция сохраняется и создаются условия для возникновения ДВС • Почечная недостаточность при септическом шоке возникает в результате гиперкоагуляции. Быстро развиваются необратимые изменения, вплоть до массивного тубулярного некроза • Повреждения поджелудочной железы имеют ишемическое происхождение. Вначале происходит активация секреторной функции с выбросом в кровоток протеолитических ферментов. На поздних сроках возможен асептический панкреонекроз. Дисфункция поджелудочной железы вызывает: •• гипергликемию •• избыточное образование кининов (протеазы поджелудочной железы трансформируют неактивные кининогены в активные кинины), кинины вызывают повышение проницаемости сосудистой стенки и снижают АД •• геморрагический гастроэнтероколит (в результате повышенной секреции протеаз в просвет кишечника и застоя крови в брыжейке) • Возникает вторичный иммунодефицит.
• Симптомы инфекции: гипертермия, ознобы, бактериемия, изменения белой и красной крови.
• Нервно-психические расстройства: возбуждение, судороги, сопор, кома.
• Сердечно-сосудистые расстройства: артериальная гипотензия, нарушения ритма, ишемия миокарда. Нарушения микроциркуляции: •• при гипердинамическом синдроме кожные покровы тёплые, сухие, гиперемированные •• при гиподинамическом синдроме — холодная, влажная, мраморная с цианозом кожа.
• Дыхательные расстройства: тахипноэ, гипоксемия, низкий артериовенозный градиент рО2.
• Нарушения функций паренхиматозных органов: •• олигурия (менее 600–700 мл/сут), гиперазотемия, гиперкреатининемия •• желтуха, повышение активности трансаминаз •• диастазурия, гиперамилаземия, гипергликемия.
• Тромбогеморрагический синдром, в т.ч. желудочно-кишечные кровотечения.
• Лабораторные данные: коагулопатия, нарушения КЩР (респираторный алкалоз, метаболический ацидоз), нарушение водно-электролитного баланса, диспротеинемия.
Лечение • Хирургическое лечение очагов инфекции • Коррекция расстройств гемодинамики • Обеспечение адекватной лёгочной вентиляции и газообмена: масочная ингаляция 100% кислорода, если при этом р a О2 не превышает 60–70 мм рт.ст. — ИВЛ • Восполнение потерь жидкости, парентеральное питание, коррекция КЩР и электролитных нарушений •• Суточный объём инфузии определяют дефицитом ОЦК •• Инфузии альбумина и протеина — при шоковом лёгком •• Белковые и аминокислотные инфузии (обеспечение не менее 4000 ккал) •• Жировые эмульсии не показаны из-за опасности блокады ретикулоэндотелиальной системы • Коррекция метаболических нарушений • При олигурии на фоне достаточного ОЦК — фуросемид (по 100–200 мг в/м или в/в дробно через каждые 4 ч) в сочетании с осмотическими диуретиками (маннитол 1 г/кг в/в капельно) • Лечение пареза кишечника •• Стимуляция моторики кишечника (гипертонические клизмы, диадинамические токи Бернара) • • Неостигмина метилсульфат (1 мл 0,05% р-ра п/к 2 р/сут), дистигмина бромид (1 мл 0,05% р-ра в/м 1 р/сут) • Антистафилококковый иммуноглобулин в/м через день до 4 доз, антистафилококковая плазма в/в, иммуноглобулин человеческий нормальный (IgG+IgA+IgM), иммуноглобулин человеческий нормальный, моноклональные АТ • Антибиотикотерапия •• Препараты выбора — пенициллины, аминогликозиды, цефалоспорины, карбапенемы, производные фторхинолона в больших дозах (например, гентамицин — до 240–400 мг/сут, цефалоспорины — до 12 г/сут) • • Для профилактики суперинфекции противогрибковые препараты (нистатин 500 000 ЕД 3–4 р/сут, леворин 500 000 ЕД 2–4 р/сут), амфотерицин В, флуконазол, бифидобактерии бифидум, бифиформ.
Синонимы • Токсико-инфекционный шок • Эндотоксиновый xe «Шок:эндотоксиновый» шок • Бактериемический шок • Инфекционно-токсический xe «Шок:инфекционно-токсический» шок
МКБ-10 • A48. 3 Синдром xe «Синдром:токсического шока» токсического шока