дыши во мгле что за болезнь у девочки
Синдром Стимбергера – как проявляется тяжелый комбинированный иммунодефицит, и как сохранить жизнь ребенку?
Все новорожденные дети изначально имеют защиту от инфекций и вирусов благодаря иммунитету, полученному от матери. Дальнейшее развитие и совершенствование защитной системы происходит в первые месяцы жизни. В случае если иммунитет не справляется, говорят об иммунодефиците. Подобным нарушением сопровождается синдром Стимбергера.
Болезнь Стимбергера – что это?
Синдром Стимбергера – это сложный симптомокомплекс, основным признаком которого является выраженный иммунодефицит. Связано это с уменьшением общего количества Т- и В-лимфоцитов. Эти специализированные лейкоциты образуются в костном мозге и защищают организм от различных инфекций. Резкое снижение их концентрации, алимфоцитоз, отрицательно отражается на работе иммунной системы, в результате чего развиваются заболевания. Характерный признак – частые инфекции, развивающиеся уже с первых дней жизни. Синонимичным названному является синдром Гланцмана-Риникера.
Тяжелый комбинированный иммунодефицит – причины, этиология
Болезнь Стимбергера представляет собой тяжелый иммунодефицит комбинированного типа. Причиной его развития специалисты нередко называют мутации в генах. При этом возможно нарушение строения как одновременно нескольких генных единиц, так и одной. Такие патологии передаются по наследству. В большинстве случаев наследование происходит по аутосомно-рецессивному типу. Специалисты не исключают возможности развития синдрома и после рождения, в старшем возрасте. Среди факторов, способствующих развитию нарушения, выделяют:
ТКИД – симптомы
Болезнь Стинбергера проявляется в раннем возрасте. Первые подозрения на патологию могут возникнуть уже на 6-м месяце жизни малыша. У пациентов с ТКИД часто развиваются кандидоз, персистирующие вирусные инфекции, пневмонии, нарушение пищеварения, сопровождающееся диареей. При аппаратном обследовании пациентов диагностируют малые размеры тимуса, лимфоидная ткань имеет малый объем или полностью отсутствует. Синдром Стимбергера требует своевременной диагностики и лечения. В противном случае существует риск гибели ребенка в младенческом возрасте.
Тяжелый комбинированный иммунодефицит – диагностика
Разобравшись, что такое синдром Стимбергера и как проявляется, назовем основные методы диагностики. Заболевание нередко именуют вторым названием – «синдром мальчика в пузыре». Обусловлено это тем, что ребенок постоянно вынужден находиться в изоляции, в специальных условиях. Частые контакты с людьми повышают риск инфицирования.
Чтобы вовремя предотвратить прогрессирование синдрома Стимбергера, нормализовать работу иммунной системы, необходима правильная диагностика. Заподозрить диагноз тяжелый комбинированный иммунодефицит мамы могут по частому развитию в организме:
При наличии названных признаков назначают комплексное обследование пациента, которое включает исследование образца крови. Врачи определяют концентрацию В- и Т-лимфоцитов. Непосредственно снижение их уровня указывает на иммунодефицит. С целью установления причины тяжёлой иммунной недостаточности может назначаться молекулярно-генетическое исследование.
ТКИД – лечение
Тяжелый комбинированный иммунодефицит трудно поддается терапии. При выявлении патологии терапевтические мероприятия направлены на нормализацию работы иммунной системы. Для исключения инфицирования все пациенты изолируются в отдельные боксы. Лечение зачастую включает использование антибактериальных препаратов, противогрибковых средств.
Однако медикаментами зачастую не удается нормализовать иммунную систему пациента. Поддерживающая терапия с применением внутривенного введения иммуноглобулина (ВВИГ) является временным решением. Для полного избавления от недуга требуется проведение трансплантации стволовых клеток костного мозга.
ТКИД – лечение без операции
ТКИД – болезнь, требующая комплексного подхода. Лекарства, используемые при заболевании, направлены на стимуляцию работы иммунной системы, защиту организма от инфекций. Эффективность этих методов обусловлена выраженностью нарушения и временем его обнаружения. Как показывают наблюдения специалистов, данные мероприятия являются временной мерой. Чтобы полностью вылечить заболевание, требуется пересадка костного мозга.
Тяжелый комбинированный иммунодефицит – операция
Около 90 % пациентов с патологией нуждаются в проведении трансплантации клеток костного мозга. Операция ТГСК (трансплантация гемопоэтических стволовых клеток) требует длительной подготовки. Для ее осуществления требуется произвести подбор донора по лейкоцитарной культуре. Для трансплантации используется материал от родственников. Проведение операции сопровождается высоким риском развития осложнений в будущем. Однако, по наблюдениям специалистов, осуществление хирургического вмешательства в период до 3 месяцев жизни в 96 % случаев дает положительный эффект.
ТКИД – прогноз
При отсутствии терапии дети с врожденной формой ТКИД погибают в течение 1–2 лет жизни. Однако операция по трансплантации костного мозга помогает малышам справиться с недугом. Взрослые люди с ТКИД вынуждены на протяжении всей жизни следить за своим здоровьем, избегать инфекций. Прогноз для таких пациентов напрямую зависит от степени выраженности патологического состояния, времени его обнаружения, грамотности проводимых терапевтических мероприятий. Пациенты с тяжёлым комбинированным иммунодефицитом погибают раньше, чем их здоровые сверстники, в целом на 10–15 лет.
Что такое синдром Стимбергера? О нем говорят в фильме «Дыши во мгле», но гугл ничего не даёт.
Тяжёлый комбинированный иммунодефицит
Тяжёлый комбинированный иммунодефицит, (англ. SCID, также алимфоцитоз, синдром Глянцмана-Риникера, синдром тяжёлого комбинированного иммунодефицита, и тимическая алимфоплазия [1]) — это генетическое заболевание, при котором в результате дефекта одного из генов нарушается работа компонентов адаптивной иммунной системы B- и T-лимфоцитов. Тяжёлый комбинированный иммунодефицит — это тяжёлая форма наследственного иммунодефицита, который также известен как синдром мальчика в пузыре, так как больные крайне уязвимы перед инфекционными болезнями и вынуждены находиться в стерильной среде. Одним из таких больных был Дэвид Веттер. Тяжёлый комбинированный иммунодефицит является результатом настолько сильного повреждения иммунной системы, что последняя считается практически отсутствующей.
Симптомами тяжёлого комбинированного иммунодефицита могут являться хроническая диарея, ушные инфекции, возвратный пневмоцистоз, обильные кандидозы полости рта. Без лечения, в случае, если не было произведено успешной трансплантации гемопоэтических стволовых клеток, дети обычно умирают в течение первого года жизни от тяжёлых рецидивирующих инфекций.
Синдром «запертого человека» (синдром изоляции, синдром деэфферентации) (англ. locked-in syndrome) — синдром, который характеризуется отсутствием адекватной реакции больного на внешние, в том числе и словесные, стимулы из-за тетраплегии и паралича бульбарной, мимической и жевательной мускулатуры.
Он проявляется полной потерей речи (афазия), параличом при полной сохранности сознания и чувствительности. При нём возможно общение с окружающими путём мигания и движения глаз. При длительном сохранении синдрома «запертого человека» больные могут быть обучены передавать глазами достаточно сложную информацию.
Причинами развития синдрома могут быть инфаркт основания мозга, инфаркт основания среднего мозга, кровоизлияние в мозг, центральный понтинный миелинолиз, синдром Гийена-Барре, полиомиелит, миастения, пароксизмальная миоплегия, некоторые яды.
Бывает, что при таком синдроме медицинский персонал, ошибочно диагностировав кому (утрату сознания), в присутствии больного свободно обсуждает все профессиональные вопросы, в том числе и вероятность смерти больного, что может нанести ему тяжелую психическую травму.
Я НАШОЛ ЧТО ЕТО
Тяжёлый комбинированный иммунодефицит, (англ. SCID, также алимфоцитоз, синдром Глянцмана-Риникера, синдром тяжёлого комбинированного иммунодефицита, и тимическая алимфоплазия [1]) — это генетическое заболевание, при котором в результате дефекта одного из генов нарушается работа компонентов адаптивной иммунной системы B- и T-лимфоцитов. Тяжёлый комбинированный иммунодефицит — это тяжёлая форма наследственного иммунодефицита, который также известен как синдром мальчика в пузыре, так как больные крайне уязвимы перед инфекционными болезнями и вынуждены находиться в стерильной среде. Одним из таких больных был Дэвид Веттер. Тяжёлый комбинированный иммунодефицит является результатом настолько сильного повреждения иммунной системы, что последняя считается практически отсутствующей.
Симптомами тяжёлого комбинированного иммунодефицита могут являться хроническая диарея, ушные инфекции, возвратный пневмоцистоз, обильные кандидозы полости рта. Без лечения, в случае, если не было произведено успешной трансплантации гемопоэтических стволовых клеток, дети обычно умирают в течение первого года жизни от тяжёлых рецидивирующих инфекций.
Эпилепсия без судорог у детей
Поделиться:
Эпилепсия — это заболевание, связанное с нарушением работы определенных групп нервных клеток. Эпилепсия может быть врожденной и приобретенной. Иногда она начинается из-за повреждения головного мозга в результате травмы или опухоли. Также ее причиной может стать врожденная киста или другие особенности мозгового строения. Бывает, что эпилептические приступы начинают происходить без видимых причин на фоне наследственной предрасположенности.
Эпилепсия у детей может проявляться судорогами всего тела или одной конечности, а также эпизодами «выключения».
Бессудорожные приступы эпилепсии у детей
Эпилептические приступы с судорогами больше характерны для малышей с рождения до 2–3 лет. У детей старше 4–5 лет чаще бывают эпилептические приступы без судорог.
Наиболее частый бессудорожный приступ — это абсанс, кратковременное выключение сознания. Со стороны это выглядит как будто ребенок «завис», задумался. Взгляд не сосредоточен. Во время приступа малыш прекращает деятельность (например, игру, ходьбу, письмо) и замирает. При этом он может выполнять стереотипные движения (например, сгибание-разгибание пальцев).
Во время приступа ребенок ни на что не реагирует, его невозможно вывести из этого состояния. Спустя несколько секунд (обычно от 2 до 20) приступ завершается, ребенок снова «включается» и продолжает то, что он делал до приступа. Сам приступ не помнит.
Таких абсансов может быть несколько десятков в день. Обычно приступ провоцируется гипервентиляцией, вызванной частым вдохами. Абсансы долгое время могут оставаться незамеченными даже близкими родственниками ребенка.
Если вы замечаете, что ваш малыш часто замирает во время игры, понаблюдайте за ним повнимательнее. При любых сомнениях лучше ничего не дожидаться, а как можно быстрее посетить вместе с малышом детского невролога.
Чем опасна эпилепсия в детском возрасте
Эпилептические приступы (даже если они протекают без судорог), особенно частые (несколько раз в день), мешают нормальной работе головного мозга и в дальнейшем нарушают развитие нервной системы ребенка. Такие дети могут отставать от сверстников в развитии.
Для эпилепсии, особенно начавшейся в детском возрасте, характерны особые изменения личности. Эти изменения связаны не только с приступами, но и с принимаемыми лекарствами, отношением окружающих. С возрастом у людей, страдающих эпилепсией, появляется раздражительность, излишняя обстоятельность, замедленность мышления.
Читайте также:
Мигрень у ребенка
Важно, что приступы эпилепсии у детей могут скрываться за непонятными головными болями или болями в животе, обмороками, рвотой и другими симптомами. Это значительно затрудняет установление диагноза.
Обследование
Если вы подозреваете у своего ребенка эпилепсию без судорог, то необходимо посетить детского невролога.
Не стоит откладывать визит к доктору, если у ребенка непонятные головные боли или боли в животе, внезапные изменения настроения (например, агрессивность). Эти симптомы тоже могут быть редкими проявлениями эпилепсии в детском возрасте.
При подозрении на эпилепсию врач обычно направляет ребенка на электроэнцефалограмму (ЭЭГ). В зависимости от результатов ЭЭГ может потребоваться видео ЭЭГ-мониторинг, магнитно-резонансная томография и другие исследования. Окончательный диагноз эпилепсии обычно устанавливает невролог-эпилептолог.
Лечение
Лечение назначает врач-эпилептолог. При бессудорожных приступах часто применяют этосуксимид, карбамазепин (антиконвульсанты), при необходимости — ламотриджин. Врач подбирает препарат и дозу индивидуально. Будьте внимательны и точно соблюдайте рекомендации. Замена дозы или пропуск лекарства может привести к обострению болезни!
Эпилептические припадки, которые начались в детстве, обычно хорошо поддаются лечению и нередко полностью проходят с возрастом. Поэтому особенно важно вовремя обратиться к врачу и выполнять все рекомендации.
Фарингит
Фарингит – это воспалительный процесс, который образуется на задней стенке гортани и поражает слизистую оболочку, а также более глубокие слои, ткани мягкого нёба и лимфатические узлы. Острая форма фарингита может перерасти в хроническую, если пациент не обращается за помощью к врачу и занимается самолечением.
Так как патологический процесс в гортани вызван распространением болезнетворных бактерий, риск развития фарингита повышается у людей со слабой иммунной системой и у тех, кто страдает ЛОР-заболеваниями или имеет к ним предрасположенность.
Чем опасен фарингит и как он проявляет себя? К какому врачу обращаться и как лечить заболевание? На эти и другие вопросы мы ответим в данной статье.
Причины развития фарингита
Специалисты полагают, что пик развития патологии приходится на конец зимы и начало весны, так как в это время иммунная система человека особо подвержена простудным заболеваниям. Часто в весеннее время года недостаток витаминов и микроэлементов в организме человека приводит к появлению авитаминоза, организм ослабевает и создает прекрасную среду для развития болезнетворных бактерий. Также возможны воспалительные процессы: как отдельно, так и на фоне основного заболевания.
Первые признаки наличия фарингита и его дальнейшее лечение могут отличаться в зависимости от стадии патологии, пола, возраста и общего состояния здоровья пациента.
К основным причинам развития фаринголарингита мы относим:
Симптомы фарингита
Острый фарингит
Острые фарингиты могут протекать самостоятельно, а также сопровождаться острыми воспалениями, охватывающими верхние дыхательные пути: ринитами или воспалениями слизистых носоглотки.
В зависимости от причины развития острый фарингит бывает:
Хронический фарингит
По глубине поражения слизистой оболочки глотки хронический фарингит различается на: катаральную, гипертрофическую и атрофическую формы.
Любой вид хронического фарингита развивается по причине того, что острая форма заболевания не была излечена вовремя и переросла в более серьезную форму. А также хронические фарингиты появляются как следствие ринитов, гайморитов, искривления носовой перегородки, полипов в носу – то есть когда длительное время затруднено носовое дыхание. Кроме того, длительное применение сосудосуживающих капель также приводит к появлению хронического фарингита.
Как проявляется и протекает фарингит у детей?
Фарингиты дети переносят тяжелее, чем взрослые. Особенно это относится к малышам до года. Отек слизистой может вызвать признаки удушья, боль, которая сопровождает заболевание, снижает аппетит у ребенка. Зачастую температура тела у малыша может достигать 40°. Самое сложное в этой ситуации то, что маленький ребенок не может сказать, что у него болит.
Неправильное лечение может привести к непоправимым последствиям для маленького неокрепшего организма. Поэтому при первых признаках фарингита, сразу же обращайтесь к врачу.
Ангина и фарингит: в чем разница?
Общее состояние пациента при острой форме ангины или тонзиллита можно спутать с симптомами фарингита. Если заболевание диагностировано неправильно, то лечение фарингита у взрослых не даст никакого эффекта. И острая форма патологии может перерасти в хроническую.
К сожалению, многие пациенты занимаются самолечением и начинают применять препараты без специального назначения врача. Это делать крайне противопоказано! Лучше вовремя позаботьтесь о своем здоровье и обратитесь за помощью к опытному отоларингологу.
Важно помнить, что во время фарингита воспаляется гортань, а при ангине – гланды. Во время ангины всегда больно глотать, болевые ощущения усиливаются еще больше при употреблении пищи. При фарингите происходит наоборот – во время поедания теплой пищи или теплых напитков боль в горле уменьшается.
Во время развития ангины нет кашля или першения, только боль в горле и иногда образование белого налета. При фарингите присутствует першение, а также шум, боль или заложенность в ушах. Трудность в различие этих двух заболеваний еще осложняется тем, что у одного пациента одновременно могут развиваться обе патологии, так как они вызваны одним возбудителем.
Диагностика фарингита
Обнаружение всех видов фарингита начинается с визуального осмотра гортани при помощи специального прибора и сборе анамнеза. Также для изучения берется мазок из зева – на дифтерию.
Другие виды диагностики:
В зависимости от симптомов заболевания, а также состояния гортани, наличия или отсутствия кашля, лихорадки, налета на миндалинах и болезненности и увеличенном размере лимфатических узлов, может понадобиться дополнительно консультации других узких специалистов: эндокринолога, кардиолога, аллерголога.
Методы лечения фарингита
Лечение должно проходить в комплексе. Пациенту прописываются медикаменты, которые снимут боль и уберут воспаление. А также важно придерживаться специальной диеты и исключить из рациона продукты, которые раздражают слизистую оболочку горла и приносят еще больше дискомфорта: алкогольная продукция, острая и соленая пища, кислые блюда, газированные напитки.
Медикаментозная терапия
В зависимости от клинической картины и общего состояния пациента, врач может прописать антигистаминные, противокашлевые и противовирусные медикаменты. Используются таблетки/пастилки для рассасывания, которые снимают боль.
В некоторых случаях прибегают к использованию антибиотиков. Их можно принимать только по наставлению врача.
Местное воздействие
Также хорошее действие на воспалительный процесс и покраснение гортани оказывают полоскания специальными растворами. Они мягко воздействуют, снимают боль и улучшают общее состояние пациента.
Для диагностики и выявления заболевания нужна консультация отоларинголога. В городской поликлинике можно обратиться к своему лечащему терапевту, который выпишет направление к ЛОРу. Однако на это требуется время. Часто своей записи к врачу приходится ждать по 2 недели. В некоторых случаях это просто невозможно, так как нужно быстрее провести обследование и назначить лечение, пока ситуация не стала критической.
Поэтому мы рекомендуем обращаться в медицинскую клинику «Медюнион». У нас работают практикующие отоларингологи, записи к которым не нужно ждать несколько недель. Запишитесь уже сегодня на удобное для вас время, и уже завтра пройдите обследование.
Пациенты выбирают нас за то, что мы оказываем услугу выезда узкого специалиста на дом в случае, если самостоятельно прибыть в клинику вы не можете. Прямо на дому можно также провести забор анализов.
Стоимость первичной консультации отоларинголога в Красноярске в клинике «Медюнион» от 1300 рублей. Записаться можно на сайте или по телефону 201-03-03.
Тики у детей
Тики, или гиперкинезы, — это повторяющиеся неожиданные короткие стереотипные движения или высказывания, внешне схожие с произвольными действиями. Характерной чертой тиков является их непроизвольность, но в большинстве случаев пациент может воспроизводить
Тики, или гиперкинезы, — это повторяющиеся неожиданные короткие стереотипные движения или высказывания, внешне схожие с произвольными действиями. Характерной чертой тиков является их непроизвольность, но в большинстве случаев пациент может воспроизводить или частично контролировать собственные гиперкинезы. При нормальном уровне интеллектуального развития детей заболеванию нередко сопутствуют когнитивные нарушения, двигательные стереотипии и тревожные расстройства.
Распространенность тиков достигает приблизительно 20% в популяции.
До сих пор не существует единого мнения о возникновении тиков. Решающая роль в этиологии заболевания отводится подкорковым ядрам — хвостатому ядру, бледному шару, субталамическому ядру, черной субстанции. Подкорковые структуры тесно взаимодействуют с ретикулярной формацией, таламусом, лимбической системой, полушариями мозжечка и корой лобного отдела доминантного полушария. Деятельность подкорковых структур и лобных долей регулируется нейромедиатором дофамином. Недостаточность работы дофаминергической системы приводит к нарушениям внимания, недостаточности саморегуляции и поведенческого торможения, снижению контроля двигательной активности и появлению избыточных, неконтролируемых движений.
На эффективность работы дофаминергической системы могут повлиять нарушения внутриутробного развития вследствие гипоксии, инфекции, родовой травмы или наследственная недостаточность обмена дофамина. Имеются указания на аутосомно-доминантный тип наследования; вместе с тем известно, что мальчики страдают тиками примерно в 3 раза чаще девочек. Возможно, речь идет о случаях неполной и зависимой от пола пенетрации гена.
В большинстве случаев первому появлению у детей тиков предшествует действие внешних неблагоприятных факторов. До 64% тиков у детей провоцируются стрессовыми ситуациями — школьной дезадаптацией, дополнительными учебными занятиями, бесконтрольными просмотрами телепередач или продолжительной работой на компьютере, конфликтами в семье и разлукой с одним из родителей, госпитализацией.
Простые моторные тики могут отмечаться в отдаленном периоде перенесенной черепно-мозговой травмы. Голосовые тики — покашливания, шмыгания носом, отхаркивающие горловые звуки — нередко встречаются у детей, часто болеющих респираторными инфекциями (бронхитами, тонзиллитами, ринитами).
У большинства пациентов существует суточная и сезонная зависимость тиков — они усиливаются вечером и обостряются в осенне-зимний период.
К отдельному виду гиперкинезов следует отнести тики, возникающие в результате непроизвольного подражания у некоторых повышенно внушаемых и впечатлительных детей. Происходит это в процессе непосредственного общения и при условии известного авторитета ребенка с тиками среди сверстников. Такие тики проходят самостоятельно через некоторое время после прекращения общения, но в некоторых случаях подобное подражание является дебютом заболевания.
Клиническая классификация тиков у детей
По этиологии
Первичные, или наследственные, включая синдром Туретта. Основной тип наследования — аутосомно-доминантный с различной степенью пенетратности, возможны спорадические случаи возникновения заболевания.
Вторичные, или органические. Факторы риска: анемия у беременных, возраст матери старше 30 лет, гипотрофия плода, недоношенность, родовая травма, перенесенные травмы головного мозга.
Криптогенные. Возникают на фоне полного здоровья у трети больных тиками.
По клиническим проявлениям
Локальный (фациальный) тик. Гиперкинезы захватывают одну мышечную группу, в основном мимическую мускулатуру; преобладают учащенные моргания, зажмуривания, подергивания углов рта и крыльев носа (табл. 1). Моргание является самым устойчивым из всех локальных тикозных расстройств. Зажмуривание отличается более выраженным нарушением тонуса (дистонический компонент). Движения крыльев носа, как правило, присоединяются к учащенному морганию и относятся к неустойчивым симптомам лицевых тиков. Единичные лицевые тики практически не мешают больным и в большинстве случаев не замечаются самими пациентами.
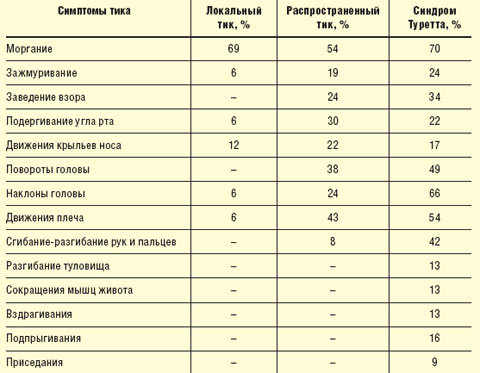 |
| Таблица 1 Виды моторных тиков (В. В. Зыков) |
Распространенный тик. В гиперкинез вовлекаются несколько мышечных групп: мимические, мышцы головы и шеи, плечевого пояса, верхних конечностей, мышцы живота и спины. У большинства больных распространенный тик начинается с моргания, к которому присоединяются заведение взора, повороты и наклоны головы, подъемы плеч. В периоды обострений тиков у школьников могут возникать проблемы при выполнении письменных заданий.
Вокальные тики. Различают вокальные тики простые и сложные.
Клиническая картина простых вокальных тиков представлена преимущественно низкими звуками: покашливанием, «прочисткой горла», хмыканием, шумным дыханием, шмыганием носом. Реже встречаются такие высокие звуки, как «и», «а», «у-у», «уф», «аф», «ай», визг и свист. При обострении тикозных гиперкинезов вокальные феномены могут изменяться, например покашливание переходит в хмыкание или шумное дыхание.
Сложные вокальные тики отмечаются у 6% больных синдромом Туретта и характеризуются произнесением отдельных слов, ругательствами (копролалией), повторением слов (эхолалией), быстрой неровной, неразборчивой речью (палилалией). Эхолалия является непостоянным симптомом и может встречаться в течение нескольких недель или месяцев. Копролалия обычно представляет собой статусное состояние в виде серийного произнесения ругательств. Нередко копролалия значительно ограничивает социальную активность ребенка, лишая его возможности посещать школу или общественные места. Палилалия проявляется навязчивым повторением последнего слова в предложении.
Генерализованный тик (синдром Туретта). Проявляется сочетанием распространенных моторных и вокальных простых и сложных тиков.
В таблице 1 представлены основные виды моторных тиков в зависимости от их распространенности и клинических проявлений.
Как видно из представленной таблицы, при усложнении клинической картины гиперкинезов, от локального к генерализованному, тики распространяются по направлению сверху вниз. Так, при локальном тике насильственные движения отмечаются в мышцах лица, при распространенном переходят на шею и руки, при генерализованном в процесс вовлекаются туловище и ноги. Моргание встречается с одинаковой частотой при всех видах тиков.
По тяжести клинической картины
Тяжесть клинической картины оценивают по количеству гиперкинезов у ребенка в течение 20 мин наблюдения. При этом тики могут отсутствовать, быть единичными, серийными или статусными. Оценка степени тяжести используется для унификации клинической картины и определения эффективности лечения.
При единичных тиках их количество за 20 мин осмотра составляет от 2 до 9, чаще встречаются у больных локальными формами и в стадии ремиссии у больных с распространенным тиком и синдромом Туретта.
При серийных тиках за 20 мин осмотра наблюдается от 10 до 29 гиперкинезов, после которых наступают многочасовые перерывы. Подобная картина характерна при обострении заболевания, встречается при любой локализации гиперкинезов.
При тикозным статусе серийные тики следуют с частотой от 30 до 120 и более за 20 мин осмотра без перерыва в течение дня.
Аналогично моторным тикам, вокальные тики также бывают единичными, серийными и статусными, усиливаются к вечеру, после эмоциональной нагрузки и переутомления.
По течению заболевания
Согласно диагностическому и статистическому руководству по психическим расстройствам (DSM–IV), выделяют преходящие тики, хронические тики и синдром Туретта.
Преходящее, или транзиторное, течение тиков подразумевает наличие у ребенка моторных или голосовых тиков с полным исчезновением симптомов заболевания в течение 1 года. Характерно для локальных и распространенных тиков.
Хроническое тиковое нарушение характеризуется моторными тиками продолжительностью более 1 года без вокального компонента. Хронические вокальные тики в изолированном виде встречаются редко. Выделяют ремиттирующий, стационарный и прогредиентный подтипы течения хронических тиков.
При ремиттирующем течении периоды обострений сменяются полным регрессом симптомов или наличием локальных единичных тиков, возникающих на фоне интенсивных эмоциональных или интеллектуальных нагрузок. Ремиттирующий подтип является основным вариантом течения тиков. При локальных и распространенных тиках обострение длится от нескольких недель до 3 мес, ремиссии сохраняются от 2–6 мес до года, в редких случаях до 5–6 лет. На фоне медикаментозного лечения возможна полная или неполная ремиссия гиперкинезов.
Стационарный тип течения заболевания определяется наличием стойких гиперкинезов в различных группах мышц, которые сохраняются на протяжении 2–3 лет.
Прогредиентное течение характеризуется отсутствием ремиссий, переходом локальных тиков в распространенные или генерализованные, усложнением стереотипий и ритуалов, развитием тикозных статусов, резистентностью к терапии. Прогредиентное течение преобладает у мальчиков с наследственными тиками. Неблагоприятными признаками является наличие у ребенка агрессивности, копролалии, навязчивостей.
Существует зависимость между локализацией тиков и течением заболевания. Так, для локального тика характерен транзиторно-ремиттирующий тип течения, для распространенного тика — ремиттирующе-стационарный, для синдрома Туретта — ремиттирующе-прогредиентный.
Возрастная динамика тиков
Чаще всего тики появляются у детей в возрасте от 2 до 17 лет, средний возраст — 6–7 лет, частота встречаемости в детской популяции — 6–10%. У большинства детей (96%) тик возникает до 11 лет. Наиболее частое проявление тика — моргание глазами. В 8–10 лет появляются вокальные тики, которые составляют примерно треть случаев всех тиков у детей и возникают как самостоятельно, так и на фоне моторных. Чаще первоначальными проявлениями вокальных тиков являются шмыгания носом и покашливания. Для заболевания характерно нарастающее течение с пиком проявлений в 10–12 лет, затем отмечается уменьшение симптоматики. В возрасте 18 лет приблизительно 50% пациентов самопроизвольно освобождаются от тиков. При этом нет зависимости между тяжестью проявления тиков в детстве и во взрослом возрасте, но в большинстве случаев у взрослых проявления гиперкинезов менее выражены. Иногда тики впервые возникают у взрослых, но они характеризуются более мягким течением и обычно продолжаются не более 1 года.
Прогноз для локальных тиков благоприятный в 90% случаев. В случае распространенных тиков у 50% детей отмечается полный регресс симптомов.
Синдром Туретта
Наиболее тяжелой формой гиперкинезов у детей является, без сомнения, синдром Туретта. Частота его составляет 1 случай на 1000 детского населения у мальчиков и 1 на 10 000 у девочек. Впервые синдром описал Жиль де ля Туретт в 1882 г. как «болезнь множественных тиков». Клиническая картина включает моторные и голосовые тики, дефицит внимания и обсессивно-компульсивное расстройство. Синдром наследуется с высокой пенетратностью по аутосомно-доминантному типу, причем у мальчиков тики чаще сочетаются с синдромом дефицита внимания и гиперактивностью, а у девочек — с обсессивно-компульсивным расстройством.
Общепринятыми в настоящее время являются критерии синдрома Туретта, приведенные в классификации DSM III пересмотра. Перечислим их.
Клиническая картина синдрома Туретта зависит от возраста пациента. Знание основных закономерностей развития болезни помогает выбрать правильную тактику лечения.
Дебют заболевания развивается в 3–7 лет. Первыми симптомами являются локальные лицевые тики и подергивания плеч. Затем гиперкинезы распространяются на верхние и нижние конечности, появляются вздрагивания и повороты головы, сгибание и разгибание кисти и пальцев, запрокидывание головы назад, сокращение мышц живота, подпрыгивания и приседания, один вид тиков сменяется другим. Вокальные тики часто присоединяются к моторным симптомам в течение нескольких лет после дебюта заболевания и усиливаются в стадии обострения. У ряда больных вокализмы являются первыми проявлениями синдрома Туретта, к которым в последующем присоединяются моторные гиперкинезы.
Генерализация тикозных гиперкинезов происходит в период продолжительностью от нескольких месяцев до 4 лет. В возрасте 8–11 лет у детей отмечается пик клинических проявлений симптомов в виде серий гиперкинезов или повторных гиперкинетических статусов в сочетании с ритуальными действиями и аутоагрессией. Тикозный статус при синдроме Туретта характеризует тяжелое гиперкинетическое состояние. Для серии гиперкинезов характерна смена моторных тиков вокальными с последующим появлением ритуальных движений. Больные отмечают дискомфорт от избыточных движений, например боль в шейном отделе позвоночника, возникающую на фоне поворотов головы. Наиболее тяжелый гиперкинез представляет собой запрокидывание головы — при этом пациент может повторно ударяться затылком о стену, нередко в сочетании с одновременными клоническими подергиваниями рук и ног и появлением мышечных болей в конечностях. Продолжительность статусных тиков колеблется от нескольких суток до нескольких недель. В некоторых случаях отмечаются исключительно моторные или преимущественно вокальные тики (копролалия). Во время статусных тиков сознание у детей полностью сохранено, однако гиперкинезы не контролируются пациентами. Во время обострений заболевания дети не могут посещать школу, у них затрудняется самообслуживание. Характерно ремиттирующее течение с обострениями длительностью от 2 до 12–14 мес и неполными ремиссиями от нескольких недель до 2–3 мес. Длительность обострений и ремиссий находится в прямой зависимости от тяжести тиков.
У большинства больных в 12–15 лет генерализованные гиперкинезы переходят в резидуальную фазу, проявляющуюся локальными или распространенными тиками. У трети больных с синдромом Туретта без обсессивно-компульсивных расстройств в резидуальной стадии наблюдается полное прекращение тиков, что можно рассматривать как возрастзависимую инфантильную форму заболевания.
Коморбидность тиков у детей
Тики нередко возникают у детей с уже имеющимися заболеваниями со стороны центральной нервной системы (ЦНС), такими как синдром дефицита внимания с гиперактивностью (СДВГ), церебрастенический синдром, а также тревожные расстройства, включающие генерализованное тревожное расстройство, специфичные фобии и обсессивно-компульсивное расстройство.
Примерно у 11% детей с СДВГ встречаются тики. Преимущественно это простые моторные и вокальные тики с хроническим рецидивирующим течением и благоприятным прогнозом. В отдельных случаях затруднен дифференциальный диагноз между СДВГ и синдромом Туретта, когда гиперактивность и импульсивность появляются у ребенка до развития гиперкинезов.
У детей, страдающих генерализованным тревожным расстройством или специфичными фобиями, тики могут быть спровоцированы или усилены волнениями и переживаниями, непривычной обстановкой, длительным ожиданием какого-либо события и сопутствующим нарастанием психоэмоционального напряжения.
У детей с обсессивно-компульсивными расстройствами голосовые и моторные тики сочетаются с навязчивым повторением какого-либо движения или занятия. По всей видимости, у детей с тревожными расстройствами тики являются дополнительной, хотя и патологической формой психомоторной разрядки, способом успокоения и «переработки» накопившегося внутреннего дискомфорта.
Церебрастенический синдром в детском возрасте является следствием перенесенных черепно-мозговых травм или нейроинфекций. Появление или усиление тиков у детей с церебрастеническим синдромом нередко провоцируется внешними факторами: жарой, духотой, изменением барометрического давления. Характерно нарастание тиков при утомлении, после длительных или повторных соматических и инфекционных заболеваний, увеличении учебных нагрузок.
Приведем собственные данные. Из 52 детей, обратившихся с жалобами на тики, было 44 мальчика, 7 девочек; соотношение «мальчики : девочки» составило «6 : 1» (табл. 2).
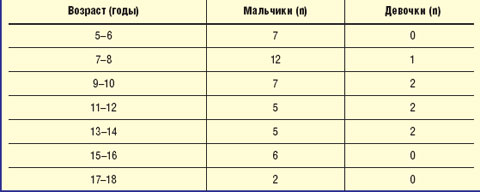 |
| Таблица 2 Распределение детей с тиками по возрасту и полу |
Итак, наибольшее число обращений по поводу тиков отмечалось у мальчиков в возрасте 5–10 лет с пиком в 7–8 лет. Клиническая картина тиков представлена в табл. 3.
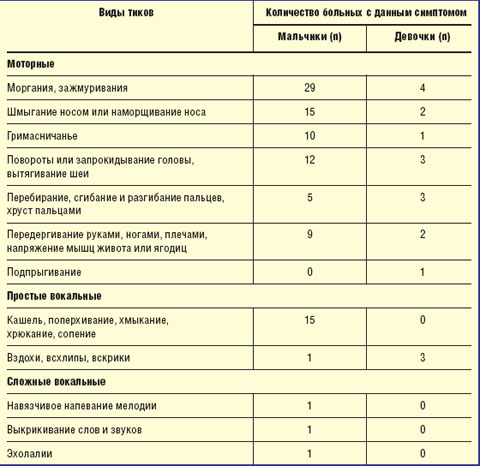 |
| Таблица 3 Виды тиков у пациентов группы |
Таким образом, чаще всего отмечались простые моторные тики с локализацией преимущественно в мышцах лица и шеи и простые вокальные тики, имитирующие физиологические действия (кашель, отхаркивание). Подпрыгивания и сложные вокальные высказывания встречались гораздо реже — только у детей с синдромом Туретта.
Временные (транзиторные) тики продолжительностью менее 1 года наблюдались чаще, чем хронические (ремиттирующие или стационарные). Синдром Туретта (хронический стационарный генерализованный тик) отмечался у 7 детей (5 мальчиков и 2 девочки) (табл. 4).
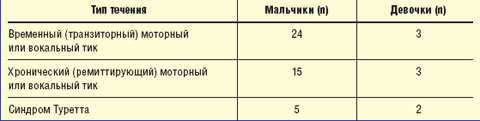 |
| Таблица 4 Распределение пациентов по типу лечения тиков |
Лечение
Основным принципом терапии тиков у детей является комплексный и дифференцированный подход к лечению. До назначения медикаментозной или иной терапии необходимо выяснить возможные причины возникновения заболевания и обсудить с родителями способы педагогической коррекции. Необходимо разъяснить непроизвольный характер гиперкинезов, невозможность контроля их усилием воли и, как следствие этого, недопустимость замечаний ребенку по поводу тиков. Нередко выраженность тиков снижается при уменьшении требований к ребенку со стороны родителей, отсутствии фиксации внимания на его недостатках, восприятии его личности в целом, без вычленения «хороших» и «плохих» качеств. Терапевтический эффект оказывают упорядочение режима, занятия спортом, особенно на свежем воздухе. При подозрении на индуцированные тики необходима помощь психотерапевта, поскольку подобные гиперкинезы снимаются внушением.
При решении вопроса о назначении медикаментозного лечения необходимо учитывать такие факторы, как этиология, возраст пациента, тяжесть и выраженность тиков, их характер, сопутствующие заболевания. Медикаментозное лечение необходимо проводить при тяжелых, выраженных, упорных тиках, сочетающихся с нарушениями поведения, неуспеваемостью в школе, влияющих на самочувствие ребенка, осложняющих его адаптацию в коллективе, ограничивающих его возможности самореализации. Лекарственная терапия не должна назначаться, если тики беспокоят только родителей, но не нарушают нормальную активность ребенка.
Галоперидол: начальная доза составляет 0,5 мг на ночь, затем ее повышают на 0,5 мг в неделю до достижения терапевтического эффекта (1–3 мг/сут в 2 приема).
Флуфеназин назначается в дозе 1 мг/сут, затем дозу увеличивают на 1 мг в неделю до 2–6 мг/сут.
Рисперидон относится к группе атипичных нейролептиков. Известна эффективность рисперидона при тике и связанных с ним нарушениях поведения, особенно оппозиционно-вызывающего характера. Начальная доза — 0,5–1 мг/сут с постепенным ее повышением до достижения положительной динамики.
Тиаприд (Тиапридал): детям 7–12 лет рекомендуется по 50 мг (1/2 таблетки) 1–2 раза в день.
При выборе препарата для лечения ребенка с тиками следует учитывать наиболее удобную для дозирования форму выпуска. Оптимальными для титрования и последующего лечения в детском возрасте являются капельные формы (галоперидол, рисперидон), позволяющие наиболее точно подобрать поддерживающую дозу и избежать неоправданной передозировки лекарства, что особенно актуально при проведении длительных курсов лечения. Предпочтение также отдается препаратам, обладающим относительно низким риском развития побочных эффектов (рисперидон, тиаприд).
Метоклопрамид (Реглан, Церукал) является специфическим блокатором дофаминовых и серотониновых рецепторов триггерной зоны ствола мозга. При синдроме Туретта у детей применяется в дозе 5–10 мг в день (1/2–1 таблетка), в 2–3 приема. Побочные действия — экстрапирамидные расстройства, проявляющиеся при превышении дозы 0,5 мг/кг/сут.
Для лечения гиперкинезов в последние годы применяют препараты вальпроевой кислоты. Основной механизм действия вальпроатов заключается в усилении синтеза и высвобождении γ-аминомасляной кислоты, которая является тормозным медиатором ЦНС. Вальпроаты являются препаратами первого выбора при лечении эпилепсии, однако интерес представляет их тимолептический эффект, проявляющийся в уменьшении гиперактивности, агрессивности, раздражительности, а также положительное влияние на выраженность гиперкинезов. Терапевтическая доза, рекомендуемая для лечения гиперкинезов, значительно ниже, чем при лечении эпилепсии, и составляет 20 мг/кг/сут. Из побочных эффектов отмечены сонливость, повышение массы тела, выпадение волос.
При сочетании гиперкинезов с обсессивно-компульсивным расстройством положительный эффект оказывают антидепрессанты — кломипрамин, флуоксетин.
Кломипрамин (Анафранил, Кломинал, Клофранил) является трициклическим антидепрессантом, механизм действия — торможение обратного захвата норэпинефрина и серотонина. Рекомендованная доза у детей с тиками — 3 мг/кг/сут. К побочным эффектам относятся преходящие нарушения зрения, сухость во рту, тошнота, задержка мочи, головная боль, головокружение, бессонница, возбудимость, экстрапирамидные расстройства.
Флуоксетин (Прозак) — антидепрессивное средство, селективный ингибитор обратного захвата серотонина, обладающий низкой активностью по отношению к норэпинефриновой и дофаминергической системам головного мозга. У детей с синдромом Туретта хорошо устраняет беспокойство, тревогу, страх. Начальная доза в детском возрасте составляет 5 мг/сут 1 раз в день, эффективная — 10–20 мг/сут 1 раз утром. Переносимость препарата в целом хорошая, побочные эффекты возникают относительно редко. Среди них наиболее значимыми являются тревожность, нарушения сна, астенический синдром, потливость, снижение массы тела. Препарат также эффективен в комбинации с пимозидом.
Литература
Н. Ю. Суворинова, кандидат медицинских наук
РГМУ, Москва



 Читайте также:
Читайте также: