Ацетат натрия для чего используется
Ацетат натрия
| Ацетат натрия | |
|---|---|
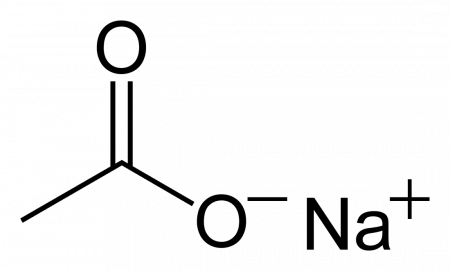 | |
| Систематическое наименование | sodium acetate (ИЮПАК) sodium ethanoate (систематическое) ацетат натрия натрия этаноат натрий уксуснокислый |
| Хим. формула | C2H3O2Na |
| Рац. формула | CH3COONa |
| Состояние | белый гигроскопичный порошок |
| Молярная масса | 82.03 грамм/моль (безводная форма) 136.08 грамм/моль (тригидрат) г/моль |
| Плотность | 1,45 г/см³ |
| Температура | |
| • плавления | 328 °C |
| • разложения | 324 °C |
| Удельная теплота плавления | 264—289 кДж/кг |
| Растворимость | |
| • в воде | 76 г/100 мл |
| Рег. номер CAS | 127-09-3 |
| PubChem | 517045 |
| Рег. номер EINECS | 204-823-8 |
| SMILES | |
| Кодекс Алиментариус | E262 |
| ChEBI | 32954 |
| ChemSpider | 29105 |
| Токсичность | ирритант, малотоксичен |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Ацетат натрия CH3COONa, — натриевая соль уксусной кислоты, кристаллы со слабым солёным вкусом и уксусным запахом, производится и применяется в промышленных масштабах.
Содержание
Область применения
Ацетат натрия используется в текстильном производстве для нейтрализации отработанной серной кислоты в сточных водах и как фоторезист при использовании анилиновых красителей. Также используется при дублении солями хрома (для протравливания), и замедляет процесс вулканизации хлоропрена при производстве синтетических резин.
Ацетат натрия известен как пищевая добавка E262 и применяется как консервант.
Также ацетат натрия является источником углерода для бактерий, выращиваемых на питательной среде.
В растворе ацетат натрия (будучи солью слабой кислоты) и уксусная кислота могут применяться как буфер, для сохранения относительно постоянного pH. Это особенно полезно в биохимии в pH-зависимых реакциях.
Ацетат натрия также используется в быту как составная химических грелок (англ. heating pad ) или химических обогревателей (англ. Hand warmer ), применяется как составная часть смеси «горячего льда» (англ. «hot ice» ), при кристаллизации ацетата натрия выделяется тепло — это экзотермический процесс. При нагреве тригидрата ацетата натрия (имеющего точку плавления в 58 °C) до 100 °C (обычно ёмкость с ним кладут в кипящую воду) он расплавляется (вернее, растворяется в собственной кристаллизационной воде) и переходит в водный раствор ацетата натрия. При охлаждении этого раствора образуется перенасыщенный раствор ацетата натрия в воде. Этот раствор прекрасно переохлаждается до комнатной температуры без образования твёрдой фазы, затем нажатием на металлический диск в ёмкости образуется центр кристаллизации, который, вырастая, заставляет перенасыщенный раствор переходить в твёрдую фазу тригидрата ацетата натрия. Этот процесс сопровождается значительным выделением тепла (экзотермическая реакция), теплота фазового перехода составляет 264-289 кДж/кг.
На этом свойстве основан довольно красивый химический опыт — «горячий лёд».
Способы получения
Это — хорошо известная реакция «гашения» пищевой соды и винного уксуса, происходящая в тесте. 84 г гидрокарбоната натрия реагируют с 750 г 8%-го винного уксуса (или же с 86 г 70%-й уксусной эссенции) с образованием 82 г ацетата натрия в растворе. Выпариванием воды можно получить чистый кристаллический ацетат натрия. Для получения тригидрата ацетата натрия без выпаривания необходимо смешать 84 г гидрокарбоната натрия (пищевой соды) с 86 г 70%-ной уксусной кислоты и 10 г воды.
Характерные реакции
Ацетат натрия может быть использован для образования сложного эфира по реакции с алкилгалогенидами, такими как, например, бромэтан:
При сильном нагревании (более 324 °C) ацетат натрия разлагается на карбонат натрия и ацетон:
2CH3COONa → Na2CO3 + (CH3)2CO
Влияние на организм
Ацетат натрия может всасываться в организм при проглатывании. Является ирритантом. LD50 25956 мг/кг. По другим данным из того же источника: LD50(крысы, орально): 3500 мг/кг, LD50(мыши, орально): 4960 мг/кг.
Натрия Ацетат
Химическое название
Натриевая соль уксусной кислоты, натрия этаноат.
Химические свойства
Белый гигроскопичный мелкий порошок, растворимый в воде. Разлагается при 324 градусах Цельсия. Молекулярная масса = 82 грамма на моль для безводной формы, 136,1 грамм на моль – для тригидрата. Формула Натрия Ацетата: CH3COONa; рацемическая формула: C2H3O2Na; формула тригидрата: C2H3O2Na х 3H2O.
Химические свойства
Вещество можно получить с помощью реакции уксусной кислоты с карбонатом или гидрокарбонатом натрия, с NaOH. В домашних условиях — это реакция винного уксуса с пищевой содой, к 1 грамму соды добавляют 9 грамм уксуса.
Реакция электролиза Ацетата Натрия. Во время превращения происходит диссоциация CH3COONa до CH3COO- и Na+. У анода выделяется этан и углекислый газ. Далее углекислый газ вступает в реакцию с гидроксидом бария или натрия (NaOH), во втором случаев пробирке останется чистый этан.
Достаточно популярна в химии реакция гидролиза Ацетата Натрия. Для наглядности, образованную слабой к-ой и сильным основанием соль, смешивают с индикатором-фенолфталеином. Смесь нагревают, при этом соль частично плавится и в расплаве появляются гидроксид-ионы. Затем пробирку охлаждают, соль кристаллизуется, и смесь утрачивает фиолетовую окраску. Соединение также реагирует с алкилгалогенидами, бромэтаном с образованием сложных эфиров.
Качественная реакция на Ацетат Натрия проводится в два этапа. Сначала определяют наличие в соединении ионов Na, а затем – кислотного ацетат-остатка. Натрий будет гореть ярко желтым пламенем, если небольшое количество раствора (или сухого вещ-ва) внести в пламя спиртовой горелки. Качественную реакцию на ацетат ион можно провести с помощью любой растворимой соли трехвалентного железа. Раствор станет красно-коричневого цвета, а при нагревании выпадет темно-коричневый осадок Fe(OH)3.
Химическое соединение используют при производстве текстиля; в качестве фоторезиста после применения анилиновых красителей; при вулканизации и в кожевенном производстве. Вещество получило широкое применение в виде пищевой добавки E262, используется в качестве консерванта; его применяют для сохранения стабильного рН в биохимии. Соединение используют при производстве химических обогревателей и грелок, («горячий лёд»). В медицине также используют тригидрат Натрия Ацетата.
Фармакологическое действие
Восстанавливает водно-солевой баланс.
Фармакодинамика и фармакокинетика
Натрия Ацетат применяют в комбинации с другими хим. соединениями. Вещество используют для дезинтоксикации и регидратации. Средство обладает способностью восстанавливать водный и электролитный баланс во время обезвоживания. Стимулирует диурез и предотвращает развитие метаболического ацидоза. Обладает дезинтоксикационным, регидратирующим и плазмозамещающим действием.
Показания к применению
Применяется при регидратации, интоксикации, гиперкалиемии, обезвоживании у пациентов с пищевыми инфекциями, холерой, острой дизентерией и так далее.
Противопоказания
Побочные действия
Редко при применении растворов для внутривенного введения с данным лекарственным средством возникает отечность, тахикардия, озноб.
Инструкция по применению (Способ и дозировка)
Натрия Ацетат в составе различных препаратов для внутривенного введения применяется в условиях стационара, под контролем лабораторных показателей. Растворы вводят струйно или капельно. Дозировка зависит от состояния пациента и тяжести состояния. Как правило, если пациент находится в тяжелом состоянии, то сначала вводят лекарство струйно, затем переходят на инфузии.
Передозировка
Нет сведений о передозировке средством.
Взаимодействие
Вещество часто применяют в комбинации с другими электролитами.
Ацетат Натрия можно сочетать с натрия хлоридом и натрием фумаровокислым, при этом необходимо визуально следить за совместимостью растворов.
Условия продажи
Может потребоваться рецепт.
Особые указания
Лечение препаратом проводят под контролем уровня электролитов крови и гематокрита.
Ацетаты натрия (Е262)

Характеристика химических свойств и способа получения добавки Е262
По своей структуре ацетаты натрия – это соли уксусной кислоты, так как именно из этого сырья её и получают: карбонаты или гидроксиды натрия подвергают реакции с кислотой. Как ни странно, часть производство вещества связано с перегонкой и обработкой древесины.
Добавка имеет вид кристаллического порошка, которое имеет слабый запах уксуса. Может иметь белесоватый, светло-жёлтый или коричневый оттенок. Вещество хорошо растворимо в воде, хуже – в спиртах и эфире. Кроме того, оно не подвержено горению.
Основные свойства ацетатов натрия, за которые его так ценят промышленники – это способность к регуляции уровня кислотности химической среды, консервации и стабилизации веществ. Добавка помогает сохранить форму и текстуру продуктов, их вкусовые и ароматические характеристики, способна улучшить консистенцию сырья.
Немногие добавки могут похвастаться тем, что они встречаются в живой природе. Как раз ацетаты натрия могут: они существуют как элемент клеток животных и растений, как составляющая кислот во фруктах, присутствует в кисломолочных продуктах как результат ферментации бактерий.
Области применения вещества человеком
Существует несколько видов ацетатов натрия: технический и пищевой. Первую разновидность используют в производстве химических грелок и обогревателей, как составную часть смеси “горячий лёд”. В сфере строительства ацетаты натрия дают противоморозный эффект для бетона, используются при возведении монолитных конструкций.
Текстильная промышленность применяет вещество при окрашивании тканей и дублении кожи. Также добавка используется в сфере фотографии и гальванотехники, в производстве красящих продуктов, средств гигиены, в химической отрасли.
По своей структуре технический ацетат натрия – это тригидрат натриевой соли уксусной кислоты, который имеет вид чешуек или кусочков различных форм.
Вообще человеку знакомы два типа добавки Е262:
Вещества имеют различные химические формулы, но мало отличаются друг от друга по своим свойствам.

В медицинской промышленности добавка применяется в изготовлении мочегонных препаратов и других лекарств.
Требования к упаковке добавки Е262
В любом из видов упаковки внутри должен быть дополнительный подклад из плотного пищевого полиэтилена. Так как вещество очень подвержено реакции с водой, на таре обычно ставят отметку “Беречь от влаги”.
Чаще всего ацетаты натрия хранятся и транспортируются в пищевых мешках из ткани (в таких обычно можно видеть муку и крупы). Также для этих целей используются ящики из гофрированного картона или многослойные бумажные пакеты, бочки, контейнеры.
Влияние на здоровье человека
По различным данным, вред от употребления продуктов с ацетатами натрия в составе колеблется от крайне незначительного уровня до среднего.
На сегодня официально добавка разрешена в США, Канаде, Европейском союзе, Украине, России, Австралии. Нет никаких официальных данных по поводу возможной связи между её применением и появлением онкологических заболеваний, генных мутаций, бесплодия, отравлений, по крайней мере, при потреблении в тех количествах, в которых вещество используется в пищевых продуктах.
Зафиксировано несколько случаев появления аллергической реакции у людей, страдающих аллергией на уксус.
Тем, кто имеет проблемы с функционированием вегетативной системы, жёлчного пузыря, кишечника, в частности, дисбактериоз, печени, почек, сердечно-сосудистой системы, лучше воздержаться от питания едой с добавкой в составе.
Превышение нормальной суточной дозировки ацетатов натрия для взрослого человека может обернуться некоторыми неприятными симптомами: головной болью и головокружением, нарушением координации, болями и спазмами в животе, судорогами, удушьем, изменением цвета кожных покровов и слизистых на более бледный.
По некоторым неподтверждённым данным, вещество всё-таки имеет свойства канцерогена по причине того, что в кишечнике оно превращается в нитраты, которые могут провоцировать появление злокачественных опухолей, или, как минимум, мощной аллергии. Официального подтверждения этой информации мировому сообществу предоставлено не было, поэтому ацетаты натрия не признаны онкогенной или опасной добавкой.
Некоторые специалисты советуют ограничить поступление вещества в организм ребёнка, чтобы не вызвать у него появление аллергии.
Натрия ацетат считается безвредным веществом, и имеет широкую сферу применения, от производства кожаных изделий до приготовления картофельных чипсов. Он обладает выраженными свойствами консерванта и стабилизатора, однако от других консервантов отличается тем, что не угнетает рост и развитие бактерий, и выступает как фермент, образующийся в процессе жизнедеятельности этих бактерий в веществах.
Существуют некоторые ограничения в употреблении продуктов с веществом в составе для аллергиков, детей и людей с нарушениями в работе внутренних органов.
Процессы исследований действия ацетатов натрия на человека продолжаются до сих пор, а пока, в силу отсутствия значительного негативного влияния на организм здорового человека, мировым сообществом не было установлено нормы суточного потребления добавки Е262.
Натрий уксуснокислый — реактив, востребованный промышленностью в больших количествах
Натрий уксуснокислый (ацетат натрия, натрия этаноат) — органическое соединение, соль уксусной кислоты, традиционно называемая ацетатом. Формула CH3COONa или C2H3O2Na. 
Кристаллическое вещество с гигроскопичными кристаллами белого, светло-желтого, желтого, коричневого цвета; со слабым запахом уксуса. Водорастворимое, плохо растворяется в спиртах и эфирах.
Процесс кристаллизации экзотермический. При нагревании ацетат натрия разлагается с образованием ацетона и углекислого натрия. Считается малотоксичным, огне- и взрывобезопасен. Взаимодействует с кислотами. Реакция с серной кислотой приводит к образованию нерастворимого осадка — это свойство используется для нейтрализации серной кислоты. Образует сложные эфиры.
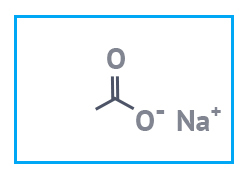 | 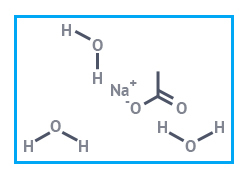 |
| Натрий уксуснокислый (ацетат) б/в | Натрий уксуснокислый 3-вод. (ацетат) |
«Горячий лед», который используется в бытовых химических грелках, — это 3-водный ацетат натрия. Он плавится при температуре +58 °С. При помещении грелки в кипяток, вещество становится жидким, сохраняя это состояние и при комнатной температуре. Для начала процесса кристаллизации достаточно нажать на небольшой металлический диск внутри грелки. Он становится центром кристаллизации и запускает процесс. По мере кристаллизации реактива выделяется значительное количество тепла. Тепло выделяется до тех пор, пока все вещество внутри грелки не станет твердым (поэтому и называют — «горячий лед»). Чтобы вернуть грелку в исходное состояние, ее нужно опять прокипятить в воде, чтобы расплавить содержимое.
Пищевая добавка E262 (ацетат натрия): влияние на здоровье
Что это такое?
Е262 — это ацетат натрия (лат. Sodium Acetatei), натриевая соль уксусной кислоты. Ацетат натрия используют в пищевой промышленности в качестве консерванта, ароматизатора и регулятора кислотности. Добавка Е262 может быть двух видов: Е262i и E262ii

| Добавка Е262i | |
| Химическая формула | C2H3O2Na |
| Химическое название | Ацетат натрия ангидридный (безводный) |
| Состав | Получают соединением уксусной кислоты и карбоната натрия |
| Происхождение | Искусственное |
| Вид | Порошок или гранулы |
| Вкус | Отсутствует |
| Цвет | Белый |
| Запах | Отсутствует |
| Функция | Консервант, регулятор кислотности, ароматизатор |

| Добавка Е262ii | |
| Химическая формула | C4H7O4Na |
| Химическое название | Диацетат натрия |
| Состав | Получают соединением уксусной кислоты и гидроксида натрия |
| Происхождение | Искусственное |
| Вид | Кристаллическая твёрдая масса |
| Вкус | Отсутствует |
| Цвет | Белый |
| Запах | Запах уксусной кислоты |
| Функция | Консервант, регулятор кислотности, ароматизатор |
Производство
Консерванты Е262i (ацетат натрия) и Е262ii (диацетат натрия) производят промышленным путем:
Основные зарубежные производители добавки:
В России добавку производят:
Применение
Ацетат натрия используется во многих сферах производства. Ценные химические свойства соединения позволяют использовать его в различных видах промышленности.
Пищевая промышленность
Добавка Е262 применяется в пищевой промышленности в качестве консерванта. Она добавляется в муку, чтобы защитить хлеб от поражения бактериями картофельной палочки. Также Е262 добавляется в майонезы, сухие бульоны и супы быстрого приготовления.
В качестве усилителя вкуса ацетат натрия используется в приготовлении чипсов. Он придает продукту легкий уксусный аромат, который усиливает слюноотделение и даже вызывает привыкание у потребителя.
Е262 используется при производстве овощных и фруктовых консервов. Добавка нейтрализует резкий запах уксусной кислоты.
Медицинская промышленность
Используется при производстве антисептиков, мочегонных и противовоспалительных препаратов.
Текстильная промышленность
Натриевая соль уксусной кислоты используется для протравки кожевенных изделий. При окраске тканей она играет роль закрепителя цвета.
Другое
Влияние на организм
Пищевая добавка Е262 не канцерогенна. В природе ацетат натрия образуется в результате бактериальной ферментации и входит в состав многих продуктов, например, кисломолочных. Но, как природные продукты могут вызывать позитивную и негативную реакции организма, так и химическое соединение Е262 неоднозначно влияет на здоровье.
Польза
Ацетат натрия обладает дезинфицирующим и бактерицидным действием. Подавляет рост бактерий и грибков. Согласно ГОСТ 12.1.007-76 ему присвоен четвертый (наивысший) класс безопасности.
Возможны аллергические реакции при высокой чувствительности к уксусу.
При длительном вдыхании Е262ii (диацетата натрия) или чрезмерного употребления внутрь возможны негативные реакции:
Рекомендуется ограниченно употреблять продукты, содержащие Е262 людям с болезнями сердца, желудка, почек, печени и желчевыводящих путей.
Допустимое суточное применение
Каких-либо ограничений по суточному употреблению Е262 не выявлено. Ацетат натрия содержится во фруктах, овощах и кисломолочных продуктах в естественном виде. Чтобы не допустить негативных реакций организма, достаточно не переедать.
Как определить добавку в продукте
На вкус присутствие Е262 в продукте определить практически невозможно. Ацетат натрия вкуса и запаха не имеет, а диацетат натрия имеет легкую кислинку и слабый уксусный запах.
На упаковках овощных и фруктовых консервов добавка обозначается в составе продукта в международной кодировке — Е262. Также входит в состав колбасных изделий.
В кисломолочных продуктах ацетат натрия образуется естественным путем.
Чем можно заменить?
Добавка не имеет полноценных заменителей.
В каких странах разрешена, а в каких запрещена
Пищевая добавка Е262 разрешена к применению во всех странах.




