Армс что это такое в медицине расшифровка
Хроническая почечная недостаточность
Хроническая почечная недостаточность – это состояние, при котором выделительная система человека перестаёт выполнять физиологические функции. Из-за гибели нефронов почки утрачивают способность поддерживать гомеостаз – постоянство внутренней среды. При хронической почечной недостаточности у мужчин и у женщин продукты распада нутриентов полностью не выводятся из организма, что влечет за собой тяжелые осложнения. В НИИ урологии и интервенционной радиологии имени Н.А. Лопаткина — филиале ФГБУ «НМИЦ радиологии» Минздрава России применяются все современные методы лечения данного заболевания.
Хроническая почечная недостаточность (ХПН) является обычно исходом заболеваний, приводящих к прогрессирующей потере нефронов:
Причины ХПН
Дисфункции мочевыделительной системы могут провоцировать другие острые и хронические патологии:
Хроническая почечная недостаточность также развивается по таким причинам:
Стадии хронической почечной недостаточности
В своем развитии почечная недостаточность проходит 4 стадии:
Хроническая почечная недостаточность по разным причинам может развиваться в течение нескольких месяцев и даже лет. Поэтому рекомендуется обращать внимание на первые тревожные «звоночки», чтобы не допустить развитие осложнений.
Симптомы и признаки ХПН
Клинические проявления хронической почечной недостаточности многообразны:
Прогрессирование хронической почечной недостаточности влечет за собой развитие следующих симптомов:
Хроническая почечная недостаточность на последней стадии сопровождается такими симптомами, как одышка, частое сердцебиение, отеки, глубокое шумное дыхание, судороги в конечностях. Ярким признаком прогрессирования заболевания считается уменьшение суточного объема мочи до 200 мл. Стул становится зловонным, изо рта появляется неприятный запах.
Вероятные осложнения при ХПН
При отсутствии своевременной диагностики и грамотной терапии хроническая почечная недостаточность провоцирует полиорганные нарушения со стороны:
Без соответствующего лечения хроническая почечная недостаточность может закончиться летальным исходом из-за уремической комы или сердечно-сосудистых нарушений у женщин и у мужчин.
Диагностика хронической почечной недостаточности
Ключевую роль в диагностике хронической почечной недостаточности играют лабораторные исследования. Уже при первых признаках заболевания могут наблюдаться изменения в составе крови – повышение уровня креатинина, мочевой кислоты и щелочной фосфатазы. При этом снижается уровень гемоглобина, тромбоцитов, альбумина и калия, уменьшаются показатели вязкости крови (гематокрита). Важный симптом хронической почечной недостаточности – существенное снижение плотности мочи, повышение уровня эритроцитов, лейкоцитов, белка и цилиндров.
Комплексная диагностика включает также липидограмму – исследование всего спектра жировых соединений в составе крови. Особое внимание уделяется показателям триглицеридов и холестерола.
Поставить точный диагноз «хроническая почечная недостаточность» помогают такие методы:
Лечение хронической почечной недостаточности
Лечение хронической почечной недостаточности направлено на достижение стойкой ремиссии, поскольку добиться абсолютного выздоровления современная медицина не способна. Но благодаря своевременной терапии удается сгладить симптоматику, отсрочить появление осложнений и существенно улучшить качество жизни пациента.
Лечение хронической почечной недостаточности должно начинаться с устранения основной причины патологии. Усилия врачей направлены на компенсацию признаков сахарного диабета, гломерулонефрита, поликистоза и других аутоиммунных нарушений. В приоритете – комплексный подход к лечению, который включает:
Большая роль отводится симптоматическому лечению, которое позволяет облегчить протекание болезни и улучшить самочувствие пациента. Больным назначают препараты, которые восполняют дефицит витамина D, контролируют артериальное давление, корректируют кислотно-щелочной баланс, борются с олигурией.
В некоторых случаях для лечения хронической почечной недостаточности показаны дробные переливания эритроцитной массы. Методика позволяет повысить уровень гемоглобина в крови, уменьшить проявления анемии, устранить последствия внутренних кровотечений. По достижении ремиссии пациентам с хронической почечной недостаточностью показано санаторно-курортное лечение.
Если консервативные методы терапии не дают ожидаемых результатов, пациенту может быть назначена трансплантация почки. Это физиологический метод заместительного лечения с использованием донорского органа. После пересадки почки проводится комбинированная иммуносупрессивная терапия, препятствующая отторжению донорской почки.
Основными способами лечения ТХПН повсеместно признаны диализ и трансплантация почки.
Наиболее полное замещение почечной функции происходит в результате успешной трансплантации почки, а диализ замещает ее лишь частично.
Гемодиализ (ГД)
— метод внепочечного очищения крови при острой и хронической болезни почек. Во время гемодиализа происходит удаление из организма токсических продуктов обмена веществ, для уменьшения биохимических аномалий, нормализация нарушений водного, электролитного балансов и кислотно-щелочного равновесий. Очищение крови производится путем снижения концентрации в ней вредных веществ. В зависимости от метода гемодиализа, это достигается различными путями. Под гемодиализом понимают процедуру фильтрации плазмы крови с помощью полупроницаемой мембраны, через поры которой проходят молекулы с небольшой молекулярной массой, а крупные молекулы белков остаются в плазме, которая затем возвращается в кровоток пациента.
Назначение:
1.Обеспечение компенсаторной функции почек, фильтрация крови от токсических соединений и конечных продуктов метаболизма. Гемодиализ при хронической недостаточности проводят трижды за неделю, но нарастание интоксикации – основание для более частого проведения процедуры. При крайне тяжести, диализ выполняют до конца жизни, или пока не трансплантируют здоровую почку. 2. Почечная недостаточность, как осложнение острого гломерулонефрита, пиелонефрита. Цель назначения процедуры – вывести излишек жидкости из организма, устранить отеки, эвакуировать продукты токсического свойства. 3. Дисбаланс электролитов в крови. Указанное состояние происходит вследствие массивных ожогов, перитонита, обезвоживания, лихорадочных явлений. Гемодиализ позволяет вывести чрезмерную концентрацию ионов одного вида, заместив их другими. Также показанием для рассматриваемой процедуры выступает избыток жидкости в организме, что приводит к отеку оболочек головного мозга, сердца, легких. Диализ помогает сократить отечность и снизить уровень артериального давления. Процедура гемодиализа проводится на АИП с помощью одноразовых расходных материалов, к которым относятся диализаторы, кровопроводящие магистрали, фистульные иглы, катетеры, диализные концентраты.
Аппарат для гемодиализа представляет автоматизированное высокопоточное устройство, с помощью которого достигается максимально качественная очистка жидкостей. Многочисленные датчики следят за процессом и контролируют все его показатели. Организм, подключенный к диализатору, получает необходимую качественную очищенную кровь. Диализ позволяет лишь частично заменить работу почек, так как не способен обеспечить ее эндокринные функции. Но и этого бывает достаточно, чтобы улучшить состояние больного.
Показания к началу Заместительной почечной терапии – гемодиализу:
В дневном стационаре – отделении гемодиализа вам помогут:
Процедура проводится 3 раза в неделю. Длительность ее составляет от 240 мин до 270 мин.
В дневном стационаре проводятся:
Отделение развернуто на 15 диализных мест. Парк аппаратов «Искусственная почка» насчитывает 15 диализных мест, работающих в 4 смены круглосуточно. Для диализа используются диализаторы с мембраной нового поколения (из полисульфона, благодаря высокой проницаемости такой мембраны кровь проходит глубокую очистку, и выводится больший объем токсинов, чем с обычной мембраной из целлюлозы), глюкозосодержащие концентраты диализирующей жидкости, установлена высокопроизводительная система водоочистки, качество воды которой полностью соответствует мировым стандартам. Наше отделение оборудовано пандусами, поручнями, что очень важно для пациентов с ограниченными возможностями здоровья.
В отделении гемодиализа пациенты могут получить консультативную помощь всех специалистов НИИ урологии и интервенционной радиологии имени Н.А. Лопаткина –филиала ФГБУ «НМИЦ радиологии» Минздрава России. Подключение к аппарату искусственной почки и регулярное прохождение процедуры позволяют продлить жизнь от 15 до 25 лет. Пациенты, отказавшиеся от данной процедуры, имеют риск летального исхода намного раньше – за считанные месяцы.
Все услуги и медицинская помощь оказывается пациентам абсолютно бесплатно в рамках ОМС.
Отделение, в котором лечат почечную недостаточность
Жители города Москвы для получения направления и прикрепления к гемодиализному центру должны пройти консультацию у главного внештатного специалиста – нефролога Департамента здравоохранения г. Москвы в консультативно-диагностическом отделении Городской клинической больницы №52.
Жители субъектов РФ могут поступить на лечение в Дневной стационар НИИ урологии и интервенционной радиологии имения Н.А. Лопаткина по направлению формы 057/у.
Платные медицинские услуги предоставляются в виде комплексной программы медицинской помощи, по желанию пациента, или гражданам, обеспечение которых бесплатными медицинскими услугами не предусмотрено законодательством Российской Федерации (гражданам иностранных государств, лицам без гражданства).
Позвоните нам сегодня, чтобы мы смогли Вам помочь!
Москва, 8 (499) 110 — 40 — 67
Нарушение ритма сердца и проводимости (аритмии сердца)
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
Практически у 80% пациентов с ишемической болезнью сердца регистрируются аритмии различного характера и до 65% из них угрожают жизни. НРС могут быть самостоятельными или являться осложнением заболеваний сердечно-сосудистой системы и других органов и систем
С учетом частоты сердечных сокращений их можно подразделить на две большие группы:
1. Брадиаритмии:
2. Тахиаритмии:
Важно отличать нарушения ритма сердца, вызванные органическим (необратимым) поражением миокарда, и функциональные нарушения. Как правило, функциональные нарушения встречаются при здоровом сердце и могут быть вызваны психогенными, рефлекторными и гуморальными расстройствами. Функциональные нарушения ритма сердца встречаются достаточно часто, важно выявить и исключить вызывающие их причины, что позволит избавить человека от аритмии.
Органические нарушения возникают при: коронарной ишемии, гемодинамических пороках сердца и крупных сосудов, сердечной недостаточности, гипертонии. Они могут появляться при токсическом воздействии (медикаментозных препаратов, алкоголя и др.) или инфекционно токсическом (ревматизм, вирусные инфекции, миокардиты различной этиологии и др.), гормональных сдвигах. Аритмии бывают врожденные (синдром WPW, врожденная АВ блокада и др.) и приобретенными, вызванные внешними воздействиями (миокардит,операции и травмы сердца и др.).
Основные симптомы (проявления аритмий)
Брадиаритмии:
Тахиаритмии:
Обычно диагностика аритмий осуществляется врачом поликлиники, кардиологом или врачом скорой помощи. Имеет значение сбор анамнеза, физикальное обследование, и различные инструментально-диагностические методы. Наиболее важным является регистрация НРС на ЭКГ (для предъявления аритмологу).
На сегодняшний день в специализированных или многопрофильных клиниках пациентов консультирует врач кардиохирург-аритмолог и определяет необходимость и возможность эндоваскулярного интервенционного (малотравматичного) лечения нарушения ритма сердца. В нашей Клинике есть все необходимые ресурсы для диагностики и лечения аритмий
К методам диагностики нарушения ритма сердца относят:
Тилт-тест – проба с пассивным ортостазом. Проводится на специальном поворотном столе. Позволят выявить или исключить связь между развитием обморочных состояний и нарушениями сердечного ритма.
Лечение аритмий: хирургическая коррекция нарушений ритма сердца
В нашей Клинике выбор способа лечения нарушения ритма сердца осуществляется специа-листом с учетом клинической картины заболевания, данных инструментально-диагностических исследований и рекомендаций Российского кардиологического обще-ства, Всероссийского научного общества аритмологов.
Самостоятельный прием препаратов, самолечение различными методами является крайне не желательным и не безопасным, если неизвестен и не учитывается характер, механизм и причина аритмии.
Существует несколько способов лечения нарушения ритма сердца:
Операция выполняется под местной анестезией в условиях рентгеноперационной длительностью до 40-55 минут.
Эффективным и радикальным методом лечения тахиаритмий является катетерная аблация (деструкция) очага аритмии. Операция, в среднем, длится не более 1 часа, и через сутки пациент может быть выписан из стационара.
Состояние здоровья человека напрямую зависит от количества данных форменных элементов. Для того чтобы определить их количество, назначают общий анализ крови. С помощью полученных результатов можно наблюдать течение болезни и характер воспалительных процессов, которые могут протекать в организме. Также общий анализ крови назначают при появлении таких симптомов, как усталость, постоянные головные и мышечные боли, утомляемость.
Для чего назначают общий анализ крови?
Кровь в организме человека выполняет ряд важных функций, поэтому ее состав очень информативен при диагностике возможных заболеваний. Чаще всего во время планового обследования назначается общий анализ крови. При подозрительных результатах назначается развернутый биохимический анализ.
Процедура сдачи общего анализа крови
Перед визитом в клинику не рекомендовано принимать пищу. Также в течение нескольких дней следует прекратить прием медикаментов (только по рекомендации врача). Процедура проводится утром. Забор крови делают из пальца или вены.
Таблица – Нормы общего анализа крови для взрослых
Из таблицы выше следует что, нормы анализа крови у мужчин и женщин отличаются. Во время беременности также изменяются показатели анализа крови.
Гемоглобин
Гемоглобин – это белок, в составе которого имеются ионы железа. Он отвечает за дыхательную функцию крови и производит газообмен между клетками организма.
Если у человека обезвоживание организма, сердечная недостаточность; имеются проблемы с пищеварением, вследствие чего была рвота и диарея – то анализ покажет пониженный уровень гемоглобина.
При повышенном уровне речь идет о закупорке сосудов за счет того, что кровь становится гуще. Из-за этого образуются тромбы, что повышает риск развития сердечно-сосудистых заболеваний.
После рассмотрения результатов анализов должно быть подобрано соответствующее лечение для улучшения показателей. Самолечение в данном случае недопустимо.
Эритроциты
Если человек испытывает стресс, сидит на изнуряющих диетах, которые сочетаются с высокими физическими нагрузками, то уровень эритроцитов будет понижен.
Для коррекции происходящих в организме нарушений назначаются лекарства. Препарат должен быть подобран врачом с учетом результатов проведенных исследований и особенностей организма пациента.
Если при расшифровке биохимического анализа крови СОЭ выше нормы, то это говорит о том, что в организме идут инфекционные и воспалительные процессы, также возможны онкологические заболевания.
Снижение уровня СОЭ свидетельствует о болезнях, сопровождающиеся изменениями формы эритроцитов, например серповидно-клеточная анемия.
Лейкоциты
В норме общее количество лейкоцитов в крови находится в диапазоне 4х109/л до 1,1х1010 /л. Лейкоциты – это форменные элементы крови. Если количество выше нормы, то это указывает на то, что в организме происходит воспалительный процесс. Причины повышения лейкоцитов могут быть следующие: острые инфекции, онкологические заболевания, острое и хроническое воспаление.
Чтобы осуществить подсчет процентного соотношения лейкоцитов разных видов в лабораторной диагностике используют лейкоцитарную формулу. Если из результатов биохимического анализа крови видно, что идет сдвиг лейкоцитарной формулы влево, это значит, что в крови находятся незрелые нейтрофилы. Хотя в норме они должны быть только в костном мозге.
Тромбоциты
Образование тромбоцитов идет в красном костном мозге. Норма у женщин составляет 170,0-320,0х109/л и у мужчин 180,0-320,0х109/л.Туберкулез, рак печени и почек, острые инфекции, отравления, стресс провоцируют повышенное содержание тромбоцитов при расшифровке общего анализа крови.
Пониженное содержание тромбоцитов при расшифровке анализа наблюдается при частом приеме лекарственных препаратов. Низкий уровень тромбоцитов наблюдается также у людей, страдающих алкоголизмом. Если при расшифровке показателей анализа у женщин наблюдается низкий уровень тромбоцитов, то это может говорить о затяжных менструациях.
Гематокрит
При расшифровке биохимического анализа крови особое место выделяют такому показателю, как гематокрит. Он указывает на отношение объема клеток крови к общему объему крови и выражается в процентах.
У женщин низкий уровень гематокрита может говорить о наступлении беременности. Биохимические исследования крови являются важным показателем при установке диагноза пациента и назначении лечения. Сдавать общий анализ крови рекомендовано не только при возникновении недомоганий, но и в целях диагностики организма на отсутствие болезней.
Интерпретация полученных результатов проводится на приеме у врача, который назначил анализ. Специалист учитывает половую принадлежность и возраст пациента. На основании полученных данных врач разрабатывает индивидуальную схему лечения.
Самостоятельная расшифровка полученных результатов может привести к получению ложного представления о диагнозе. Без определенных знаний невозможно определить состояние здоровья даже при наличии результатов анализа крови. Доверяйте расшифровку результатов лабораторных исследований опытным специалистам.
Главное меню
Главное меню
Экстракорпоральная резекция врожденной единственной почки с тромбэктомией из нижней полой вены с ортотопической реплантацией сосудов почки при раке почки
Злокачественные новообразования почки (ЗНП) в 2013 году составили 3,9% всех злокачественных новообразований населения РФ, занимая 10 ранговое место в структуре онкологической заболеваемости обоих полов. Абсолютное число больных с впервые в жизни установленным диагнозом ЗНП в РФ в 2013 году составило 11 442 человек. Прирост заболеваемости за 10 лет был равен 41%, стандартизированный показатель заболеваемости – 9,39 на 100 000 человек [1, 2].
Рак врожденной единственной почки встречается крайне редко. Частота аплазии почки по данным аутопсий составляет 1 на 1100. Ультразвуковое скрининговое исследование 280 000 детей школьного возраста выявило подобную частоту встречаемости 1 на 1200 (0,083%) [3, 4].
Стандартом хирургического лечения рака почки долгое время считалась радикальная нефрэктомия (РНЭ). Однако у больных, перенесших РНЭ, в большем проценте случаев, по сравнению с резекцией почки, развивается хроническая почечная недостаточность (ХПН), повышается риск развития сердечнососудистых заболеваний (ССЗ) и смерти 7.
Анализируя результаты лечения более 1 миллиона пациентов в США, A.S. Go и соавт. установили, что значительное снижение функции почек ассоциируется с увеличением заболеваемости ССЗ и смертности от них, а также с повышением частоты госпитализаций по разным причинам [8]. Исторически считалось, что, поскольку большинство доноров почки на протяжении длительного времени после удаления органа чувствуют себя хорошо, то нефрэктомия у пациентов опасности также не представляет. Современные взгляды это представление более не разделяют. Данные, полученные P. Koenig, показывают, что у больных почечно-клеточным раком (ПКР) вероятность развития ХПН больше, чем у здоровых доноров [9]. Кроме того, J. McKiernan продемонстрировал развитие ХПН у трети больных ПКР еще до лечения [10]. Несмотря на значительные успехи в заместительной терапии почечной недостаточности (ЗТПН) с использованием таких методов как диализ или трансплантация, ЗТПН остается значимой причиной появления других заболеваний и смертности от них. У пациентов, находящихся на длительном гемодиализе, смертность от ССЗ в 10-30 раз выше, чем в общей популяции [11]. При анализе смертности от инфаркта миокарда R.N. Foley и соавт. отметили, что общая выживаемость пациентов на диализе значительно меньше, чем у пациентов без ХПН или даже при наличии сопутствующих болезней [12]. Согласно базе данных США по заболеваниям почек (USRDS) смертность у больных на диализе составляет 22% в первые два года после начала его применения и 15% во время последующих трех лет. M. Rocco и соавт. показали, что в стационарном лечении нуждаются более 50% больных, находящихся на хроническом диализе. Несмотря на стационарное лечение около 20% больных погибают [13]. При этом необходимо отметить высокую стоимость диализа: только в США выделяется около 70000$ в год на одного пациента [14].
Трансплантация почки является жизненно важной для некоторых пациентов, но и она сопряжена с рисками. Согласно современным рекомендациям трансплантацию почки в случае ПКР можно проводить через 2 года безрецидивного периода [15]. Это вынуждает пациентов ждать, получая диализ не менее двух лет. Кроме того, недостаточное количество аллогенных трансплантантов может привести к увеличению периода ожидания трансплантации и сроков проведения гемодиализа. При этом, несмотря на очевидные достижения в трансплантации, от 20 до 33% трансплантатов функционируют не более 5 лет [11, 16]. Согласно результатам некоторых исследований 5-летняя выживаемость после трансплантации составляет только 75% [13, 16]. Поскольку в этих исследованиях эффективность диализа и трансплантации изучалась в группе пациентов с множеством сопутствующих заболеваний, результаты ЗТПН в группе пациентов с ПКР без серьезной сопутствующей патологии могут отличаться. Тем не менее, осложнения длительной заместительной терапии являются очевидными.
Следует обсудить отдельную, сложную группу больных с опухолями единственной почки больших размеров, являющихся потенциально резектабельными. Для таких пациентов выполнение резекции почки является единственно возможным методом сохранения почечной функции и возможность избежать перевода в ренопривное состояние. Зачастую таким больным отказывают в выполнении оперативных вмешательств. Однако выявление опухоли единственной или единственно функционирующей почки не должно быть причиной отказа от оперативного лечения, так как только активная хирургическая тактика у этой категории больных позволяет добиться продления их жизни, а в ряде случаев – излечения. Выполнение таким пациентам экстракорпоральной резекции почки (ЭКРП) с последующей ее аутотрансплантацией является наиболее перспективным, а порой и единственно возможным методом лечения.
Представляем клиническое наблюдение органосохраняющего оперативного лечения ex vivo почечно-клеточного рака врожденной единственной почки с интралюминальной инвазией (подпеченочная форма).
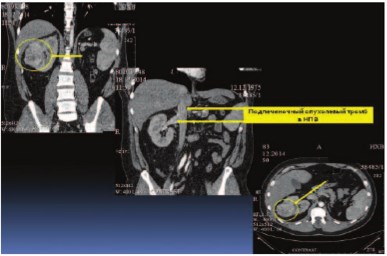
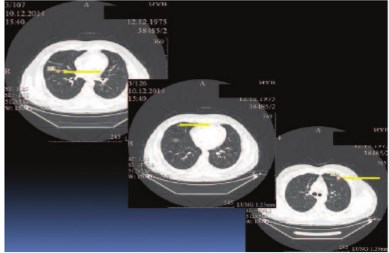
Больной К., 38 лет, госпитализирован в урологическую клинику Института хирургии им. А.В. Вишневского с жалобами на постоянный вечерний субфебрилитет. Обследовал-ся по месту жительства по поводу лихорадки неясного генеза в течение трех месяцев. При ультразвуковом исследовании (УЗИ) впервые в жизни была выявлена аномалия развития мочевыводящей системы: единственная правая почка. По данным мультиспиральной компьютерной томографии (МСКТ), магнитно-резонансной томографии (МРТ), УЗИ диагностировано объемное образование единственной правой почки, размерами 65х70х68 мм, активно накапливающее контрастный препарат в артериальную фазу до 97 ед. Н. У больного выявлена интралюминальная опухолевая инвазия в нижнюю полую вену (НПВ): в ее просвете, начиная от уровня устья почечной вены, определяются тромботические массы с четкими контурами, протяженностью до 50 мм, распространяющиеся антеградно, занимающие большую часть просвета вены. Окрашиваемый просвет вены определялся диаметром 4,0 – 6,0 мм. Верхушка тромба лоцировалась в 10 мм от устьев печеночных вен. По данным МСКТ грудной клетки выявлены мелкие метастазы в обоих легких, числом 8, размерами от 2 мм (самый крупный 15 мм). Других отдаленных метастазов не выявлено (рис. 1, 2). Установлен диагноз: Аномалия развития мочевыводящей системы (АРМС). Рак единственной правой почки IV ст., сТ3вNхМ1[PUL]. Опухолевый тромб (подпеченочная форма).
Рис. 1. Мультиспиральная компьютерная томография (МСКТ) почек. Стрелками указана локализация опухоли и опухолевого тромба в нижней полой вене.
Рис. 2. Мультиспиральная компьютерная томография (МСКТ) органов грудной клетки. Стрелками указаны легочные метастатические очаги.
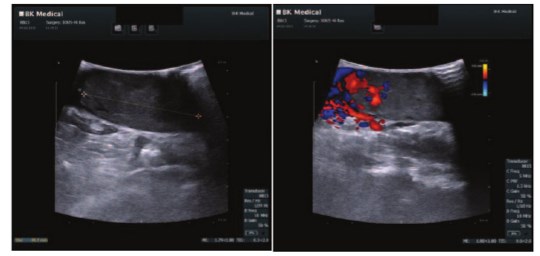
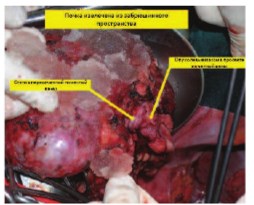
В случае реализации паллиативного оперативного пособия больной будет отнесен к группе хорошего прогноза по MSKCC (Memorial Sloan Kettering Cancer Center) с последующей таргетной терапией. Учитывая немногочисленность и размер легочных метастазов, удовлетворительное соматическое состояние больного было решено выполнить резекцию единственной правой почки ex vivo с тромбэктомией по разработанной в Институте хирургии собственной методике экстракорпоральной резекции (рис. 3, 4).
Рис. 3. Интраоперационная допплерография нижней полой вены с опухолевым тромбом
Рис.4. Почка ex vivo. Стрелками изображена почечная вена с опухолевыми тромботическими массами.
04.02.15г. пациенту выполнено оперативное вмешательство: резекция единственной правой почки ex vivo в условиях фармако-холодовой ишемии раствором Кустодиол без пересечения мочеточника с одномоментной тромбэктомией из НПВ, резекцией НПВ с ортотопической реплантацией почечных сосудов, аорто-кавальной лимфаденэктомией и установкой внутреннего стента.
Интраоперационно: имеется одна почечная артерия до 6 мм в диаметре, одна почечная вена диаметром до 25 мм. При интраоперационном допплерографическом исследовании подтверждены данные МСКТ.
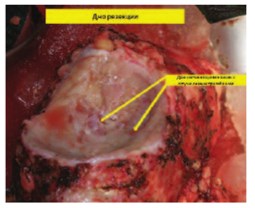
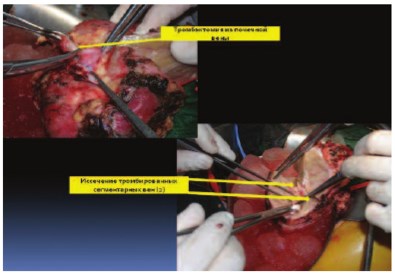
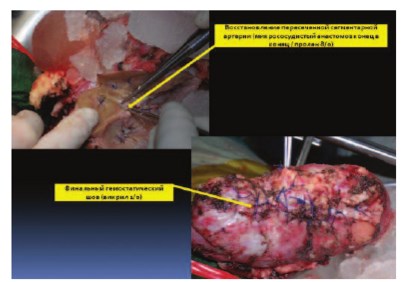
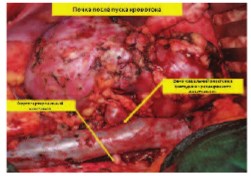
Верхушка опухолевого тромба находилась в 10 мм от устьев печеночных вен. Пересечена почечная артерия в области устья. Наложены сосудистые зажимы на стенку НПВ ниже устьев печеночных вен в инфраренальном отделе. Выполнена венотомия НПВ по линии устья с выкройкой «капюшона» из стенки НПВ в дистальном направлении. Опухолевый тромб выведен в рану. На образовавшийся дефект в НПВ наложены сосудистые зажимы. Сняты сосудистые зажимы с сосудистой изоляции НПВ. Почка сразу же извлечена из забрюшинного пространства в лоток с ледяной крошкой для налаживания перфузии охлажденным раствором Кустодиола через почечную артерию. Восстановлена целостность НПВ. Завершена перфузия 700 м раствора Кустодиола. Выполнена резекция опухоли почки в пределах здоровых тканей с отступом 2 мм от края резекции. Со стороны пересеченной почечной вены извлечен опухолевый тромб до уровня сегментарных вен. В дне резекции паренхимы почки визуализируется две пересеченные сегментарные вены до 3х3 мм с опухолевыми массами. Интрапаренхиматозная часть измененных сегментарных вен иссечена остро и отправлена на морфологическое исследование. Зияющие сосуды, дефекты в собирательной системе дна резекции почки ушиты (рис. 5-7). Полость ЧЛС дренирована стентом 7 Ch. Пересеченная нижнесегментарная почечная артерия восстановлена непрерывном микро-сосудистым проленовым швом 8\0. Паренхима почки ушиты узловыми викриловыми швами 1\0. Произведено формирование аорто-артериального (на 2 см дистальнее истинного устья почечной артерии и почечной вены), каваренального сосудистого анастомозов (пролен 5\0). После пуска кровотока перфузия почки по данным допплерографии удовлетворительная (рис. 8, 9). Гемостаз надежный. Время тепловой ишемии составило 4 минуты. Время фармако-холодовой ишемии составило 2 часа 23 минуты. На всем протяжении оперативного пособия проводилась холодовая ишемия органа ледяной крошкой с термометрией (6 литров замороженного физиологического раствора). Продолжительность операции была 8 ч 35 мин. Кровопотеря составила 700 мл (рис. 10).
Рис. 5. Почка ex vivo после резекции. Стрелками указаны сегментарные почечные вены с интралюминальными опухолевыми массами
Рис. 6. Почка ex vivo после резекции. Стрелками показана тромбэктомия из почечной вены и резекция сегментарных вен
Рис. 7. Почка ex vivo после резекции. Стрелками указан микросоудистый анастомоз пересеченной сегментарной вены и финальный гемостатичекий шов
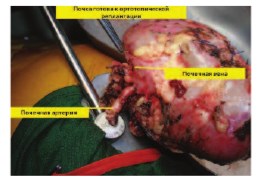
Рис. 8. Почка после восстановительного этапа резекции готова для перемещения в ортотопическую позицию
Рис. 9. Почка после пуска кровотока (удовлетворительная перфузия). Стрелками указаны зоны артерио-аортального и вено-венозного анастомозов почечных сосудов
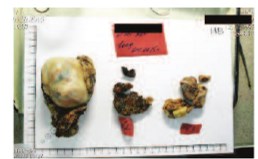
Рис. 10. Макроскопические препараты после резекции почки и регионарной лимфаденэктомии
В первые сутки после операции у больного отмечалось незначительное повышение уровня креатинина крови до 177 ммоль/л и снижение уровня гемоглобина до 93 г/л, незначительный метаболический ацидоз. Наблюдалась транзиторная анурия. В таблице 1 приведена динамика уровня креатинина, мочевины и скорость клубочковой фильтрации (СКФ).
Таблица 1. Динамика уровня сывороточного креатина, мочевины, скорость клубочковой фильтрации (СКФ)
| Дата | 03.02. | 04.02. | 05.02. | 06.02. | 07.02. | 08.02. | 09.02. | 10.02. | 13.02. |
|---|---|---|---|---|---|---|---|---|---|
| Креатинин, мкМоль/л | 112 | 177 | 291 | 386 | |||||
| Мочевина, мМоль/л | 3,54 | 5,9 | 8, 6 | 11,6 | |||||
| СКФ, мл/мин | 71 | 30 | 21 | 15 | 12 | 18 | 20 | 22 | 25 |
На 2-е сутки в отделении ОРИТ у больного сохранялось состояние анурии, которое было расценено как ОПН RIFLE-F. При допплерографии отмечена проходимость сосудистых анастомозов. На 3-и сутки после операции отмечен рост азотистых шлаков, снижение СКФ. Всего проведено 3 сеанса гемодиализа. Фаза восстановления диуреза началась с третьих суток. На 5-е сутки послеоперационного периода пациент переведен в профильное отделение. На 10-е сутки после операции по данным УЗИ почка размерами 157 х 80 мм, отчетливо прослеживается кортико-медуллярная дифференцировка, паренхиматозный слой достаточно выражен – 26,0 мм, ЧЛС не расширена, сохранен внутриорганный кровоток. На 11-е сутки после операции пациент выписан из отделения в удовлетворительном состоянии.
По данным гистологического исследования материала, полученного в ходе оперативного вмешательства, диагностирован низкодифференцированный светлоклеточный ПКР (Grade 4 по Fuhrman) с размерами опухолевого узла 7,5х6х5 см с массивными некрозами (около 25% площади всех срезов) и выраженной воспалительной инфильтрацией, участками веретеноклеточного строения, фокусами сосудистой инвазии в структуре и наличием опухолевого тромба в почечной и НПВ, без метастазов в региональные лимфатические узлы. Статус краев резекции – негативный. Патоморфологический диагноз: рак единственной правой почки pT3в pN0(0/6) cM1; M 8310/3, Grade 4; R0; Pn0; L0, V1. ИП Ki67 – около 55%.
Через 8 недель после операции пациенту была назначена таргетная терапия: бевацизумаб в дозе 10 мг\кг внутривенно 1 раз в 14 дней + интерферон альфа-2а в дозе 3 млн МЕ внутримышечно 3 раза в неделю. Через 6 месяцев после операции при контрольном обследовании у больного не выявлены признаки местного и системного прогрессирования (стабилизация метастатического процесса в легких).
ОБСУЖДЕНИЕ
Сохранение почки при распространении опухолевого процесса в почечную и тем более в нижнюю полую вену – весьма сложная и далеко не всегда выполнимая задача. В мировой литературе описано не более 20 наблюдений использования органосохраняющей техники у этих пациентов. Эти случаи в большей степени являются казуистическими, нежели отражают какую-либо сложившуюся хирургическую стратегию. Основными показаниями для выполнения органосохраняющего лечения у подобных больных является наличие опухоли единственной или единственно функционирующей почки. При этом перед врачом и пациентом стоит непростой выбор: радикальная нефрэктомия с последующим хроническим диализом, либо менее радикальная, но органосохраняющая операция, позволяющая избежать ренопривного состояния.
В мировой литературе мы обнаружили четыре отчета, которые посвящены проблеме лечения этих больных. Первое исследование было проведено в 1990 году группой авторов из Кливленда во главе с K.W. Angermeier и A.C. Novick. Авторами были оценены результаты органосохраняющих операций 10 пациентов с ПКР и сосудистой инвазией. Билатеральное опухолевое поражение имело место у 6 больных, опухоль единственной почки – у 4-х. Все случаи имели локализованный характер и опухоли были удалены в пределах здоровых тканей. Однако нужно учитывать один немаловажный факт – в 4-х наблюдениях отмечалась всего лишь микроскопическая венозная инвазия, в остальных 6 случаях опухоль достигала притоков или основного ствола почечной вены. У трех больных выявлена инвазия опухоли в паранефральную клетчатку. Анализ онкологических результатов показал, что 40% больных погибли от прогрессирования процесса, в среднем, через 35,5 мес. Пять пациентов оставались живыми без очевидной прогрессии заболевания при наблюдении от 5 до 88 мес. (в среднем 28,4 мес.). У 3-х из 4-х умерших имел место локальный рецидив ПКР. Авторы заключают, что органосохраняющая операция является технически возможной у пациентов с венозным распространением опухоли, однако риск рецидива у них высок [17].
В 1999 году R.S. Pruthi и соавт. опубликовали сообщение о больной с раком единственной правой почки, которой была выполнена резекция верхнего полюса почки и удаление опухолевого тромба, распространяющегося в подпеченочный отдел НПВ. За период наблюдения, который составил больше года, у больной не было выявлено признаков рецидива заболевания [18].
M.K. Tollefson и соавт. в 2005 году также продемонстрировали результаты органосохраняющего хирургического лечения пациента с опухолью единственной почки и неопластическим подпеченочным тромбозом. Решение о проведении этой операции было принято на основе данных МСКТ, выявившей добавочную почечную вену [19].
Анализ результатов лечения 13 больных с опухолью единственной почки в стадии рТ3в, находившихся на лечении в клинике Mayo, представлен в 2005 году S. Sengupta и соавт. [20]. Резекции почки успешно выполнены у 7 больных, один больной умер во время операции от тромбоэмболии легочной артерии. Остальным 5 пациентам произведена радикальная нефрэктомия, у двух из них сначала была выполнена резекция почки. Причинами выполнения в дальнейшем нефрэктомии послужили кровотечение, большие размеры внутрипочечного образования, а также малые размеры остающейся части органа и инвазия опухоли венозную стенку. Рассматривая спектр органосохраняющих вмешательств, необходимо отметить, что в 4-х случаях операции проводились in situ, тогда как в трех наблюдениях ex vivo с аутотрансплантацией почки. В 11 случаях опухолевая инвазия ограничивалась почечной веной. В двух случаях опухоль распространялась в подпеченочный отдел НПВ. У трех пациентов отмечались серьезные осложнения после резекции почки: мочевой свищ, эвентерация, гемоперитонеум, необходимость установки кава-фильтра из-за легочной эмболии и интимэктомия артерии аутотрансплантата. В двух случаях возник острый тубулярный некроз, потребовавший несколько сеансов гемодиализа. Четверо больных умерли от прогрессирования заболевания в среднем через 9,5 мес. (всем пациентам были выполнены органосохраняющие операции), еще 4 погибли по причинам не связанным с наличием опухоли почки. Пять больных живы при медиане наблюдения 25 мес. (8-204 мес.). При этом у одного из них имеется прогрессирование заболевания.
До сих пор сложным остается вопрос о приоритете лечебной тактики у подобных больных: органосохраняющая или органоуносящая операция? По данным мировой литературы в большинстве случаев проводится нефрэктомия, которая рассматривается как стандарт лечения. Это обосновывается следующим: во-первых, резекция опухоли с тромбэктомией – более длительная и сложная операция, чем нефрэктомия; во-вторых, она значительно чаще сопровождается осложнениями (15-30%); в-третьих, онкологические результаты нефрэктомии с последующим гемодиализом оказались прогностически лучше [21, 22].
Хотя большая часть локальных рецидивов и смертей, связанных с ПКР наблюдалась в группе органосохраняющих операций, в настоящее время делать выводы еще преждевременно, т.к. количество больных небольшое, а резекция почки зачастую использовалась у больных с регионарными и отдаленными метастазами или стадией Т2-Т3. До сих пор остается открытым вопрос – насколько нефрэктомия продлевает жизнь по сравнению с органосохраняющей операцией. S. Sengupta и соавт. считают оба метода эквивалентными по эффективности [20]. Нельзя забывать и о проблемах, связанных с хроническим гемодиализом, включающих осложнения, низкое качество жизни пациентов и высокую смертность [23, 24]. С уверенностью можно констатировать только одно – органосохраняющая хирургия может успешно использоваться для лечения пациентов с опухолью единственной почки и неопластическим тромбозом. Показания к данному хирургическому пособию еще предстоит разработать.
ЗАКЛЮЧЕНИЕ
В работе описан редкий клинический случай пациента с диагнозом: АРМС. Рак единственной правой почки IV стадии, рТ3вN0М1[PUL], интралюминальная инвазия (подпеченочная форма). Пациенту успешно выполнено органосохраняющее оперативное пособие с морфологически подтвержденным местным радикальным эффектом. Использовался метод резекции почки ex vivo, разработанный в урологической клинике Института хирургии им. А.В. Вишневского. Данный случай демонстрирует широкие возможности сложной техники оперативного пособия: экстракорпоральной резекции почки в условиях фармако-холодовой ишемии без пересечения мочеточника с ортотопической реплантацией почечных сосудов при ПКР, что позволяет избежать ренопривного состояния как в процессе ожидания трансплантации почки, так и в процессе таргетной терапии.
ЛИТЕРАТУРА
1. Каприн А.Д., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2013 году. М., 2015. С. 9-15.
2. Широкорад В.И., Махсон А.Н., Ядыкова О.А. Состояние онкоурологической помощи в Москве, онкоурология. 2013. №4. С.11.
3. Duroshow LW, Abeshouse BS. Congenital unilateral solitary kidney report of 37 cases and a review of the literature. // Urol Surv. 1961. Vol. 11. P. 219.
4. Sheih C P, Hung C S. Cystic dilatations within the pelvis in patients with ipsilateral renal agenesis or dysplasia. // J Urol. 1990. Vol. 144 (2 Pt 1). P. 324-327.
5. Bratslavsky G, Boris RS. Emerging Strategies of Nephron Sparing Surgery in Patients with Localized and Recurrent Renal Cell Carcinoma. // Malign Tumours 2010. Vol. 1. P. 5-14. 6. Gill I. Laparoscopic radical nephrectomy for cancer. // Urol Clin. 2000. Vol. 27. Р. 707-719.
7. Клиническая онкоурология. [Под редакцией профессора Б.П. Матвеева] 2011. М.: ООО «Издательский дом «АБВ-пресс». С.76-77.
8. Go AS, Chertow GM, Fan D, McCulloch CE, Hsu CY. Chronic kidney disease and the risks of death, cardiovascular events, and hospitalization. // N Engl J Med. 2004. Vol. 351. P. 1296.
9. Koenig P, Gill IS, Kamoi K, Aron M, Haber G, Singh AB, Weight CJ, Desai MM, Kaouk JH, Goldfarb DA, Poggio ED. Kidney cancer and the risk for chronic kidney disease: matched-paired comparison with living donors. // Jour Urol. 2008. Vol. 179. P. 170.
10. McKiernan J, Simmons R, Katz J, Russo P. Natural history of chronic renal insufficiency after partial and radical nephrectomy. // Urol. 2002. Vol. 59. P. 816.
11. System U. S. R. D.: Annual Data Report. National Institute of Diabetes and Digestive and Kidney Diseases (NIDDK), National Institutes of Health (NIH), and US Department of Health and Human Services (DHHS). // 2007
12. Foley RN, Parfrey PS, Sarnak MJ. Clinical epidemiology of cardiovascular disease in chronic renal disease. // Am J Kidney Dis. 1998. Vol. 32. P. 112.
13. Rocco M, Frankenfield DL, Hopson SK, McClellan WM. Relationship between clinical performance measures and outcomes among patients receiving long-term hemodialysis. // Ann Intern Med. 2006. Vol. 145. P. 512.
14. Neil N, Guest S, Wong L, Inglese G, Bhattacharyya SK, Gehr T. The financial implications for Medicare of greater use of peritoneal dialysis. // Clin fter. 2009. Vol. 31. P. 880.
15. Kasiske BL, Cangro CB, Hariharan S, Hricik DE, Kerman RH, Roth D. The evaluation of renal transplantation candidates: clinical practice guidelines. // 2001. Am J Transplant. 2001. 1 Suppl 2. P. 3. 16. Lin SJ. The association between length of post-kidney transplant hospitalization and long-term graft and recipient survival. // Clin Transplant. 2006. Vol. 20. P. 245.
17. Angermeier KW, Novick AC, Streem SB, Montie JE. Nephron-sparing surgery for renal cell carcinoma with venous involvement. // Journal of Urology. 1990. Vol. 144, N 6. P. 1352-1355. 18. Pruthi RS, Angell SK, Brooks JD, Gill H. Partial nephrectomy and caval thrombectomy for renal cell carcinoma in a solitary kidney with an accessory renal vein. // BJU Int. 1999. Vol. 83. P.142-143.
19. Tollefson MK, Kawashima A, Blute ML. In situ partial nephrectomy and tumor thrombectomy for renal cell carcinoma wiyh level 11 vena cava extension in a solitary kidney. // Urology. 2005. Vol. 66, N 4. P.882.
20. Sengupta Sh, Zinke H, Leibovich BC and Blute ML. Surgical treatment of stage pT3b renal cell carcinova in solitary kidneys: a case sries. // BJU Int. 2005. Vol. 96. P. 54-57.
21. Stephenson AJ, Hakimi AA, Snyder ME and Russo P. Complications of radical and partial nephrectomy in a large contemporary cohort. // J Urol. 2004. Vol. 171. P. 130-134.
22. Campbell SC, Novick AC, Streem SB, Klein E, Licht M. Complications of nephron sparing surgery for renal tumors. // J Urol. 1994. Vol. 151. P. 1177–1180.
23. Thomas N. Measurement of quality of life for elderly people on dialysis. // Br J Nurs. 1992. Vol. 1. P. 284-285.
24. Okechukwu CN, Lopes AA, Stack AG. Impact of years of dialysis therapy on mortality risk and the characteristics of longer term dialysis survivors. // Am J Kidney Dis. 2002. Vol. 39. P. 533-538.